Гипосульфита натрия: инструкция по применению, аналоги, статьи » Справочник ЛС
Натрия тиосульфат 30%/10 мл №10 р-р д/ин.амп.
УТВЕРЖДЕНА
Приказом председателя
Комитета контроля медицинской и
фармацевтической деятельности
Министерства здравоохранения
Республики Казахстан
от «____»______________20 г.
№ ______________
Инструкция по медицинскому применению
лекарственного средства
Натрия тиосульфат
Торговое название
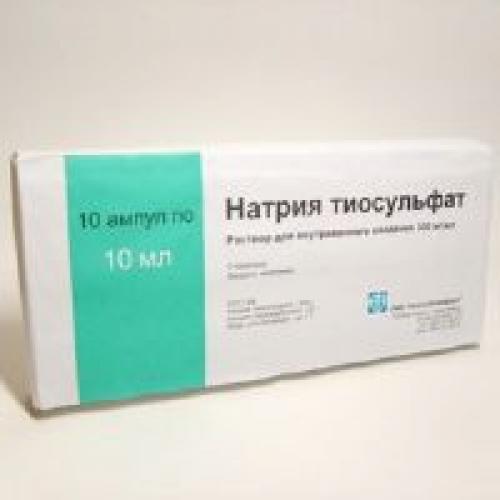
Натрия тиосульфат
Международное непатентованное название
Нет
Лекарственная форма
Раствор для внутривенного введения 300 мг/мл, 10 мл
Состав:
1 л раствора содержит
активное вещество: натрия тиосульфат — 300 г,
впомогательные вещества: натрия гидрокарбонат, вода для инъекций.
Описание
Прозрачная бесцветная жидкость
Фармакотерапевтическая группа
Другие терапевтические продукты. Антидоты.
Код АТС V03AВ06
Фармакологические свойства
Фармакокинетика
После внутривенного введения распространяется во внеклеточной жидкости.
Выводится из организма с мочой. Период полувыведения составляет 0,65 часа.
Фармакодинамика
Комплексообразующее средство.
Оказывает дезинтоксикационное, противовоспалительное, десенсибилизирщее действие, обезвреживает препараты галоидов (йод). При отравлении соединениями мышьяка, ртути, свинца образует неядовитые сульфиты. При отравлении цианидами образует менее ядовитые роданистые соединения. В кислой среде разлагается с образованием серы и сернистого ангидрида, которые оказывают противопаразитарное действие.
Показания к применению
В комплексной терапии:
— аллергических заболеваний
— невралгии
— диабетической полинейропатии
— артритов.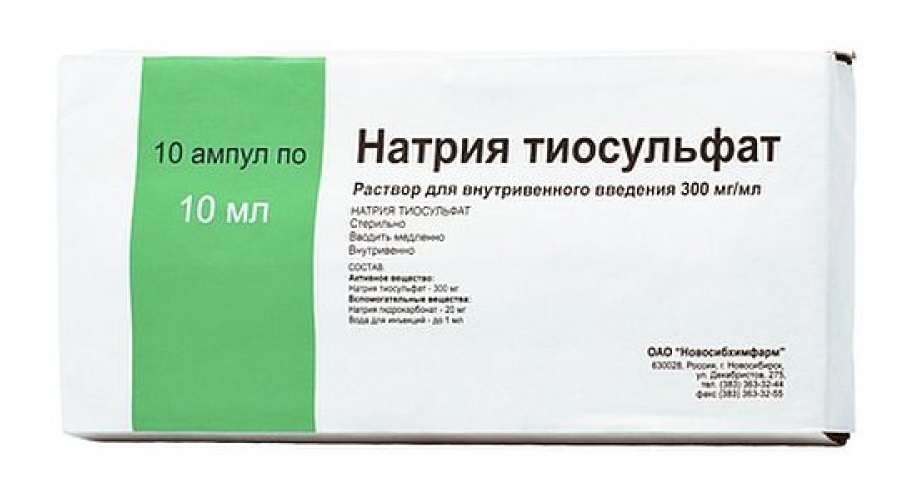
Способ применения и дозы
Внутривенно медленно по 5-10 мл раствора 300 мг/мл (в зависимости от тяжести интоксикации), при поражениях цианистыми соединениями – по 50 мл раствора 300 мг/мл.
Побочные действия
— аллергические реакции.
Противопоказания
Лекарственные взаимодействия
Категорически нельзя допускать контакта натрия тиосульфата с нитратами, перманганатом калия.
Особые указания
При отравлении цианидами рекомендуется одновременное назначение натрия гипосульфита и натрия нитрита.
Применение в педиатрии
Опыт применения препарата у детей отсутствует.
Применение при беременности и в период лактации
При беременности и в период лактации препарат применяют исключительно по жизненным показаниям, когда ожидаемая польза для матери превышает риск для плода/ребенка.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Не влияет
Передозировка
Случаи передозировки неизвестны.
Форма выпуска и упаковка
Раствор для внутривенного введения 300 мг/мл.
По 10 мл в ампулы.
По 10 ампул с инструкцией по применению на государственном и русском языках и скарификатором ампульным в коробке из картона.
По 5 или 10 в контурную ячейковую упаковку из пленки поливинилхлоридной с инструкцией по медицинскому применению на государственном и русском По 1 или 2 контурных ячейковых упаковок вместе с инструкцией по применению на государственном и русском языках и скарификатором ампульным помещают в пачку из картона.
При упаковке ампул с кольцом излома или точкой надлома скарификатор ампульный не вкладывают.
Условия хранения
Хранить в защищенном от света месте при температуре от 5 до 25 ºС.
Хранить в недоступном для детей месте!
Срок хранения
5 лет.
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту.
Производитель
ОАО «Новосибхимфарм»
630028, Россия, г.Новосибирск, ул.Декабристов, 275
тел. (383)363-32-44,
факс (383) 363-32-55
Владелец регистрационного удостоверения
Адрес организации, принимающей претензии на территории Республики
Казахстан от потребителей по качеству продукции (товара):
ТОО «Валента Азия», г. Алматы, пр. Абая, уг.ул. Радостовца, 151/115, бизнес-
центр «Алатау» офис №702
Тел./факс 8727 334-15-52, Е-mail: [email protected]
Продукты убоя птицы, полуфабрикаты из мяса птицы и объекты окружающей производственной среды. Методы отбора проб и подготовка к микробиологическим исследованиям – РТС-тендер
ГОСТ 7702.2.0-2016
МКС 67.120.20
Дата введения 2018-01-01
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН «Всероссийским научно-исследовательским институтом птицеперерабатывающей промышленности» — филиалом Федерального государственного бюджетного научного учреждения Федерального научного центра «Всероссийский научно-исследовательский и технологический институт птицеводства» Российской академии наук (ВНИИПП)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 28 июня 2016 г. N 49)
N 49)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономразвития Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | Росстандарт |
(Поправка. ИУС N 6-2019).
4 Приказом Федерального агентства по техническому регулированию и метрологии от 8 сентября 2016 г. N 1091-ст межгосударственный стандарт ГОСТ 7702.2.0-2016 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2018 г.
5 ВЗАМЕН ГОСТ 7702.2.0-95
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты».
ВНЕСЕНА поправка, опубликованная в ИУС N 6, 2019 год
Поправка внесена изготовителем базы данных
1 Область применения
1.1 Настоящий стандарт распространяется на продукты убоя птицы (тушки, части тушек, жир-сырец, кожу, субпродукты, мясо птицы механической обвалки, кость птицы пищевую, сырье коллагенсодержащее), предназначенные для пищевых целей, полуфабрикаты из мяса птицы (далее — продукт) и объекты окружающей производственной среды (технологическое оборудование, тара, инвентарь, стены и полы производственных цехов, воздух в производственных цехах, одежда и поверхность рук работников) и устанавливает отбор проб методами: смыва ополаскиванием; протирания; вырезания (иссечения) кусочков ткани продукта; смыва с объектов окружающей производственной среды, обследование воздуха в производственных помещениях седиментационным и аспирационным методами, а также подготовку к микробиологическим исследованиям.
1.2 Отбор проб проводят с целью производственного контроля на предприятиях, где проводится убой птицы и/или переработка продуктов убоя птицы.
1.3 Отбор проб методом вырезания (иссечения) кусочков тканей продуктов убоя птицы и полуфабрикатов из мяса птицы проводят для испытания их по показателям микробиологической безопасности.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 171-81* Дрожжи хлебопекарные прессованные. Технические условия
________________
* В Российской Федерации действует ГОСТ Р 54731-2011 «Дрожжи хлебопекарные прессованные. Технические условия».
ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
ГОСТ 2493-75 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 3145-84 Часы механические с сигнальным устройством. Общие технические условия
ГОСТ 3164-78 Масло вазелиновое медицинское. Технические условия
ГОСТ 4147-74 Реактивы. Железо (III) хлорид 6-водный. Технические условия
ГОСТ 4148-78 Реактивы. Железо (II) сернокислое 7-водное. Технические условия
ГОСТ 4159-79 Реактивы. Йод. Технические условия
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4201-79 Реактивы. Натрий углекислый кислый. Технические условия
ГОСТ 4209-77 Реактивы. Магний хлористый 6-водный. Технические условия
ГОСТ 4232-74 Реактивы. Калий йодистый. Технические условия
ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
ГОСТ 4530-76 Реактивы. Кальций углекислый. Технические условия
ГОСТ 4919.1-77 Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов
ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия
ГОСТ 5789-78 Реактивы. Толуол. Технические условия
ГОСТ 5833-75 Реактивы. Сахароза. Технические условия
ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ 6038-79 Реактивы. D-глюкоза. Технические условия
ГОСТ 6672-75 Стекла покровные для микропрепаратов. Технические условия
ГОСТ 6691-77 Реактивы. Карбамид. Технические условия
Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 6824-96 Глицерин дистиллированный. Общие технические условия
ГОСТ ISO 7218-2015 Микробиология пищевых продуктов и кормов для животных. Общие требования и рекомендации по микробиологическим исследованиям
ГОСТ 7702.2.6-2015 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы выявления и определения количества сульфитредуцирующих клостридий
ГОСТ 7702.2.7-2013 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы выявления бактерий рода Proteus
ГОСТ 8273-75 Бумага оберточная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия
ГОСТ 9285-78 (ИСО 992-75, ИСО 995-75, ИСО 2466-73) Калия гидрат окиси технический. Технические условия
ГОСТ 9412-93 Марля медицинская. Общие технические условия
ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
ГОСТ 10444.12-2013 Микробиология пищевых продуктов и кормов для животных. Методы выявления и подсчета количества дрожжей и плесневых грибов
ГОСТ 10929-76 Реактивы. Водорода пероксид. Технические условия
ГОСТ 11078-78 Натр едкий очищенный. Технические условия
ГОСТ ISO/TS 11133-1-2014 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству питательных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления питательных сред в лаборатории
ГОСТ ISO 11133-2-2011 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству питательных сред. Часть 2. Практические руководящие указания по эксплуатационным испытаниям питательных сред
ГОСТ 11293-89 Желатин. Технические условия
ГОСТ 11773-76 Реактивы. Натрий фосфорно-кислый двузамещенный. Технические условия
Натрий фосфорно-кислый двузамещенный. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 12302-2013 Пакеты из полимерных пленок и комбинированных материалов. Общие технические условия
ГОСТ 13805-76 Пептон сухой ферментативный для бактериологических целей. Технические условия
ГОСТ 17206-96 Агар микробиологический. Технические условия
ГОСТ 19126-2007 Инструменты медицинские металлические. Общие технические условия
ГОСТ 21240-89 Скальпели и ножи медицинские. Общие технические требования и методы испытаний
ГОСТ 21241-89 Пинцеты медицинские. Общие технические требования и методы испытаний
ГОСТ 22180-76 Реактивы. Кислота щавелевая. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 25706-83 Лупы. Типы, основные параметры. Общие технические требования
ГОСТ 26669-85 Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов
ГОСТ 27068-86 Реактивы. Натрий серноватистокислый (натрия тиосульфат) 5-водный. Технические условия
ГОСТ 27543-87 Изделия кондитерские. Аппаратура, материалы, реактивы и питательные среды для микробиологических анализов
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 29228-91 (ИСО 835-2-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 2. Пипетки градуированные без установленного времени ожидания
ГОСТ 30425-97 Консервы. Метод определения промышленной стерильности
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
ГОСТ 31468-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Метод выявления сальмонелл
ГОСТ 31473-2012 Мясо индеек (тушки и их части). Общие технические условия
Общие технические условия
ГОСТ 31490-2012 Мясо птицы механической обвалки. Технические условия
ГОСТ 31654-2012 Яйца куриные пищевые. Технические условия
ГОСТ 31657-2012 Субпродукты птицы. Технические условия
ГОСТ 31659-2012 (ISO 6579:2002) Продукты пищевые. Метод выявления бактерий рода Salmonella
ГОСТ 31746-2012 (ISO 6888-1:1999; ISO 6888-2:1999; ISO 6888-3:2003) Продукты пищевые. Методы выявления и определения количества коагулазоположительных стафилококков и Staphylococcus aureus
ГОСТ 31747-2012 (ISO 4831:2006, ISO 4832:2006) Продукты пищевые. Методы выявления и определения количества бактерий группы кишечных палочек (колиформных бактерий)
ГОСТ 31797-2012 Мясо. Разделка говядины на отрубы. Технические условия
ГОСТ 31936-2012 Полуфабрикаты из мяса и пищевых субпродуктов птицы. Общие технические условия
ГОСТ 31962-2013 Мясо кур (тушки кур, цыплят, цыплят-бройлеров и их части). Технические условия
ГОСТ 31990-2012 Мясо уток (тушки и их части). Общие технические условия
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины, определения и сокращения
3.1 В настоящем стандарте применены следующие термины с соответствующими определениями:
3. 1.1 продукты убоя птицы: Пищевая продукция в сыром виде, не подвергнутая тепловой обработке, полученная в результате промышленного убоя птицы и предназначенная для дальнейшей переработки (обработки) и/или для реализации, включающая потрошенные тушки птицы, их части, жир-сырец, кожу тушки птицы, обработанные субпродукты, мясо птицы механической обвалки, кость птицы пищевую, сырье коллагенсодержащее птицы.
1.1 продукты убоя птицы: Пищевая продукция в сыром виде, не подвергнутая тепловой обработке, полученная в результате промышленного убоя птицы и предназначенная для дальнейшей переработки (обработки) и/или для реализации, включающая потрошенные тушки птицы, их части, жир-сырец, кожу тушки птицы, обработанные субпродукты, мясо птицы механической обвалки, кость птицы пищевую, сырье коллагенсодержащее птицы.
3.1.2 сырье коллагенсодержащее птицы: Продукт убоя птицы (ноги, кисти крыльев, хрящи, кость птицы пищевая), в состав которого входят ткани, являющиеся источником получения коллагенсодержащих продуктов.
3.1.3 объекты окружающей производственной среды: Технологическое оборудование, тара, инвентарь, стены и полы производственных цехов, воздух в производственных цехах, одежда и поверхность рук работников.
3.2 В настоящем стандарте приведены следующие сокращения:
МПМО — мясо птицы механической обвалки.
КМАФАнМ — количество мезофильных аэробных и факультативно-анаэробных микроорганизмов.
БГКП — бактерии группы кишечной палочки (колиформы).
4 Требования безопасности
4.1 Требования безопасности при работе с микроорганизмами — по ГОСТ ISO 7218; с химическими реактивами — по ГОСТ 12.1.007; требования пожарной безопасности — по ГОСТ 12.1.004, с электрооборудованием по документу, действующему на территории государства, принявшего стандарт.
4.2 Требования к персоналу — по ГОСТ ISO 7218.
5 Аппаратура, оборудование, материалы, реактивы
5.1 Общие требования к аппаратуре, оборудованию, материалам, реактивам — по ГОСТ ISO 7218, ГОСТ 31467.
5.2 При отборе проб и подготовке к микробиологическим исследованиям используют следующие аппаратуру, оборудование, материалы и реактивы.
Бокс биологической безопасности по ГОСТ ISO 7218.
Весы лабораторные по ГОСТ OIML R 76-1 или по документу, действующему на территории государства, принявшего стандарт.
Ватно-марлевый тампон стерильный.
Гомогенизаторы, смесители и миксеры по ГОСТ ISO 7218.
Губки (спонжи) стерильные увлажненные забуференной пептонной водой или нейтрализующим раствором, или летиновым бульоном.
Дозатор (устройство для разливки) питательных сред и реактивов по ГОСТ ISO 7218.
Контейнеры, флаконы лабораторные для взятия проб (стерильные) с завинчивающейся крышкой.
Контейнер (сумка-холодильник).
Температурные индикаторы для контроля повышения и понижения температуры транспортировки образцов химические одноразовые на клеевой основе.
Морозильная камера по ГОСТ ISO 7218.
Ножницы медицинские по ГОСТ 19126.
Одноразовое оборудование и материалы по ГОСТ ISO 7218.
Перчатки медицинские одноразовые.
Пакеты из полимерных пленок и комбинированных материалов по ГОСТ 12302.
Пакеты для отбора проб стерильные вместимостью 6750 см, 4000 см, 1650 см, 650 см, 450 см, 355 см.
Пакеты для гомогенизации проб с фильтром и без фильтра стерильные.
Пинцеты, зажимы медицинские по ГОСТ 19126.
Пипетки и пипеточные дозаторы по ГОСТ ISO 7218.
Портативная газовая горелка.
Рамки-трафареты.
Спиртовка по ГОСТ 25336.
Скальпели медицинские по ГОСТ 19126.
Спирт этиловый по ГОСТ 5962.
Стеклограф-маркер.
Тампоны (свабы), аппликаторы в пробирке стерильные с нейтрализующим раствором или с летиновым бульоном, или с забуференной пептонной водой.
Тампоны (свабы), аппликаторы в пробирке (стерильные).
Тампоны (свабы) на палочках стерильные сухие.
Термометры и температурно-контролирующие устройства, включая автоматические записывающие устройства по ГОСТ ISO 7218.
Холодильник по ГОСТ ISO 7218.
Шпатель из нержавеющей стали медицинский по ГОСТ 19126.
Штатив металлический.
Раствор физиологический.
Вода водопроводная стерильная.
Пептонная вода.
Готовая питательная среда дипслайды (пластинка, на которую с обеих сторон нанесен слой питательной среды [неселективной или селективной]; пластинки находятся в стерильных пробирках с крышками).
Разбавители для приготовления разведений по документу, действующему на территории государства, принявшего стандарт.
Готовые разбавители для приготовления разведений с забуференной пептонной водой или с восстанавливающим разбавителем.
5.3 Допускается применение других средств измерений с метрологическими характеристиками и аппаратуры с техническими характеристиками, а также реактивов и материалов по качеству не ниже указанных в 5.2.
5.4 Подготовка аппаратуры, оборудования, материалов и реактивов — по ГОСТ ISO 7218.
6 Метод смыва ополаскиванием со всей поверхности продукта
6.1 Метод смыва ополаскиванием применяют для потрошеных тушек птицы, частей тушки, полученных в результате разделки потрошеной тушки, массой не более 1,5 кг, кусковых непанированных натуральных полуфабрикатов из мяса птицы и субпродуктов птицы.
Смыв проводят со всей поверхности продукта стерильной жидкостью — физиологическим раствором, водопроводной водой и другими разбавителями.
Отбор проб методом смыва (ополаскивания) всей поверхности проводят без обжига поверхности пробы продукта.
6.2 Отбор лабораторных проб проводят из выборки по нормативным документам на конкретную продукцию (на мясо индеек — ГОСТ 31473, мясо кур — ГОСТ 31962, мясо уток — ГОСТ 31990, мясо птицы механической обвалки — ГОСТ 31490, субпродукты птицы — ГОСТ 31657, полуфабрикаты из мяса птицы и субпродуктов птицы — ГОСТ 31936 и по документу государства, принявшего стандарт), но не менее чем с трех тушек или пяти частей тушек птицы.
Тушку птицы или ее часть, находящуюся на линии (конвейере), в перчатках помещают в одноразовый пакет. Размер пакета должен соответствовать предполагаемой массе тушки или ее части с учетом объема жидкости для смыва.
Размер пакета должен соответствовать предполагаемой массе тушки или ее части с учетом объема жидкости для смыва.
Прежде чем тушку или ее часть поместить в пакет, следует дождаться стекания с нее избытка воды. В случае если это невозможно, то тушку или ее часть, соблюдая правила асептики, перемещают с подвески конвейера на отдельные продезинфицированные подвески и оставляют до полного стекания воды, после чего помещают в пакет.
Освободив ноги тушки с подвески, тушку в пакете снимают с конвейера. Пакет с тушкой или ее частью закрывают, взвешивают, помещают на ровную поверхность, придерживая верх пакета, приоткрывают его и наливают во внутреннюю полость тушки и на поверхность тушки или ее части жидкость для смыва. Соотношение массы тушки или ее части к объему жидкости для смыва 1:1.
Допускается использовать жидкость для смыва в объеме, равном половине массы образца. Результаты количественных определений микроорганизмов, полученные при посеве 1 см смывной жидкости, в таком случае должны делиться на 2. В случае использования другого объема жидкости для проведения смыва (ополаскивания) результаты количественных определений микроорганизмов в 1 см смывной жидкости следует делить на коэффициент пересчета объема жидкости, используемой для смыва, к массе образца, при этом объем используемой жидкости должен быть достаточным для гарантированного ополаскивания всей поверхности образца.
Из пакета удаляют избыток воздуха и закрывают. Пакет с содержимым встряхивают в течение 1 мин, аккуратно держа его одной рукой за днище, другой за верх, затем переворачивают круговыми движениями для более тщательного ополаскивания внутренней и внешней поверхности тушки или ее части. Пакет ставят на ровную поверхность и, придерживая его за тушку или ее часть, открывают. Из пакета рукой в одноразовой перчатке или стерильным пинцетом, медицинским зажимом достают тушку или ее часть, избегая чрезмерного стекания жидкости в пакет. Пакет со смывной жидкостью плотно закрывают. Допускается смывную жидкость, соблюдая правила асептики, переносить из пакета в стерильный контейнер с плотной крышкой для доставки в лабораторию.
Допускается смывную жидкость, соблюдая правила асептики, переносить из пакета в стерильный контейнер с плотной крышкой для доставки в лабораторию.
6.3 Отбор проб кусковых непанированных натуральных полуфабрикатов или обработанных субпродуктов для смывов проводят, соблюдая правила асептики, без обжига поверхности пробы.
Общая масса объединенной лабораторной пробы одного наименования (для кускового мяса или обработанных субпродуктов) должна быть не менее 300 г. Пробу помещают в пакет или в предварительно взвешенный контейнер (флакон), соблюдая правила асептики. Далее следуют процедурам по 6.2.
6.4 Полученная смывная жидкость служит исходным материалом для последующих 10-кратных разведений.
6.5 Определение КМАФАнМ, БГКП и других условно-патогенных микроорганизмов проводят в 1 см смывной жидкости.
6.6 Выявление патогенных микроорганизмов (например, сальмонелл, листерий) в пробах смывов проводят в 25 см смывной жидкости.
7 Метод протирания поверхности продукта
7.1 Общие положения
Отбор проб методом протирания тампоном (свабом), губкой (спонжем) поверхности тушки или ее части, полученной в результате разделки потрошеной тушки, применяют к потрошеным тушкам или ее частям любой массы.
Смывы тампоном (свабом) или губкой (спонжем) берут с разных участков поверхности тушки или ее частей. Зоны для отбора проб смывов с тушки птицы или ее части выбирают в зависимости от поставленной задачи исследований.
Общая площадь поверхности для отбора проб методом протирания с тушек птицы малых размеров (перепелов) и части тушки должна составлять не менее 10 см, с тушек крупной птицы (кур, цыплят бройлеров, индеек, гусей, уток и др.) должна составлять не менее 100 см.
Для отбора проб методом протирания используют фламбированные проволочные металлические или разовые, стерильные, гибкие рамки-трафареты. Учитывая сложную конфигурацию поверхности тушки птицы или ее части и их размеры, используют проволочные металлические или разовые, стерильные рамки-трафареты с внутренней площадью 5, 10, 20, 50 или 100 см. После проведения отбора проб методом протирания рамку-трафарет многоразового пользования фламбируют.
Учитывая сложную конфигурацию поверхности тушки птицы или ее части и их размеры, используют проволочные металлические или разовые, стерильные рамки-трафареты с внутренней площадью 5, 10, 20, 50 или 100 см. После проведения отбора проб методом протирания рамку-трафарет многоразового пользования фламбируют.
Отбор проб методом протирания проводят с использованием стерильных, ватных, вискозных тампонов, стерильных губок (спонжей), свободных от ингибиторов, которые помещают в пробирку с жидкостью для смачивания.
Определение КМАФАнМ проводят в 1 см смывной жидкости.
Расчет КМАФАнМ проводят на 1 см поверхности пробы [например, если смыв тампоном проведен с площади 100 см, общий объем жидкости для смачивания тампона и первоначального разбавления (исходная суспензия) составил 100 см, то 1 см данной исходной суспензии соответствует 1 см исследуемой поверхности].
Выявление патогенных микроорганизмов (например, сальмонелл, листерий) проводят в 25 см смывной жидкости.
7.2 Метод протирания поверхности продукта с использованием тампона
Тампон увлажняют жидкостью для смыва. На каждую зону, выбранную для отбора проб, плотно прикладывают рамку-трафарет выбранной площади. Всю площадь внутри рамки-трафарета в горизонтальном направлении протирают смоченным в жидкости для смыва стерильным тампоном, удерживаемым предварительно фламбированным пинцетом, или тампоном, закрепленным на стержне (аппликатор). Для лучшего использования всей поверхности тампона при протирании его поворачивают, слегка надавливая на поверхность образца.
Затем тампон помещают в пробирку с 10 см жидкости для смыва.
Протирание разных участков осуществляют одним и тем же увлажненным тампоном (аппликатором).
С тушек крупной птицы протирание осуществляют двумя-пятью тампонами с площади 100 см. Все тампоны помещают в колбу со 100 см жидкости для смыва. В случае использования тампонов, закрепленных на стержне (аппликатор), стержень надламывают о внутреннюю поверхность колбы и все используемые при протирании тампоны помещают в одну колбу со 100 см жидкостью для смыва.
7.3 Метод протирания поверхности продукта с использованием губки (спонжа)
Метод протирания губкой (спонжем) применим к тушкам крупной птицы и ее частям. Отбор проб методом протирания проводят с использования стерильной губки (спонжа), помещенной в стерильный пластиковый пакет.
Пакет с губкой (спонжем) открывают и добавляют жидкость для смыва в объеме, достаточном для смачивания губки (спонжа). С внешней стороны пакета губку разминают до полного ее увлажнения. Рукой в стерильной перчатке или ручкой (в случае использования губки, закрепленной на ручке) осторожно немного приподнимают губку (спонж) над дном пакета и слегка отжимают для удаления излишней жидкости.
На каждую зону, выбранную для отбора проб, плотно прикладывают стерильную рамку-трафарет площадью 100 см. Всю площадь внутри рамки-трафарета, слегка надавливая на поверхность пробы, протирают смоченной губкой (спонжем) приблизительно 10 раз в вертикальном и 10 раз в горизонтальном направлениях. Губку (спонж) помещают в пакет. В случае использования губки, закрепленной на ручке, губку (спонж) помещают в пакет и, удерживая ее одной рукой снаружи пакета, другой рукой отсоединяют губку от ручки, которую удаляют из пакета.
В пакет добавляют жидкость для смыва до достижения общего объема жидкости 100 см. Из пакета удаляют избыток воздуха и закрывают. Добавление жидкости для смыва до достижения нужного объема допускается проводить в лаборатории.
8 Метод вырезания (иссечения) кусочков тканей
8.1 Общие положения
Отбор проб методом вырезания (иссечения) кусочков тканей из глубины продукта проводят не менее чем от трех тушек или пяти частей тушек.
Зоны для отбора проб выбирают в зависимости от поставленной задачи и конкретных методов испытаний.
Отбор проб проводят только после обжига поверхности, используя оборудование для обжига (например, портативную газовую горелку или подожженный ватно-марлевый тампон, смоченный этиловым спиртом).
В случае если продукт упакован в потребительскую тару, упаковку предварительно протирают этиловым спиртом и вскрывают с помощью стерильных ножниц и скальпеля. Продукт извлекают из упаковки, соблюдая правила асептики, и помещают горизонтально в стерильный лоток анализируемой поверхностью к верху.
Поверхность образца обжигают, удаляют поверхностный слой площадью приблизительно 4х4 см и толщиной 1 см. Из этого участка, используя стерильные скальпель и пинцет, вырезают кусочки ткани на всю глубину мышцы, не касаясь нижней части мышцы.
Для формирования объединенной пробы из попавших в выборку проб продукта одного наименования вырезают точечные пробы приблизительно в равных количествах и помещают в стерильный контейнер или пакет.
Объединенная проба должна составлять не менее 300 г съедобной части.
8.2 Отбор проб из тушки или части тушки
8.2.1 Тушку или часть тушки (полутушка, грудка, половина грудки), попавшей в выборку, помещают на стерильный лоток: тушку — спинкой вниз, а части тушек — кожей вверх. Кожу грудки или открытый участок грудной мышцы обжигают. Обожженный участок удаляют, используя стерильные скальпель и пинцет. Не касаясь нижней части мышцы, с глубины вырезают кусочки ткани. Пробу помещают в стерильный контейнер или пакет и направляют в лабораторию.
8.2.2 Отбор проб кусочков ткани от других частей тушек, попавших в выборку, проводят по 8.1.
8.2.3 Отбор проб кускового мяса, мяса птицы механической обвалки, пищевых субпродуктов птицы, полуфабрикатов из мяса птицы и пищевых субпродуктов, пищевого жира-сырца птицы, коллагенсодержащего сырья проводят от партии каждого наименования. Из разных мест, соблюдая правила асептики, отбирают не менее трех точечных проб по 10-50 г по 8.1 и 8.2.1.
8.2.4 Точечные пробы охлажденного мяса птицы механической обвалки (МПМО) отбирают не менее чем из трех мест на разной глубине куска или блока. Масса объединенной пробы должна быть не менее 1000 г. При отборе проб от замороженного в блоках МПМО необходимо учитывать, что поверхностные слои МПМО подвержены более быстрой порче, чем внутренние. Поэтому для получения представительной пробы ее отбирают вырезанием куска МПМО на всю толщину блока так, чтобы величина отношения площади отрезанной поверхности блока к объему пробы равнялась величине отношения площади поверхности всего блока к его объему. В случае блока прямоугольной формы от середины боковой поверхности и перпендикулярно ей вырезают кусок прямоугольной формы, содержащий часть верхней, нижней и одной боковой поверхности блока. Длину L, см, разреза перпендикулярно боковой поверхности вычисляют по формуле:
Масса объединенной пробы должна быть не менее 1000 г. При отборе проб от замороженного в блоках МПМО необходимо учитывать, что поверхностные слои МПМО подвержены более быстрой порче, чем внутренние. Поэтому для получения представительной пробы ее отбирают вырезанием куска МПМО на всю толщину блока так, чтобы величина отношения площади отрезанной поверхности блока к объему пробы равнялась величине отношения площади поверхности всего блока к его объему. В случае блока прямоугольной формы от середины боковой поверхности и перпендикулярно ей вырезают кусок прямоугольной формы, содержащий часть верхней, нижней и одной боковой поверхности блока. Длину L, см, разреза перпендикулярно боковой поверхности вычисляют по формуле:
, (1)
где a и b — длина и ширина блока МПМО, см.
Точечные пробы отбирают не менее чем от двух блоков МПМО. Масса объединенной пробы МПМО должна быть не менее 1000 г. В случае значительной неоднородности состояния поверхности МПМО количество отбираемых точечных проб увеличивают.
8.2.5 Субпродукты из групповой упаковки отбирают в виде трех точечных проб из разных мест каждой из двух или более единиц групповой упаковки, попавших в выборку. Масса объединенной пробы каждого наименования должна быть не менее 1000 г.
8.2.6 Точечные пробы жира-сырца, субпродуктов, содержащих кости, коллагенсодержащего сырья отбирают с учетом содержания в них съедобной части, общая масса которой в объединенной пробе должна быть не меньше 300 г (головы, ноги) или 600 г (шеи). Из каждой попавшей в выборку транспортной упаковки субпродуктов, жира-сырца, коллагенсодержащего сырья случайным образом отбирают одну единицу потребительской упаковки. Если масса продуктов в одной потребительской упаковки не превышает 1000 г, то не менее трех отобранных единиц потребительской упаковки с субпродуктами или жиром-сырцом, или коллагенсодержащего сырья целиком направляют в лабораторию.
Общая масса точечных проб жира-сырца должна быть не менее 300 г.
Отбор точечных проб субпродуктов или жира-сырца проводят ложкой, половником, пинцетом или другим инструментом, в зависимости от вида субпродукта.
8.2.7 Отбор проб кожи с тушки или части тушки проводят по документу, действующему на территории государства, принявшего стандарт.
8.2.8 Пробы исследуют на определение КМАФАнМ в 1 г продукта, а также другие виды микроорганизмов (например, сальмонелл, листерий) в 25 г продукта.
9 Методы отбора проб с объектов окружающей производственной среды
9.1 Метод отбора проб (смывов) с объектов окружающей производственной среды (технологического оборудования, тары, инвентаря, стен и полов производственных цехов, одежды и поверхности рук работников)
При оценке санитарно-гигиенического состояния оборудования, тары, инвентаря, рук работников, одежды, стен и полов производственных цехов смывы берутся с поверхностей, которые непосредственно контактируют с пищевым сырьем и готовым продуктом.
Смывы с крупного оборудования, инвентаря и тары берут с поверхности 10×10 см (100 см) стерильными увлажненными забуференной пептонной водой или нейтрализующим раствором, или летиновым бульоном (см. 5.2) ватными тампонами или ватно-марлевыми тампонами. При отборе с поверхности более 100 см следует использовать губки. Смывы с мелких объектов (поверхность которых менее 100 см) берут со всей поверхности.
При взятии смывов с ровной поверхности используют металлические рамки-трафареты, ограничивающие площадь 100 см. Перед каждым употреблением трафарет обжигают. Для ровных поверхностей допускается использовать метод отпечатков с помощью питательных сред на тест-пластинах или дипслайдов.
При взятии смывов с рук работников, смоченными ватным или марлевым тампоном тщательно проводят по ладони не менее 5 раз, протирают им пальцы, межпальцевые пространства и особенно ногтевые ложа у каждого проверяемого лица. С перчаток берут смывы только со стороны ладоней.
С перчаток берут смывы только со стороны ладоней.
Смывы с санитарной одежды берут тампоном с четырех площадок по 25 см: обследуют нижнюю часть каждого рукава и две площадки с верхней и средней частей передних пол одежды.
Смывы исследуют на наличие бактерий группы кишечных палочек (БГКП), а по мере необходимости определяют содержание КМАФАнМ на 1 см поверхности, а также другие виды микроорганизмов в случае выявления источника обсеменения продуктов (сальмонеллы, листерии, клостридии и др.).
9.2 Метод отбора проб с объекта окружающей производственной среды (воздуха в производственных помещениях)
Воздух на предприятиях обследуют седиментационным и аспирационным методами.
При седиментационном методе анализа воздуха чашки Петри (диаметром 9-10 см) с питательным агаром (для определения КМАФАнМ) и с сусло-агаром или со средой Сабуро (для определения количества колоний плесневых грибов) оставляют открытыми в течение 10 мин в трех местах обследуемого помещения, затем закрывают и инкубируют для определения КМАФАнМ при (30±1)°С в течение 72 ч, для определения дрожжей и плесневых грибов при (24±1)°С в течение 5 сут.
При обследовании воздуха аспирационным методом используются аспираторы различных видов (эксплуатация в соответствии с инструкцией к прибору).
10 Транспортирование, хранение и утилизация проб
10.1 Транспортирование, хранение и утилизацию проб проводят в соответствии с ГОСТ ISO 7218, ГОСТ 31467.
10.2 Каждая упаковка (пробирка, колба, пакет, флакон) с отобранной пробой должна быть герметично упакована и промаркирована. Отобранные пробы, направляемые для анализа вне предприятия-изготовителя, должны быть обеспечены условиями, предотвращающими нарушение упаковки, изменение состава и состояния пробы и сопровождаться актом отбора проб и заявкой на испытания по ГОСТ 31467.
11 Подготовка к микробиологическим исследованиям
11.
 1 Общие положения
1 Общие положения
Общие положения по подготовке к микробиологическим исследованиям — по ГОСТ ISO 7218.
11.2 Средства измерений, оборудование, материалы, реактивы, растворы и питательные среды
11.2.1 При подготовке к микробиологическим анализам применяют средства измерений, оборудование, материалы, реактивы, растворы и питательные среды по ГОСТ 7702.2.7, ГОСТ 7702.2.6, ГОСТ 31467, ГОСТ 31468, а также следующие.
Автоклав по ГОСТ ISO 7218.
Бутыли.
Весы лабораторные по ГОСТ ISO 7218, ГОСТ OIML R 76-1.
Дозатор для розлива питательных сред и реактивов по ГОСТ ISO 7218.
Колбы по ГОСТ 25336.
Кружка по ГОСТ 9147.
Ламинарный шкаф класса биологической безопасности II.
Баня водяная.
Лампы бактерицидные (1,5-2,5 Вт на 1 м воздуха).
Лоток.
Лупа по ГОСТ 25706.
Магнитные мешалки с подогревом до 300°С.
Материалы для упаковки посуды при стерилизации.
Петля бактериологическая.
Пинцеты медицинские по ГОСТ 21241.
Пипетки градуированные по ГОСТ 29227, ГОСТ 29228.
Пипетки Пастера.
Пробирки с поплавками (трубки Дархема).
Пробирки по ГОСТ 25336.
Пробирки агглютинационные.
Пипетки автоматические вместимостью 10, 2, 1 см по ГОСТ 29227.
Посуда одноразовая для микробиологических исследований.
Печь микроволновую для расплавления питательных сред по ГОСТ ISO 7218.
Прибор для подсчета колоний по ГОСТ ISO 7218.
рН-метр с точностью калибровки ±0,1 ед. рН при температуре от 20°С до 25°С по ГОСТ ISO 7218.
Скальпели и ножи медицинские по ГОСТ 21240.
Спиртовка по ГОСТ 25336.
Стаканы по ГОСТ 25336.
Стекла предметные по ГОСТ 9284.
Стекла покровные по ГОСТ 6672.
Стерилизационный сушильный шкаф для температурного режима (180±0,5)°С по ГОСТ ISO 7218.
Ступка по ГОСТ 9147.
Термометры жидкостные стеклянные с диапазоном температуры от 0°С до 50°С и от 50°С до 100°С по ГОСТ 28498.
Термостаты электрические для выращивания микроорганизмов с автоматическим терморегулятором, обеспечивающие поддержание температуры от 20°С до 55°С по ГОСТ ISO 7218.
Фильтр Зейтца.
Флаконы из темного стекла с притертой пробкой.
Холодильник или холодильная камера по ГОСТ ISO 7218.
Часы механические с сигнальным устройством по ГОСТ 3145.
Чашки Петри стеклянные по ГОСТ 25336.
Бумага оберточная по ГОСТ 8273.
Бумага крепированная.
Крафт-бумага.
Пробки силиконовые, резиновые.
Пеналы для стерилизации лабораторной посуды.
Пакеты бумажные самоклеящиеся с индикаторами для паровой и воздушной стерилизации (для упаковывания изделий медицинского назначения перед стерилизацией).
Материал пластиковый без складок с индикаторами для паровой и воздушной стерилизации (для упаковывания изделий медицинского назначения перед стерилизацией).
Аппарат термосварочный ротационного или импульсного типа для запечатывания упаковок для стерилизации.
Бумага фильтровальная по ГОСТ 12026.
Вата медицинская гигроскопическая по ГОСТ 5556.
Марля медицинская по ГОСТ 9412.
Агар микробиологический по ГОСТ 17206.
Агар сухой питательный.
Азид натрия (NaN).
Аминопептид.
Ацетат свинца.
Бриллиантовый зеленый.
Бромтимоловый синий.
Бромкрезоловый пурпурный.
Вода дистиллированная по ГОСТ 6709.
Вода питьевая.
Генциан фиолетовый.
Глицерин дистиллированный по ГОСТ 6824.
D-Глюкоза по ГОСТ 6038.
Дрожжевой диализат.
Дрожжевой экстракт.
Дрожжи хлебопекарные прессованные по ГОСТ 171.
Желатин по ГОСТ 11293.
Железо (II) аммония сульфат (соль Мора) (NH)SO·FеSO·6HO.
Железо (III) аммония сульфат.
Железо треххлористое 6-водное по ГОСТ 4147.
Железо (III) цитрат.
Железо (II) сернокислое 7-водное по ГОСТ 4148.
Желчь крупного рогатого скота натуральная или сухая.
Индикатор Андреде.
Йод по ГОСТ 4159.
Калия гидрат окиси технический по ГОСТ 9285.
Калий йодистый по ГОСТ 4232.
Калий фосфорнокислый двузамещенный 3-водный по ГОСТ 2493.
Калий фосфорнокислый двузамещенный безводный.
Калий фосфорнокислый однозамещенный по ГОСТ 4198.
Кальций углекислый по ГОСТ 4530.
Кислота карболовая кристаллическая (фенол).
Кислота розоловая, ч.д.а.
Кислота соляная по ГОСТ 3118.
Кислота щавелевая по ГОСТ 22180.
Кристаллический фиолетовый.
Хлорид лития 6-водный.
Лактоза.
Магний хлористый 6-водный по ГОСТ 4209.
Малахитовый зеленый.
Мальтоза.
Маннит.
Масло вазелиновое медицинское по ГОСТ 3164.
Метиленовый синий (голубой).
Метиловый красный.
Карбамид (мочевина) по ГОСТ 6691.
Мясо — говядина охлажденная по ГОСТ 31797.
Мясной экстракт.
Натрия гидроокись, раствор молярной концентрацией 1,0 моль/дм (фиксанал).
Натрия гидроокись, раствор молярной концентрацией 0,1 моль/дм (фиксанал).
Натр едкий очищенный по ГОСТ 11078.
Натрий углекислый кислый по ГОСТ 4201.
Натрий кислый селенистокислый.
Натрий серноватистокислый (тиосульфат натрия, гипосульфит натрия) по ГОСТ 27068, ч.д.а.
Натрий углекислый (карбонат).
Натрий фосфорнокислый двузамещенный по ГОСТ 11773.
Натрий фосфорнокислый однозамещенный 2-водный по ГОСТ 245.
Натрий хлористый по ГОСТ 4233.
Натрия сульфит.
Пируват натрия.
Парадиметиламинобензальдегид.
Пептон сухой ферментативный для бактериологических целей по ГОСТ 13805.
Плазма кроличья сухая.
Сахароза по ГОСТ 5833.
Спирт этиловый ректификованный по ГОСТ 5962.
Триптон.
Теллурит калия.
Толуол по ГОСТ 5789.
Фуксин кислый.
Феноловый красный.
Фуксин основной.
DL-фенилаланин.
L-фенилаланин.
DL-аминокислоты (лизин, орнитин, аргинин).
L-аминокислоты (лизин, орнитин, аргинин).
-нафтол.
L-цистин.
Яйца куриные по ГОСТ 31654.
Желточная эмульсия.
Водный раствор метиленового синего (голубого) массовой концентрацией 0,1%.
Раствор карболовый кристаллического фиолетового или генциан фиолетового.
Раствор карболовый фуксина Циля.
Раствор Люголя.
Раствор серноватистокислого натрия (тиосульфата, гипосульфита).
Раствор розоловой кислоты массовой концентрацией 5,0%.
Раствор индикатора бромтимолового синего.
Раствор индикатора Андреде.
Раствор фенолового красного массовой концентрацией 1,6%.
Раствор фенолового красного массовой концентрацией 0,4%.
Раствор бриллиантового зеленого массовой концентрацией 0,001%.
Раствор бриллиантового зеленого массовой концентрацией 0,5%.
Раствор малахитового зеленого массовой концентрацией 1,0%.
Раствор трифенилтетразолиума хлористого массовой концентрацией 0,4%.
Раствор натрия кислого селенистокислого массовой концентрацией 10,0%.
Раствор L-цистина.
Раствор мочевины массовой концентрацией 40,0%.
Раствор мочевины массовой концентрацией 20,0%.
Раствор метилового красного.
Раствор гидрата окиси калия массовой концентрацией 40,0%.
Раствор щавелевой кислоты массовой концентрацией 12,0%.
Раствор железа треххлористого 6-водного массовой концентрацией 8,0%.
Реактив Эрлиха.
Реактив Ковача по ГОСТ 31659.
-галактозидный реактив по ГОСТ 31659.
Реактивы для теста Григорсена по ГОСТ 31747.
Спирто-водный раствор фуксина Пфейфера.
Спиртовой раствор -нафтола.
Физиологический раствор.
Физиологический фосфат-буферный раствор.
Бумага индикаторная для обнаружения индола.
Бумага индикаторная для определения сероводорода.
Красящие бумажки с кристаллическим фиолетовым или генциан фиолетовым для окраски по Граму.
Растворы и реактивы для окрашивания по Граму и для выявления спор — по ГОСТ 10444.1, ГОСТ 30425, ГОСТ ISO 7218.
Реактивы для реакции Фогес-Проскауера по ГОСТ 31659.
Калий гидрофосфатный безводный.
Диски с углеводами для тестов на ферментацию сахаров, по прилагаемой к ним инструкции.
Диски индикаторные бумажные для определения оксидазы.
Диск для биохимического подтверждения сальмонелл.
Диск для подтверждения St. aureus.
Сухие аглютинирующие адсорбированные поливалентные сальмонеллезные О-сыворотки основных групп А, В, С, Д, Е и редких групп; Vi-, Н-аглютинирующие сыворотки по прилагаемой к ним инструкции.
Системы биохимических микротестов по прилагаемой к ним инструкции. Биохимические микротесты со специальной адаптированной базой данных ГОСТ 31468.
Водорода пероксид по ГОСТ 10929 массовой концентрацией 30 г/дм.
Сухой или жидкий панкреатический гидролизат казеина.
Сусло-агар по ГОСТ 27543.
Среда Сабуро по ГОСТ 10444.12.
Голодный агар.
Агар желточно-солевой.
Агар яично-желточный азидный.
Агар Байрд-Паркера.
Агар с мочевиной (Кристенсена).
Агар трехсахарный по Олькеницкому.
Агар полужидкий.
Агар с феноловым красным и бриллиантовым зеленым.
Агар SPS.
Агар усиленный для клостридий.
Агар триптононно-сульфитный с неомицином.
Амино-пептидный бульон.
Бульон Хоттингера по ГОСТ 10444.1.
Бриллиантовый зеленый лактозный желчный бульон по ГОСТ 31747.
Желатиновая среда.
Среда железосульфитная.
Забуференная пептонная вода.
Забуференная пептонная вода готовая жидкая стерильная.
Забуференная пептонная вода сухая.
Мясная вода.
Солевой бульон.
Мясо-пептонный бульон с 1% глюкозы.
Мясо-пептонный агар.
Мясо-пептонный агар с глюкозой.
Мясо-пептонный агар с глюкозой и дрожжевым экстрактом.
Пептонная вода.
Пептонно-солевой раствор.
Пептонно-буферная среда.
Питательная среда для выявления сальмонелл.
Селенитовая среда Лейфсона.
Среды Гисса с углеводами.
Среда Вильсон-Блера (агаризованная), измененная для анаэробов.
Среда Кларка для реакции Фогес-Проскауэра.
Агаризованная среда Байрд-Паркера по ГОСТ 31746.
Среда для расщепления фенилаланина.
Среды с аминокислотами (лизином, орнитином, аргинином).
Среда Китт-Тароцци.
Среда Кесслера (с лактозой).
Среда Кауфмана.
Среда Мюллера.
Селенитовая среда.
Селенитово-цистиновая среда.
Селенит-цистиновый накопительный бульон.
Магниевая или хлористомагниевая среда.
Среда Ресселя.
Среда из сухого питательного агара с глюкозой.
Среда с углеводом (маннитом или мальтозой) и феноловым красным.
Среда Хейфеца с лактозой.
Среда Раппапорта-Вассилиадиса с соей (RVS-бульон) по ГОСТ 31659.
Среда Раппапорта-Вассилиадиса (R-V R10).
Сахарный бульон.
Тетратионатный бульон Мюллера-Кауфмана по ГОСТ 31659.
Агаризованная среда с кроличьей плазмой и бычьим фибриногеном по ГОСТ 31746.
Готовая питательная среда с растворами теллурита калия, сульфамезатина и эмульсии яичного желтка по ГОСТ 31746.
ГРМ агар (сухой питательный агар для культивирования микроорганизмов на основе гидролизата рыбной муки) по ГОСТ 31746.
Модифицированная полужидкая среда по инструкции на этикетке.
Висмут-сульфитный агар по инструкции на этикетке.
Среда Плоскирева по инструкции на этикетке.
Среда Эндо.
Среда готовая на тест-пластине (например, Petrifilm*).
________________
* Данная информация является рекомендуемой, приведена для удобства пользователей настоящего стандарта и не исключает возможность использования другой аппаратуры с аналогичными свойствами.
Среда Левина по инструкции на этикетке.
Среда Клиглера по ГОСТ 31659.
Среда SIM для идентификации по инструкции на этикетке.
Среда для реакции Фогес-Проскауера по ГОСТ 31659.
Среда Олькеницкого.
Триптон-триптофановая среда по ГОСТ 31659.
L-лизиндекарбоксилазная среда по ГОСТ 31659.
ONPG-диски для определения -галактозидазной активности по инструкции на этикетке.
Модифицированная полужидкая среда MSRV по инструкции на этикетке.
Бриллиантово-зеленый агар по инструкции на этикетке.
XLD-4 агар по инструкции на этикетке.
VP-среда по ГОСТ 31659.
Агар тройной сахарный по инструкции на этикетке.
Агар с цитратом железа (Симмонса) по инструкции на этикетке.
Агар Кристенсена с мочевиной по ГОСТ 31659.
Агар Байрд-Паркера по ГОСТ 31746.
Агар тройной сахарный с цитратом железа по инструкции на этикетке.
Агар лактозный с бриллиантовым зеленым и феноловым красным по ГОСТ 31747.
Глюкозо-триптонный (агар) бульон по ГОСТ 10444.1.
Кристалл виолет нейтральный красный желчный лактозный агар (VRBL-arap).
Трехсахарный железистый агар (TSI-arap) по ГОСТ 31746.
Скошенный столбик агара с цитратом (Симмонса).
Скошенный столбик мясо-пептонного агара.
Селективная обогатительная среда (лаурил сульфат триптозный бульон) по ГОСТ 31747.
Селективная обогатительная среда (бульон Мак-Конки) по ГОСТ 31747.
Селективная добавка.
Система для культивирования анаэробных микроорганизмов и капнофильных бактерий (например, Fnoxomat*).
________________
* Данная информация является рекомендуемой, приведена для удобства пользователей настоящего стандарта и не исключает возможность использования другой аппаратуры с аналогичными свойствами.
Диагностикум латексный для серотипирования бактерий рода Salmonella по документу, действующему на территории государства, принявшего стандарт.
Набор для подтверждения идентификации бактерий рода Salmonella с помощью латекс-теста по документу, действующему на территории государства, принявшего стандарт.
Тест-наборы для биохимической идентификации бактерий рода Salmonella.
Тест-штампы бактерий рода Salmonella, не относящихся к тифозной группе.
11.2.2 Допускается применение других средств измерений с метрологическими характеристиками и оборудования с техническими характеристиками, а также материалов, реактивов, растворов и питательных сред по качеству не ниже указанных.
Допускается использование аналогичных готовых и сухих (дегидратированных), питательных сред, предназначенных для указанных целей.
11.2.3 Подготовка посуды и материалов — по ГОСТ ISO 7218.
11.2.4 Подготовку исходной суспензии и приготовление десятикратных разведений для микробиологических исследований проводят по документу, действующему на территории государства, принявшего стандарт*.
________________
* В Российской Федерации действует ГОСТ Р ИСО 6887-2-2013 «Микробиология пищевых продуктов и кормов для животных. Подготовка проб, исходной суспензии и десятикратных разведений для микробиологических исследований. Часть 2. Специальные правила подготовки мяса и мясных продуктов».
11.3 Приготовление растворов реактивов, красок, индикаторов, разведений и питательных сред в лаборатории
11. 3.1 Общие положения по обеспечению качества приготовления питательных сред в лаборатории, сроки и условия их хранения — по ГОСТ ISO/TS 11133-1, ГОСТ ISO 11133-2.
3.1 Общие положения по обеспечению качества приготовления питательных сред в лаборатории, сроки и условия их хранения — по ГОСТ ISO/TS 11133-1, ГОСТ ISO 11133-2.
11.3.2 Приготовление растворов индикаторов — по ГОСТ 4919.1.
11.3.3 Приготовление разведений — по ГОСТ ISO 7218, ГОСТ 26669.
11.3.4 Раствор Люголя
2 г калия йодистого растворяют в 5-10 см дистиллированной воды в мерной колбе объемом 300 см, прибавляют 1 г кристаллического йода, оставляют на несколько часов до полного его растворения, затем доводят объем раствора дистиллированной водой до метки.
11.3.5 Раствор серноватистокислого натрия (тиосульфата, гипосульфита)
5 г ч.д.а. серноватистокислого натрия кристаллического (тиосульфата, гипосульфита) растворяют в 5-1 см дистиллированной воды, затем доводят объем раствора дистиллированной водой до 100 см и стерилизуют кипячением в течение 30 мин.
11.3.6 Физиологический раствор
В 1000 см дистиллированной воды растворяют 8,5 г хлористого натрия. Стерилизуют при температуре (121±1)°С в течение 20 мин.
11.3.7 Реактив Эрлиха
В 50 см этилового спирта массовой долей 96,0% растворяют 4,0 г парадиметиламинобензальдегида, затем медленно добавляют 50 см концентрированной соляной кислоты.
Реактив хранят во флаконе из темного стекла с притертой пробкой при температуре (4-8)°С.
11.3.8 Раствор розоловой кислоты массовой концентрацией 5,0%
0,5 г розоловой кислоты всыпают во флакон из темного стекла с притертой пробкой и заливают 10 см этилового ректификованного спирта массовой концентрацией 96,0%. Через 24 ч раствор готов к употреблению, раствором можно пользоваться в течение месяца.
Раствор хранят во флаконе из темного стекла с притертой пробкой при температуре 4°С-8°С.
11.3.9 Водный раствор метиленового синего (голубого) массовой концентрацией 0,1%
0,1 г метиленового синего (голубого) всыпают во флакон из темного стекла с притертой пробкой и заливают 100 см дистиллированной воды, ставят на сутки в термостат при температуре (37±0,5)°С.
11.3.10 Раствор индикатора бромтимолового синего
0,4 г бромтимолового синего растворяют в 40 см дистиллированной воды, нагревая ее до кипения. После этого к раствору прибавляют 6,4 см раствора гидроокиси натрия молярной концентрацией 0,1 моль/дм, в результате чего жидкость приобретает зеленоватый цвет, и доливают дистиллированной водой до 100 см.
Индикатор следует хранить во флаконе с притертой пробкой в темном месте.
11.3.11 Раствор индикатора Андреде
0,5 г кислого фуксина растворяют в 100 см дистиллированной воды, прибавляют 16,4 см раствора гидроокиси натрия молярной концентрацией 1,0 моль/дм. Стерилизуют 5 мин при температуре (100±1)°С.
Индикатор должен иметь соломенно-желтый цвет.
Раствор индикатора Андреде хранят в темном флаконе с притертой пробкой, в темном месте.
11.3.12 Раствор фенолового красного массовой концентрацией 1,6%
1,6 г фенолового красного помещают в мерную колбу на 100 см, растворяют в дистиллированной воде, добавляя ее до метки 100 см.
11.3.13 Раствор фенолового красного массовой концентрацией 0,4%
0,4 г фенолового красного помещают в мерную колбу на 100 см, растворяют в дистиллированной воде, добавляя ее до метки 100 см.
11.3.14 Раствор бриллиантового зеленого массовой концентрацией 0,001%
1,0 г бриллиантового зеленого помещают в мерную колбу на 100 см. В колбу добавляют до метки 100 см этиловый ректификованный спирт с массовой долей 96,0%, растворяют и настаивают в течение 24 ч. К 10 см полученного 1,0%-ного спиртового раствора добавляют до 90 см дистиллированной воды, тщательно взбалтывают.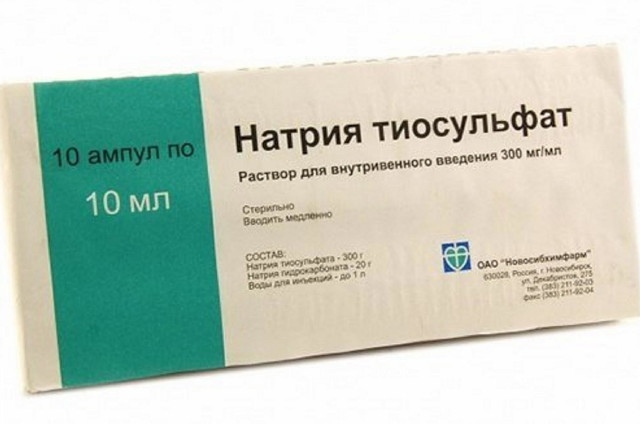
Раствор хранят во флаконе из темного стекла с притертой пробкой при комнатной температуре не более 3 мес.
11.3.15 Раствор бриллиантового зеленого массовой концентрацией 0,5%
0,5 г бриллиантового зеленого помещают в фарфоровую ступку и, постепенно растирая, растворяют в дистиллированной воде. Раствор переливают в мерную колбу на 100 см и доводят дистиллированной водой до метки 100 см.
Раствор хранят во флаконе из темного стекла с притертой пробкой при комнатной температуре не более 3 мес.
11.3.16 Карболовый раствор кристаллического фиолетового или генциан фиолетового
1 г кристаллического фиолетового или генциан фиолетового растирают в фарфоровой ступке с 2,0 г кристаллической карболовой кислоты (фенола). Во время растирания небольшими порциями добавляют 10 см этилового ректификованного спирта массовой концентрацией 96,0%. Раствор переливают в мерную колбу на 100 см и доводят дистиллированной водой до метки 100 см. Раствор фильтруют через влажный бумажный фильтр.
Растворы генциан фиолетового или кристаллического фиолетового нестойки. Готовят перед употреблением.
11.3.17 Карболовый раствор фуксина Циля
1 г порошка фуксина основного растирают в ступке с 5 г кристаллической карболовой кислоты и 0,5 см (несколько капель) глицерина. Во время растирания небольшими порциями прибавляют 10 см этилового ректификованного спирта массовой концентрацией 96,0%. После полного растирания к смеси прибавляют при постоянном помешивании 100 см дистиллированной воды и выдерживают 2 сут, после чего фильтруют через бумажный фильтр.
Фуксин Циля хранят во флаконе из темного стекла с притертой пробкой.
11.3.18 Спирто-водный раствор фуксина Пфейфера
К одной части карболового раствора фуксина Циля (см. 11.3.17) приливают девять частей дистиллированной воды. Раствор нестойкий. Готовят перед использованием.
Раствор нестойкий. Готовят перед использованием.
11.3.19 Раствор малахитового зеленого массовой концентрацией 1,0%
1 г малахитового зеленого засыпают во флакон из темного стекла с притертой пробкой и заливают 100 см этилового ректификованного спирта массовой концентрацией 96,0%. Через 24 ч раствор готов к употреблению.
Раствором можно пользоваться в течение месяца.
11.3.20 Раствор трифенилтетразолиума хлористого массовой концентрацией 0,4%
0,4 г трифенилтетразолиума хлористого засыпают во флакон из темного стекла с притертой пробкой и заливают 100 см дистиллированной воды, тщательно перемешивают до полного растворения.
11.3.21 Раствор натрия кислого селенистокислого массовой концентрацией 10,0%
10 г натрия кислого селенистокислого (гидроселенит) помещают в стерильную мерную колбу объемом 100 см и добавляют до метки 100 см стерильную дистиллированную воду, тщательно перемешивают до полного растворения.
Раствор готовят перед употреблением.
11.3.22 Раствор L-цистина
0,1 г L-цистина, 15 см раствора гидроокиси натрия массовой долей 1 моль/дм помещают в стерильную мерную колбу объемом 100 см и стерильной дистиллированной водой доводят до метки 100 см, тщательно перемешивают до полного растворения.
Раствор стерилизации не подлежит.
11.3.23 Дрожжевой экстракт
100 г измельченных хлебопекарных прессованных дрожжей заливают 1000 см дистиллированной воды, кипятят при постоянном перемешивании до тех пор, пока не сойдет пена, и помещают на 24 ч при 4°С-8°С в холодильник. Затем эмульсию фильтруют через вату и фильтрат стерилизуют в течение 20 мин при температуре (121±1)°С.
5 см жидкого дрожжевого экстракта равноценны 1 г дрожжевого экстракта в порошке.
Дрожжевой экстракт из сухих дрожжей готовят по инструкции изготовителя.
11.3.24 Желточная эмульсия
Для приготовления желточной эмульсии на дно стерильной чашки Петри помещают куриное яйцо, тщательно протирают его ватой, смоченной этиловым ректификованным спиртом, и обжигают. Стерильным пинцетом пробивают с двух противоположных сторон яйца два отверстия, через одно из этих отверстий из яйца полностью удаляют белок, а затем, несколько увеличив отверстие, выливают желток в стерильную колбу вместимостью 200 см. К желтку постепенно добавляют (частями по 20-30 см) 150-200 см (в зависимости от размера яйца) стерильного физиологического раствора, содержимое тщательно встряхивают (гомогенизируют) до получения гомогенной массы.
Готовят перед применением.
11.3.25 Раствор мочевины массовой концентрацией 40,0%
40 г карбамида (мочевины) помещают в мерную колбу объемом 100 см и добавляют стерильную дистиллированную воду до метки 100 см, тщательно перемешивают до полного растворения. Стерилизуют фильтрацией через фильтр Зейтца. Допускается «самостерилизация» раствора мочевины путем выдерживания его при комнатной температуре в течение 2-3 сут. Проверяют стерильность раствора контрольным посевом.
11.3.26 Раствор метилового красного
0,1 г метилового красного помещают в мерную колбу объемом 500 см и добавляют в 300 см этилового ректификованного спирта массовой концентрацией 96,0%, тщательно перемешивают до полного растворения и добавляют дистиллированную воду до метки 500 см. Раствор хранят во флаконе из темного стекла с притертой пробкой.
11.3.27 Спиртовой раствор -нафтола массовой долей 60 г/дм
6 г -нафтола растворяют в 100 см этилового ректификованного спирта массовой концентрацией 96,0%.
11.3.28 Раствор калия гидрат окиси массовой концентрацией 40,0%
40 г калия гидрат окиси помещают в мерную колбу объемом 100 см и добавляют стерильную дистиллированную воду до метки 100 см, тщательно перемешивают до полного растворения.
11.3.29 Раствор щавелевой кислоты массовой концентрацией 12,0%
12 г щавелевой кислоты помещают в мерную колбу объемом 100 см и добавляют стерильную дистиллированную воду до метки 100 см, тщательно перемешивают до полного растворения.
11.3.30 Раствор железа треххлористого 6-водного с массовой концентрацией 8,0%
8,0 г железа треххлористого 6-водного переносят в мерную колбу объемом 100 см, добавляют дистиллированную воду до метки 100 см, тщательно перемешивают до полного растворения.
11.3.31 Физиологический фосфат-буферный раствор
8,5 г натрия хлористого 0,45 г калия фосфорнокислого двузамещенного безводного, 5,34 г натрия фосфорнокислого однозамещенного 2-водного помещают в мерную колбу объемом 1000 см, доливают до метки 1000 см дистиллированной водой, стерилизуют 30 мин при температуре (121±1)°С.
11.3.32 Плазма крови кроличья
Плазму крови кроличью сухую восстанавливают по инструкции изготовителя.
11.3.33 Раствор мочевины массовой концентрацией 20,0%
20 г карбамида (мочевины) переносят в мерную колбу вместимостью 100 см, добавляют стерильную дистиллированную воду до метки 100 см, тщательно перемешивают до полного растворения.
11.3.34 Бумага индикаторная для определения сероводорода
20 г ацетата свинца, 1 г натрия углекислого (карбоната) растворяют в 100 см дистиллированной воды. Раствором пропитывают фильтровальную бумагу, высушивают ее при температуре 18°С-25°С и нарезают на узкие полоски. После приготовления бумага остается белой, при наличии сероводорода чернеет.
Бумагу индикаторную хранят во флаконе из темного стекла с притертой пробкой.
11.3.35 Бумага индикаторная для обнаружения индола
Листы фильтровальной бумаги обильно смачивают горячим раствором щавелевой кислоты массовой концентрацией 12,0% (11. 3.29), высушивают при температуре 18°С-25°С, нарезают полосками шириной 0,2-0,4 см, длиной 5,0-6,0 см.
3.29), высушивают при температуре 18°С-25°С, нарезают полосками шириной 0,2-0,4 см, длиной 5,0-6,0 см.
Бумагу индикаторную хранят во флаконе из темного стекла с притертой пробкой.
11.3.36 Красящие бумажки с кристаллическим фиолетовым или генциан фиолетовым для окраски по Граму в модификации Синева
1 г кристаллического фиолетового или генциан фиолетового, 100 см этилового ректификованного спирта массовой концентрацией 96,0% и 5 см глицерина смешивают, наливают в лоток. Фильтровальную бумагу нарезают в виде полосок шириной 1-2 см и длиной 30-50 см. Полоски погружают на несколько секунд в лоток с приготовленным раствором так, чтобы смачивались обе их поверхности. Окрашенные полоски вынимают пинцетом, дают раствору стечь и подвешивают для высушивания. Бумагу сушат в термостате при температуре (37±1)°С. Высушенные полоски бумаги разрезают на кусочки размерами 2 х 2 см или 2,0 х 4,5 см. Хранят во флаконе из темного стекла с притертой пробкой.
11.3.37 Мясная вода
Охлажденную говядину освобождают от костей, сухожилий, жира, измельчают. 1,0 кг полученного фарша заливают двух- или четырехкратным количеством питьевой воды (по массе), медленно нагревают до кипения и кипятят в течение 1,5 ч, постоянно помешивая и удаляя накипь. После кипячения мясную воду остужают, удаляют жир. Жидкость фильтруют через вату, затем через фильтровальную бумагу до полной прозрачности. Фильтрат измеряют и доливают до первоначального объема кипяченой питьевой водой, затем разливают по флаконам и стерилизуют при температуре (121±1)°С в течение 30 мин.
11.3.38 Мясо-пептонный бульон, мясо-пептонный бульон с глюкозой
10 г пептона бактериологического, 5 г натрия хлористого (хлорид) добавляют к 1000 см мясной воды (см. 11.3.37) устанавливают рН (7,0-7,2) ед. рН, кипятят. Жидкость фильтруют через фильтровальную бумагу, разливают по бутылям.
Стерилизуют при температуре (121±1)°С в течение 20 мин.
Мясо-пептонный бульон с глюкозой: к 1000 см мясо-пептонного бульона перед стерилизацией добавляют 1,0 или 10,0 г глюкозы, устанавливают рН (7,0-7,2) ед. рН и стерилизуют при температуре (121±1)°С в течение 20 мин.
11.3.39 Амино-пептидный бульон
В 250 см жидкого аминопептида добавляют 5,5 г натрия хлористого (хлорид), 750 см дистиллированной воды, перемешивают, стерилизуют в течение 20 мин при температуре (121±1)°С.
Срок хранения при температуре (4-8)°С не ограничен.
11.3.40 Пептонная вода
В 1000 см дистиллированной воды при медленном нагревании растворяют 1 г пептона бактериологического. Полученный раствор при необходимости фильтруют через бумажный фильтр, устанавливают рН (7,0-7,2) ед. рН, и стерилизуют при температуре (121±1)°С в течение 30 мин.
11.3.41 Забуференная пептонная вода
В 1000 см воды дистиллированной при медленном нагревании растворяют 10 г пептона и 5 г натрия хлористого (хлорид), 9 г фосфорнокислого двузамещенного натрия, 1,5 г фосфорнокислого однозамещенного калия, устанавливают рН (7,0-7,2) ед. рН и стерилизуют при температуре (121±1)°С в течение 15 мин.
11.3.42 Пептонно-солевой раствор
В 1000 см дистиллированной воды при медленном нагревании растворяют 1 г пептона бактериологического, 8,5 г хлористого натрия (хлорид). Полученный раствор при необходимости фильтруют через бумажный фильтр, устанавливают рН (7,0-7,2) ед. рН.
Стерилизуют при температуре (121±1)°С в течение 30 мин.
Раствор хранят в темном месте при температуре (4±2)°С не более одного месяца.
11.3.43 Голодный агар
2 г агара микробиологического растворяют в 98 см дистиллированной воды при нагревании и постоянном помешивании до полного растворения, устанавливают рН (7,0-7,2) ед. рН.
рН.
Стерилизуют в течение 20 мин при температуре (121±1)°С.
11.3.44 Мясо-пептонный агар
В 1000 см мясо-пептонного бульона (11.3.38) добавляют 15-20 г агара микробиологического и кипятят на слабом огне при постоянном помешивании до полного растворения агара, устанавливают рН (7,0-7,2) ед. рН.
Стерилизуют в течение 20 мин при температуре (121±1)°С.
11.3.45 Мясо-пептонный агар с глюкозой
К 1000 см мясо-пептонного агара (11.4.44) перед стерилизацией добавляют 1 или 10 г глюкозы, устанавливают рН (7,0-7,2) ед. рН.
Стерилизуют в течение 20 мин при температуре (121±1)°С.
11.3.46 Мясо-пептонный агар с глюкозой и дрожжевым экстрактом
К 1000 см стерильного расплавленного и охлажденного до температуры 50°С мясо-пептонного агара с глюкозой (11.3.45) перед применением асептически добавляют 2 г дрожжевого экстракта (11.3.23).
11.3.47 Среда Кесслера (с лактозой)
10 г пептона бактериологического, 5 г сухой желчи или 50 см натуральной стерильной желчи, 2,5 г лактозы, 0,01 г генциан фиолетового добавляют в 1000 см дистиллированной воды. Тщательно перемешивают, кипятят в течение 20-30 мин. Фильтруют через ватно-марлевый фильтр, устанавливают рН таким образом, чтобы после стерилизации он составлял (7,3±0,2) ед. рН при температуре (25±1)°С. Разливают в пробирки с поплавками (трубки Дархема) дном вверх.
Стерилизуют в течение 20 мин при температуре (114±1)°С. Если в поплавках остался воздух, среду не используют. Цвет готовой среды фиолетовый.
Срок хранения — не более 14 сут при температуре (4±1)°С.
11.3.48 Среда Хейфеца (с лактозой)
10 г пептона бактериологического, 5 г натрия хлористого (хлорида), 5 г лактозы растворяют в 1000 см дистиллированной воды, устанавливают рН (7,4-7,6) ед. рН, нагревают до кипения, фильтруют, добавляют 1 см 5,0%-ного спиртового раствора розоловой кислоты (11. 3.8) и 2,5 см 0,1%-ного водного раствора метиленового синего (голубого) (11.3.9). Среду разливают по 10 см в стерильные пробирки с поплавками (трубки Дархема). Стерилизуют при температуре (112±1)°С в течение 20 мин. Цвет среды красно-фиолетовый. Если в поплавках остался воздух, среду не используют.
3.8) и 2,5 см 0,1%-ного водного раствора метиленового синего (голубого) (11.3.9). Среду разливают по 10 см в стерильные пробирки с поплавками (трубки Дархема). Стерилизуют при температуре (112±1)°С в течение 20 мин. Цвет среды красно-фиолетовый. Если в поплавках остался воздух, среду не используют.
Срок хранения среды — не более 14 сут при температуре (4±2)°С.
11.3.49 Среда с углеводом (маннитом или мальтозой) и феноловым красным
К 1000 см стерильного, расплавленного и охлажденного до (80±2)°С питательного или мясо-пептонного агара (11.3.44) добавляют 10 г углеводов (маннита или мальтозы) (предварительно углеводы растворяют в небольшом объеме стерильной дистиллированной воды) и 52 см 1,6%-ного водного раствора фенолового красного (11.3.12). Смесь перемешивают, при необходимости еще раз расплавляют готовую среду, разливают в стерильные чашки Петри и подсушивают. Среду готовят с соблюдением стерильности.
Среда пурпурно-красного цвета.
Срок хранения среды — не более 30 сут при температуре (4±2)°С.
11.3.50 Среды Гисса с углеводами с индикатором Андреде
К 1000 см дистиллированной воды прибавляют 10 г пептона сухого ферментативного для бактериологических целей, 5,0 г натрия хлористого (хлорид). Пептон и соль растворяют при нагревании воды в течение нескольких минут. Фильтруют через бумажный фильтр до прозрачности раствора, устанавливают рН (7,1±0,1) ед. рН, прибавляют 10 г одного из необходимых углеводов (лактоза, глюкоза, сахароза, маннит и т.д.) и 10 см раствора индикатора Андреде (11.3.11). Среду разливают по 10,0 см в стерильные пробирки с поплавками (трубки Дархема) дном вверх и стерилизуют в течение 20 мин при температуре (112±1)°С.
Если в поплавках остался воздух, среду не используют.
Среды Гисса с индикатором Андреде должны быть бесцветны или соломенно-желтого цвета без розового оттенка.
Срок хранения среды — не более 30 сут при температуре (4±2)°С.
11.3.51 Среда Ресселя
К 1000 см 2,0%-ного питательного или мясо-пептонного агара (11.3.44) прибавляют 10 г лактозы, 1 г глюкозы и 10 см раствора индикатора Андреде (11.3.11).
Среду разливают по 10 см в пробирки, стерилизуют при температуре (112±1)°С в течение 20 мин и скашивают так, чтобы на 2,0-3,0 см от дна пробирки агар оставался в виде столбика.
Готовая среда бледно-розового цвета.
Срок хранения среды — не более 30 сут при температуре (4±2)°С.
11.3.52 Среда Мюллера
2,5 г стерильного кальция углекислого помещают в стерильный флакон, добавляют 90 см бульона Хоттингера, приготовленного по ГОСТ 10444.1, стерилизуют в течение 30 мин при температуре (121±1)°С, рН готовой среды (7,2-7,4) ед. рН.
Срок хранения среды — не более 30 сут при температуре (4±2)°С.
Перед использованием с соблюдением правил асептики добавляют 2 см раствора Люголя (11.3.4), и 10 см раствора серноватистокислого натрия (тиосульфата) (11.3.5). Готовая среда стерилизации не подлежит.
11.3.53 Среда Кауфмана
В 100 см стерильной среды Мюллера (11.3.52), с соблюдением правил асептики, добавляют 1 см раствора бриллиантового зеленого массовой концентрацией 0,001% (11.3.14) и 5 см стерильной натуральной говяжьей желчи, перемешивают. Среда стерилизации не подлежит.
Срок хранения среды — не более семи суток при температуре (4±2)°С.
11.3.54 Селенитовая среда
Основа среды: 5 г пептона сухого ферментативного для бактериологических целей или триптона, 4 г лактозы, 7 г натрия фосфорнокислого двузамещенного безводного и 3 г натрия фосфорнокислого однозамещенного при нагревании растворяют в 1000 см дистиллированной воды.
Устанавливают рН (7,0±0,1) ед. рН путем изменения соотношения солей: натрия фосфорнокислого однозамещенного и натрия фосфорнокислого двузамещенного. Разливают в колбы, стерилизуют в течение 30 мин при температуре (112±1)°С.
Срок хранения среды — не более 2 мес при температуре (4±2)°С.
Для приготовления основы среды допускается вместо пептона или триптона и дистиллированной воды использовать амино-пептидный бульон (11.3.39).
Перед использованием к 960 см основы среды добавляют 40 см раствора натрия кислого селенистокислого (11.3.21).
Готовую смесь не стерилизуют. Хранению не подлежит.
11.3.55 Селенитово-цистиновая среда
В 1000 см готовой селенитовой среды (11.3.54) асептически добавляют 10 см раствора L-цистина (11.3.22). Устанавливают рН (7,0±0,1) ед. рН.
Среда хранению не подлежит.
11.3.56 Питательная среда для выявления сальмонелл
Состав питательной среды: 4,3 г питательного агара, 0,3 г калия фосфорнокислого двузамещенного 3-водного, 1,5 г лактозы, 1,5 г сахарозы, 10 см стерильной натуральной желчи крупного рогатого скота (или 1 г сухой стерильной желчи), 0,3 см раствора малахитового зеленого массовой концентрацией 1,0% (11.3.19), 0,75 см раствора трифенилтетразолиума хлористого массовой концентрацией 0,4% (11.3.20), ингредиенты которого растворяют в 80 см дистиллированной воды при подогреве, последовательно, после полного растворения предыдущего ингредиента, доводят до кипения, доливают дистиллированной водой до 100 см, устанавливают рН (7,1±0,1) ед. рН. Стерилизуют в течение 15 мин при температуре (100±1)°С.
11.3.57 Магниевая среда или хлористомагниевая среда
Среду готовят из трех растворов.
Раствор I:
4,2 г пептона сухого ферментативного для бактериологических целей, 7,15 г натрия хлористого (хлорид), 1,48 г калия фосфорнокислого двузамещенного безводного, 9 см дрожжевого экстракта (11.3.23) (или дрожжевого диализата) растворяют в 890 см дистиллированной воды.
Раствор II:
35,7 г магния хлорида растворяют в 90 см дистиллированной воды.
Раствор III:
0,9 см 0,5%-ного водного раствора бриллиантового зеленого (11. 3.15).
3.15).
Все три приготовленных раствора смешивают, разливают в колбы, флаконы, пробирки. Стерилизуют при температуре (112±1)°С в течение 30 мин.
Срок хранения готовой среды — не более 14 сут при температуре (4±1)°С.
11.3.58 Агар трехсахарный по Олькеницкому
25 г сухого питательного агара, 10 г лактозы, 10 г сахарозы, 1 г глюкозы, 0,2 г железа (II) аммония сульфат (соль Мора), 10 г мочевины, 4 см 0,4%-ного раствора фенолового красного (11.3.13) растворяют в 1000 см дистиллированной воды.
Предварительно соли растворяют в небольшом объеме дистиллированной воды. Углеводы и мочевину также растворяют в небольших объемах воды при подогревании в водяной бане.
Сухой питательный агар расплавляют при нагревании в оставшемся объеме воды.
Все ингредиенты соединяют, перемешивают с расплавленным агаром, фильтруют через марлевый фильтр, устанавливают рН (7,2-7,4) ед. рН, добавляют индикатор и разливают в пробирки по 6-7 см.
Среду стерилизуют текучим паром три дня подряд по 20 мин при температуре (115±1)°С и скашивают, оставляя столбик 2-2,5 см.
Готовая среда бледно-розового цвета.
Срок хранения среды — не более 5 сут при температуре (4±1)°С.
11.3.59 Агар с мочевиной (Кристенсена)
Основа среды: 1 г пептона, 1 г глюкозы, 5 г натрия хлористого (хлорид), 2 г калия фосфорнокислого двузамещенного, 0,012 г фенолового красного, 15 г агара растворяют в 1000 см кипящей дистиллированной воды. Устанавливают рН таким образом, чтобы после стерилизации составлял (6,9±0,1) ед. рН при температуре (25±1)°С. Стерилизуют в течение 20 мин при температуре (121±1)°С.
Срок хранения среды — не более 5 сут при температуре (4±1)°С.
Перед употреблением асептически к 1000 см основы среды добавляют 50 см раствора мочевины массовой концентрацией 20,0% (11.3.33).
11.3.60 Среда Кларка для реакции Фогес-Проскауэра
7 г бактериологического пептона, 5 г гидрофосфата калия безводного, 5 г глюкозы растворяют в 1000 см дистиллированной воды. Кипятят в течение 2-3 мин, фильтруют через ватно-марлевый или бумажный фильтр, устанавливают рН (6,9-7,0) ед. рН, разливают в пробирки, стерилизуют в течение 20 мин при температуре (115±1)°С.
Кипятят в течение 2-3 мин, фильтруют через ватно-марлевый или бумажный фильтр, устанавливают рН (6,9-7,0) ед. рН, разливают в пробирки, стерилизуют в течение 20 мин при температуре (115±1)°С.
Срок хранения среды — не более 28 сут при температуре (4±1)°С.
11.3.61 Среда для расщепления фенилаланина
В 1000 см дистиллированной воды при нагревании растворяют 15 см дрожжевого экстракта (11.3.23), 2,0 г DL-фенилаланина или 1 г L-фенилаланина, 1 г фосфорнокислого двузамещенного натрия, 5 г хлористого натрия (хлорид), 12 г агара.
По 5 см среды разливают в пробирки, стерилизуют в течение 10 мин при температуре (121±1)°С и дают застыть в наклонном положении.
Срок хранения среды — не более 5 сут при температуре (4±1)°С.
11.3.62 Среды с аминокислотами (лизином, орнитином, аргинином)
5 г одной из L-аминокислот или 10 г одной из DL-аминокислот, 3 г дрожжевого экстракта (11.3.23), 1 г глюкозы, 0,012 г бромкрезолового пурпурного растворяют в 1000 см кипящей дистиллированной воды. Устанавливают рН таким образом, чтобы после стерилизации он составлял (6,8±0,1) ед. рН при температуре (25±1)°С.
Среды разливают в агглютинационные пробирки. Стерилизуют в течение 10 мин при температуре (121±1)°С или в течение 30 мин при температуре (110±1)°С.
Цвет сред — светло-фиолетовый. Хранению среды не подлежат.
11.3.63 Агар полужидкий
3 г мясного экстракта, 5 г пептона бактериологического, 4-9 г агара микробиологического растворяют при нагревании до кипения в 1000 см дистиллированной воды. Устанавливают рН таким образом, чтобы после стерилизации он составлял (7,0±0,1) ед. рН при температуре (25±1)°С. Разливают в пробирки и стерилизуют в течение 20 мин при температуре (121±1)°С.
Срок хранения — не более 28 сут при температуре (4±1)°С.
11. 3.64 Солевой бульон
3.64 Солевой бульон
К 100 см мясопептонного бульона (11.3.38) добавляют 6,5 г натрия хлористого. Стерилизуют в течение 20 мин при температуре (121±1)°С.
Срок хранения — не более 28 сут при температуре (4±1)°С.
11.3.65 Агар желточно-солевой
К 1000 см солевого бульона (11.3.64) добавляют 20 г микробиологического агара, расплавляют на водяной бане, при необходимости фильтруют через ватно-марлевый фильтр, разливают мерным цилиндром по 100 см в колбы вместимостью 250 см и стерилизуют при температуре (121±1)°С в течение 30 мин. Получают солевой агар. Вместо солевого бульона можно использовать как основу мясо-пептонный бульон (11.3.38), бульон Хоттингера по ГОСТ 10444.1, добавляя 65 г натрия хлористого.
К 1000 см стерильного, расплавленного и остуженного до температуры (45±1)°С солевого агара добавляют 200 см желточной эмульсии (11.3.24). После тщательного размешивания, желточно-солевой агар разливают в стерильные чашки Петри по 20-25 см.
Срок хранения — не более 5 сут при температуре (4±1)°С.
11.3.66 Агар яично-желточный азидный
В 1000 см дистиллированной воды растворяют при нагревании 10 г пептона, 3 г натрия хлористого, 0,2 г натрия фосфорнокислого двузамещенного, 15 г агара микробиологического, 5,5 г мясного экстракта. При отсутствии мясного экстракта используют мясную воду (11.3.37), при этом все компоненты растворяют в 1000 см мясной воды. Устанавливают рН (7,6±0,1) ед. рН. Стерилизуют в течение 30 мин при температуре (121±1)°С, охлаждают до температуры 50°С-60°С, добавляют 0,15 г азида натрия, смешивают, вновь стерилизуют в течение 30 мин при температуре (121±1)°С. После охлаждения до температуры (50±1)°С, добавляют 150 см желточной эмульсии (11.3.24), смешивают и разливают в чашки Петри.
Срок хранения — не более 5 сут при температуре (4±1)°С.
11.3.67 Желатиновая среда
10-15 г измельченного пищевого желатина добавляют в 100 см мясо-пептонного бульона (11. 3.38), растворяют при помешивании и медленном нагревании в водяной бане при температуре 40°С-50°С. После полного растворения устанавливают рН (7,1-7,3) ед. рН. Фильтруют через ватно-марлевый или бумажный фильтр, разливают в пробирки по 5-7 см, стерилизуют текучим паром один раз в день по 20 мин два дня подряд.
3.38), растворяют при помешивании и медленном нагревании в водяной бане при температуре 40°С-50°С. После полного растворения устанавливают рН (7,1-7,3) ед. рН. Фильтруют через ватно-марлевый или бумажный фильтр, разливают в пробирки по 5-7 см, стерилизуют текучим паром один раз в день по 20 мин два дня подряд.
После стерилизации среду охлаждают при строго вертикальном положении пробирок.
11.3.68 Среда Вильсон-Блера (агаризованная), измененная для анаэробов
К 1000 см стерильно расплавленного и охлажденного до температуры (80±1)°С питательного агара добавляют 10 см раствора натрия сернистокислого (сульфита) массовой концентрацией 100 г/дм, предварительно приготовленного следующим образом: 100 г натрия сернокислого (сульфита) помещают в стерильную колбу объемом 1000 см и добавляют до метки 1000 см стерильную дистиллированную воду; и 1 см раствора железа (III) аммония сульфата массовой концентрацией 50 г/дм, предварительно приготовленного следующим образом: 50 г железа (III) аммония сульфата помещают в стерильную колбу объемом 1000 см и добавляют до метки 1000 см стерильную дистиллированную воду.
Срок хранения среды в защищенном от света месте при температуре (4±1)°С — не более 7 сут.
Допускается приготовление среды Вильсон-Блера следующим образом: к 100 см расплавленного питательного агара добавляют 4 см раствора натрия сернистокислого (сульфита) массовой концентрацией 100 г/дм и 1 см раствора железа треххлористого 6-водного массовой концентрацией 80 г/дм, предварительно приготовленного следующим образом: 80 г железа треххлористого 6-водного помещают в стерильную колбу объемом 1000 см и добавляют до метки 1000 см стерильную дистиллированную воду.
Готовая среда хранению не подлежит.
11.3.69 Среда железосульфитная
К 1000 см дистиллированной воды добавляют 10 г триптона, 0,5 г сульфита натрия, 0,5 г железа (III) цитрата, 15 г агара (при приготовлении агаризованной среды) или 1,5 г агара (при приготовлении вязкой среды). Компоненты растворяют при нагревании, после чего охлаждают до температуры (50±5)°С. Устанавливают рН (7,1±0,1) ед. рН. Среду разливают в пробирки по 10-12 см и стерилизуют в течение 15 мин при температуре (121±1)°С.
Компоненты растворяют при нагревании, после чего охлаждают до температуры (50±5)°С. Устанавливают рН (7,1±0,1) ед. рН. Среду разливают в пробирки по 10-12 см и стерилизуют в течение 15 мин при температуре (121±1)°С.
Триптон может быть заменен на равноценную навеску сухого панкреатического гидролизата казеина или на десятикратный объем жидкого панкреатического гидролизата казеина. Триптон и 1000 см дистиллированной воды могут быть заменены на 1000 см мясной воды (11.3.37).
11.3.70 Среда Китт-Тароцци
Среду Китт-Тароцци готовят по ГОСТ 10444.1 со следующим дополнением: перед употреблением среду регенерируют. Для этого пробирки со средой помещают в водяную баню и прогревают в течение 20 мин при температуре (100±1)°С. Затем пробирки со средой быстро охлаждают водопроводной водой.
11.3.71 Селенитовая среда Лейфсона
Для приготовления среды готовят два раствора: А и Б.
Раствор А: 5 г пептона бактериологического, 7 г натрия фосфорнокислого двузамещенного безводного, 3 г натрия фосфорнокислого однозамещенного, 4 г химически чистой лактозы, 1000 см дистиллированной воды, рН (7,0±0,1) ед. рН, смешивают, разливают в стерильную посуду по 225 см и стерилизуют текучим паром один раз вдень по 30 мин два дня подряд или при температуре (112±1)°С в течение 30 мин однократно.
Раствор Б: раствор натрия кислого селенистокислого с массовой концентрацией 10% (11.3.21), (готовят на стерильной дистиллированной воде перед употреблением).
Перед началом работы к 225 см раствора А стерильно добавляют 9 см раствора Б.
11.3.72 Приготовление чашек со средой
Колбу с приготовленной и стерилизованной питательной средой после прогрева среды помещают в водяную баню при температуре от 44°С до 47°С, перемешивают, разливают в стерильные чашки Петри, дают затвердеть и подсушивают с открытой крышкой, соблюдая правила стерильности, пока поверхность среды не будет сухой.
Перед использованием среду в чашках предпочтительно с открытой крышкой и поверхностью среды вниз подсушивают в шкафу с температурой от 37°С до 55°С до тех пор, пока поверхность среды не будет сухой.
Срок хранения чашки со средой при температуре (4±1)°С — не более 5 сут.
11.3.73 Среда из сухого питательного агара: готовят по инструкции изготовителя.
11.3.74 Среда из сухого питательного агара с глюкозой
В 975 см сухого питательного агара (11.3.74) непосредственно перед применением асептически добавляют 25 см стерильного раствора глюкозы массовой концентрации 200 г/дм, предварительно приготовленного следующим образом: 200 г глюкозы помещают в стерильную колбу объемом 1000 см и добавляют до метки 1000 см стерильную дистиллированную воду.
11.3.75 Пептонно-буферная среда
10 г пептона, 0,45 г калия фосфорнокислого однозамещенного, 5,34 г натрия фосфорнокислого двузамещенного растворяют в 1000 см кипящей дистиллированной воды. Разливают в колбы вместимостью 500 см по 225 см среды. Стерилизуют (20±1) мин при температуре (121±1)°С, рН среды при температуре (25±1)°С составляет (7,0±0,1) ед. рН. Хранение при комнатной температуре не более 14 сут.
11.3.76 Бульон лактозный с бриллиантовым зеленым и желчью
10 г пептона, 10 г лактозы, 20 г сухой говяжьей желчи или 200 см натуральной желчи, 2,66 см раствора бриллиантового зеленого, приготовленного по 11.3.15, добавляют к 1000 см дистиллированной воды, перемешивают, нагревают на слабом огне до кипения, фильтруют через ватно-марлевый фильтр, охлаждают до температуры (50±1)°С, устанавливают рН таким образом, чтобы после стерилизации он составил (7,2±0,1) ед. рН при температуре (25±1)°С. Разливают по 10 см в пробирки с поплавками, стерилизуют (15±1) мин при температуре (121±1)°С.
Хранят не более 14 сут при температуре (4±1)°С.
11.3.77 Приготовление пробирок со скошенным столбиком среды
11.3.77.1 Приготовленную стерильную питательную среду (например, при приготовлении скошенного столбика агара с цитратом Симмонса или скошенного столбика мясо-пептонного агара) после прогрева в водяной бане при температуре от 44°С до 47°С перемешивают и по 5-7 см разливают, соблюдая правила стерильности в стерильные пробирки, скашивают, оставляя столбик высотой 2,0-2,5 см, после чего среде дают затвердеть.
Срок хранения пробирок со средой при температуре (4±1)°С — не более 5 сут.
11.3.77.2 Приготовленную нестерильную питательную среду (например, при приготовлении скошенного столбика мясо-пептонного агара) разливают в пробирки по 5-7 см, пробирки со средой стерилизуют и после остывания среды до температуры от 44°С до 47°С скашивают, оставляя столбик высотой 2,0-2,5 см, после чего среде дают затвердеть.
Срок хранения пробирок со средой при температуре (4±1)°С — не более 1 мес.
11.3.78 Приготовление сухих (дегидратированных) питательных сред проводят по инструкции на этикетке упаковки.
11.3.79 Приготовленные растворы реактивов, если не установлено иначе, хранят во флаконах из темного стекла с притертой пробкой в холодильнике при температуре (4±1)°С не более 3 мес или при температуре от 18°С до 23°С — не более 1 мес.
11.3.80 Приготовленные и стерилизованные питательные среды, разлитые в колбы, пробирки, чашки Петри, если не установлено иначе, хранят в холодильнике при температуре (4±1)°С не более 3 мес.
Перед использованием, если не установлено иначе, питательные среды доводят до температуры окружающей среды.
11.3.81 Контроль питательных сред — по ГОСТ ISO/TS 11133-1.
11.3.82 Сроки и условия хранения питательных сред — по ГОСТ ISO/TS 11133-1.
УДК 579. | МКС 67.120.20 | |
Ключевые слова: мясо птицы, субпродукты и полуфабрикаты, питательные среды, методы отбора проб, подготовка проб, разбавители, акт отбора проб, транспортирование и хранение проб, микробиологические исследования | ||
Редакция документа с учетом
изменений и дополнений подготовлена
АО «Кодекс»
Тиосульфат натрия
Тиосульфат натрия, 0,1 н. раствор (приготовление—■ см. стр. 86).[ …]
Тиосульфат натрия, раствор. Растворяют 25 г КагЗгОз-бРЬО в Ю0 мл дистиллированной воды и очищают от следов цинка обработкой раствором дитизона II, как описано выше.[ …]
Тиосульфат натрия, 0,01 н. раствор (приготовление — см. стр. 132).[ …]
Тиосульфат натрия, гипосульфит натрия №а5203 • 5НаО — бесцветные рассыпчатые кристаллы. Применяется в текстильной промышленности для уничтожения активного хлора после беления, в кино-, фотопромышленности4 в кожевенной промышленности и др. Выпускают продукт трех сортов.[ …]
Тиосульфат натрия Na2S203 • 5Н20, 0,1 н. раствор.[ …]
Тиосульфат натрия, 0,05 н. титрованный раствор: приготовление см. стр. 76. Поправку к титру раствора определяют способом, описанным в разделе 12, используя 0,05 н. раствор бихромата калия.[ …]
Тиосульфат натрия, с (ШгБгОз • 5НгО) “0,1 моль/л. Растворяют 2,5 ±0,2 г пентагидрата тиосульфата натрия в 100±5 мл воды. Раствор хранят в сосуде из желтого стекла в холодильнике не более 6 мес.[ …]
Натрий серноватистокислый (тиосульфат натрия), (ГОСТ 4215-48), 0,002 н. раствор.[ …]
Тиосульфат натрия, 0,1 н. титрованный раствор. Растворяют в дистиллированной воде 24,8 г Ма25203. 5Н20 ч. д. а. и приблизительно 2 г Ыа2С03 ч. д. а. и доводят до 1 л. Титр или поправочный коэффициент определяют, как указано на стр. 86.[ …]
Тиосульфат натрия, 0,1 н. раствор. Растворяют 24,8 г Ма25203-5Н20 ч. д. а. в 900 мл дистиллированной воДы, прибавляют 0,2 г Ма2С03 ч. д. а. и после растворения доводят дистиллированной водой до 1 л. Поправку к титру определяют способом, приведенным при определении кислорода, по 0,1 н. раствору бихромата (см. стр. 86).[ …]
д. а. в 900 мл дистиллированной воДы, прибавляют 0,2 г Ма2С03 ч. д. а. и после растворения доводят дистиллированной водой до 1 л. Поправку к титру определяют способом, приведенным при определении кислорода, по 0,1 н. раствору бихромата (см. стр. 86).[ …]
Тиосульфат натрия, 0,02 н. раствор. Смешивают 200 мл 0,1 н. раствора тиосульфата с 800 мл дистиллированной воды, в которой предварительно растворяют 0,2 г ШаСОз ч. д. а. Поправку к титру раствора определяют способом, приведенным при определении кислорода по 0,02 н. основному раствору бихромата (см. стр. 86).[ …]
Тиосульфат натрия, 0,1 н. раствор: 24,8 г МагБгОз-бНгО ч. д. а. растворяют в 000 мл дистиллированной воды, прибавляют 0,2 г N32003 ч. д. а. и после растворения доводят объем до 1 л. Поправку к титру раствора определяют следующим образом: в коническую колбу, снабженную притертой пробкой, наливают примерно 100 мл дистиллированной воды, прибавляют 10 мл 15%-ного раствора йодида калия, 5 мл разбавленной (1:4) серной кислоты и 20 мл 0,1 н. раствора бихромата калия (4,9037 г К2СГ2О7 ч.д. а. з 1 л). После перемешивания раствор оставляют стоять 5 мин в темноте и затем титруют раствором тиосульфата, добавляя 1—2 мл раствора крахмала в качестве индикатора. Титр проверяют не реже одного раза в неделю.[ …]
Тиосульфат натрия, 0,01 н. раствор; 100 мл 0,1 н. растввра разбавляют свежепрокипяченной и охлажденной дистиллированной водой, добавляют 0,2 г Ка2С03 и доводят объем до 1 л.[ …]
Тиосульфат натрия. Растворяют 25 г Ыа23203-5Н20 в 75 мл дистиллированной воды.[ …]
Тиосульфат натрия Каг820з • 5Н20, 0,002 н. раствор, свежеприготовленный.[ …]
Тиосульфат натрия, ТУ 6-09-2540—72, 0,1 н. раствор (фиксанал).[ …]
Тиосульфат натрия, ОД6 г безводного ИагЭгОз растворяют в 100 мл дистиллированной воды непосредственно перед применением. Раствор неустойчив.[ …]
Тиосульфат натрия, 0,1, 0,02 и 0,002 н. растворы. Готовят перед употреблением.[ …]
Тиосульфат натрия ЫагЭгОз • 5НгО, 0,1 и. раствор.[ …]
раствор.[ …]
Измельчают 15 г тиосульфата натрия в ступке и смешивают с 9 г возогнанного иода. К смеси прибавляют несколько капель воды и растирают до образования однородной массы. Затем прибавляют 10—15 мл этанола. Образовавшийся осадок тетратионата натрия отфильтровывают на воронке Бюхнера и отмывают от остатков иода малыми порциями этанола.[ …]
Тиосульфат натрия — 0,01 й титрованный раствор.Поправочный коэффициент раствора тиосульфата натрия К = I.[ …]
Стандартный титрованный раствор тиосульфата натрия сШагБгОз НзО) 10 ммоль/л. Растворяют 2,48 г тиосульфата натрия приблизительно в 250 мл воды в мерной колбе вместимостью 1 л, разбавляют до метки водой и перемешивают.[ …]
Выделившийся иод оттитровывают, как обычно, тиосульфатом натрия в присутствии крахмала. Содержание «активного .хлора» выражают в мг/л в пересчете на хлор.[ …]
Вг2 + 2К1 —12 + 2КВг. Выделившийся иод оттитровывают тиосульфатом натрия 12+2Ка28203— 2Ка! — -N323406.[ …]
Раствор из поглотителей оттитровывался 0,01 н. раствором тиосульфата натрия; было израсходовано 0,5 мл этого раствора.[ …]
Таким образом, для полного поглощения 1 кг хлора и полной нейтрализации стоков требуется 1 кг тиосульфата натрия и 2 кг кальцинированной соды.[ …]
Далее приливают 1,5-2 мл раствора К7 и ставят колбу на Ю мин. в темное место. Выделившийся по ходу реакции свободный иод оттитровывают О, I н раствором тиосульфата натрия до соломенного цвета, и затем, прилив I мл крахмала, оттитро-вывают окончательно до бесцветного.[ …]
Помещают исследуемую порцию в коническую колбу вместимостью 500 мл. Добавляют поочередно 1 г иодида калия, 2 мл фосфорной кислоты и с помощью пинетки 10.0 мл (V4) стандартного раствора тиосульфата натрия и затем 1 мл раствора крахмала. Реагент ы должны вводиться в строго определенной последовательности, так как в противном случае может иметь место кестехишметрическое превращение гипохлорита при воздействии тиосульфата.[ …]
Исходный раствор формальдегида. В колбу 200 мл вводят 1 мл 1%-ного раствора формалина, приливают 10 мл воды и добавляют из бюретки 10 мл раствора иода. Затем по каплям прибавляют раствор гидроксида натрия до получения светло-желтого окрашивания. Оставляют на 10 мин, добавляют 2 мл 10%-ной хлороводородной кислоты до полного выделения иода. Содержимое колбы выдерживают 10 мин и оттитровывают раствор тиосульфатом натрия с крахмалом в качестве индикатора. В таких же условиях оттитровывают и контрольный раствор (1 мл 0,1 н. раствора иода соответствует 1,5 мг формальдегида).[ …]
В колбу 200 мл вводят 1 мл 1%-ного раствора формалина, приливают 10 мл воды и добавляют из бюретки 10 мл раствора иода. Затем по каплям прибавляют раствор гидроксида натрия до получения светло-желтого окрашивания. Оставляют на 10 мин, добавляют 2 мл 10%-ной хлороводородной кислоты до полного выделения иода. Содержимое колбы выдерживают 10 мин и оттитровывают раствор тиосульфатом натрия с крахмалом в качестве индикатора. В таких же условиях оттитровывают и контрольный раствор (1 мл 0,1 н. раствора иода соответствует 1,5 мг формальдегида).[ …]
Ход определения. В коническую колбу, снабженную притертой стеклянной пробкой, наливают 50—100 мл анализируемой воды, вносят 0,5 г иодида калия и добавляют 10 мл уксусной кислоты. Через 5 мин оттитровываю! выделившийся иод раствором тиосульфата натрия (при содержании «активного хлора» выше 1 мг/л) или 0,005 н. раствором тиосульфата натрия (при содержании «активного хлора» от 0,1 до1 мг/л).[ …]
Содержание колСы доводят до метки дистиллированной водой и тщательно перемешивают; 10 мл приготовленного таким образом раствора переносят в коническую колбу, снабженную пришлифованной пробкой, добавляют 50 мл 0,1 N раствора иода и 20 .мл 1К раствора едкого натра. Колбу закрывают и оставляют ь темноте на 15 мин. Затем прибавляют 25 мл Ш раствора серной кислоты (2,8 мл коивеи 1 рарованиой Н.,304 осторожно вливают в 100 мл дистиллированной воды) и после перемешивания смесь вновь оставляют в темноте. Через 15 мин избыток йода титруют 0,1. раствором тиосульфата натрия в присутствии крахмала. Содержание формальдегида в 1 мл оттитрованного раствора равно (£0 — а) X X 0,1501 мг, где а — объем израсходованного раствора тиосульфата, мл. В мерную колбу на 1 л помещают оставшийся раствор формальдегида, чтобы в нем было гочно 20 мг формальдегида, и доводят до 1 л дистиллированной водой. Раствор устойчив в течение нескольких дней, его концентрация 0,020 мг/мл НСНО.[ …]
Определение сульфид-ионов. Фильтр с осадком помещают в коническую колбу емкостью 250 мл, прибавляют 25—50 мл 0,01 н. раствора иода и подкисляют жидкость добавлением 5 мл разбавленной (1:9) соляной кислоты. Фильтр измельчают стеклянной палочкой и затем оттитровывают избыток иода 0,01 н. раствором тиосульфата натрия в присутствии крахмала.[ …]
раствора иода и подкисляют жидкость добавлением 5 мл разбавленной (1:9) соляной кислоты. Фильтр измельчают стеклянной палочкой и затем оттитровывают избыток иода 0,01 н. раствором тиосульфата натрия в присутствии крахмала.[ …]
Если окраска пробы интенсивнее окраски в последней пробирке шкалы, то определение ведут титрометрически. Для этого растворы из трех пробирок, куда были внесены пробы из поглотителей, переливают в конические колбы. Пробирки ополаскивают раствором из третьего поглотителя. Выделившийся иод оттитро-вывают 0,01 н. раствором тиосульфата натрия до слаборозового окрашивания при постоянном интенсивном встряхивал нии раствора. Затем вносят в колбу 1 мл раствора крахмала, сильно встряхивают раствор и титруют до обесцвечивания крахмала.[ …]
В колбу приливают 2 ш 0,5£—ндго раствора крахмала и дальше титруют до обесцвечивания раствора. Наиболее точные результаты при иодометрическим определении получаются в том случае, когда, на обратное титрование расходуется тиосульфата натрия вдвое меньше,чем взят объем иода. Если объем тиосульфата оказался большим или меньший, чем 7 рассчитывают объем раствора иода, который надо взять на анализ, и проводят точное определение.[ …]
Градуировочный график № 2 (для растворов с высоким содержанием железа и меди). В делительные воронки емкостью 200 мл вводят аликвотные части раствора, содержащие 0—4 мкг никеля. В каждую воронку в зависимости от содержания железа и меди вводят 1—6 мл 1 М раствора тартрата аммония ( 20-кратный молярный избыток по отношению к железу) и 5— 10 мл 0,4 М раствора тиосульфата натрия ( 10—15-кратный молярный избыток по отношению к меди). Далее поступают так же, как при построении градуировочного графика № 1.[ …]
Мешающие вещества. Определению БГЩ мешает присутствие токсичных веществ (медь, активный хлор и другие биоциды) в таких концентрациях, что их действие проявляется даже после разбавления пробы. В таких случаях правильную величину БПК можно определить лишь после удаления из воды токсичных веществ, так, например, в случае присутствия активного хлора воду обрабатывают тиосульфатом натрия. Объем раствора тиосульфата натрия, необходимый для восстановления свободного хлора, определяют титрованием. К пробе, предназначенной для определения БПК, прибавляют эквивалентное количество 0,01 н. раствора тиосульфата натрия, рассчитанное по результату вышеприведенного титрования.[ …]
Объем раствора тиосульфата натрия, необходимый для восстановления свободного хлора, определяют титрованием. К пробе, предназначенной для определения БПК, прибавляют эквивалентное количество 0,01 н. раствора тиосульфата натрия, рассчитанное по результату вышеприведенного титрования.[ …]
Ход определения. Отбирают от 5 до 50 мл сточной воды (в зависимости от степени ее загрязнения), переносят в коническую колбу емкостью 250—300 мл, снабженную притертой пробкой, разбавляют, если нужно, дистиллированной водой до 60 мл и прибавляют 25 мл бромид-броматной смеси. Затем приливают 10 мл разбавленной (1:3) серной кислоты, закрывают колбу пробкой и оставляют стоять 30 мин. После этого добавляют 1 г иодида калия, снова закрывают колбу пробкой, перемешивают и через 5 мин титруют выделившийся иод 0,05 и. раствором тиосульфата натрия с добавлением 1—2 мл 0,5%-но-го раствора крахмала в конце титрования.[ …]
После нейтрализации пробы прибавляют из бюретки 20 мл 0,01 н. раствора бихромата калия, осторожно взбалтывают и нагревают в течение 30 минут на кипящей водяной бане. Переливают раствор в мерный цилиндр, промывают стакан дистиллированной водой и оставляют на 3—4 часа (лучше на ночь) для того, чтобы хорошо осел осадок. Отмечают объем жидкости в цилиндре и берут в две колбы по 20 мл для определения. Титрование проводят следующим образом: к 20 мл исследуемой жидкости прибавляют 2 мл 20% раствора серной кислоты, 2 мл 15% раствора йодида калия, закрывают пробкой, взбалтывают и оставляют на 5 минут. Затем прибавляют 20 мл воды и титруют 0,01 н. раствором тиосульфата натрия в присутствии крахмала.[ …]
Нагревают смесь до кипения и поддерживают слабое кипение в течение 10 мин, после чего, не охлаждая раствора, нейтрализуют разбавленным (2:5) аммиаком, прибавляя его по каплям до перехода оранжевой окраски в желтую. Раствор переносят вместе с осадком в мерную колбу емкостью 250 мл, доводят объем до метки дистиллированной водой и фильтруют через плотный фильтр, отбрасывая первые порции фильтрата-Затем отбирают 100 мл фильтрата, переносят его в коническую колбу, снабженную притертой пробкой, приливают 10 мл 10%-ного раствора иодида калия, добавляют 5 мл соляной кислоты (пл. 1,19 г/см3), дают постоять 5 мин в темном месте и титруют выделившийся иод 0,02 н. раствором тиосульфата натрия до перехода цвета раствора в бледно-желтый. Тогда прибавляют 1—2 мл, 0,5%-ного раствора крахмала и продолжают титрование до исчезновения синего окрашивания.[ …]
1,19 г/см3), дают постоять 5 мин в темном месте и титруют выделившийся иод 0,02 н. раствором тиосульфата натрия до перехода цвета раствора в бледно-желтый. Тогда прибавляют 1—2 мл, 0,5%-ного раствора крахмала и продолжают титрование до исчезновения синего окрашивания.[ …]
Гипосульфит — натрий — Большая Энциклопедия Нефти и Газа, статья, страница 3
Гипосульфит — натрий
Cтраница 3
Тиосульфат натрия, иначе называемый гипосульфит натрия, имеет формулу Na2S2O3 и представляет собой соль тиосерной кислоты. Обычно из водных растворов тиосульфат натрия кристаллизуется в виде пятиводной соли. [31]
К — поправка на титр гипосульфита натрия; 0 0065757 — количество глицерина в граммах, соответствующее 1 мл 0 1 N раствора гипосульфита натрия; g — навеска глицерина. [32]
ГДР а — число миллилитров гипосульфита натрия, пошедшее на титрование при слухом опыте; Ъ — число миллилитров гипосульфита натрия, пошедшее па титро-I1. [33]
Вещество HD легко реагирует с гипосульфитом натрия и другими тиосульфатами в водном или водно-спиртовом растворе в присутствии протонов, которые, с одной стороны, способствуют диссоциации гипосульфита, а с другой стороны, повышают полярность связей С — С1 в отравляющем веществе вследствие возникновения водородной связи с хлором. [34]
Из тиосульфатов на практике применяется лишь гипосульфит натрия N328203 — прекрасно кристаллизующаяся соль, устойчивая на воздухе как в сухом виде, так и в растворе. [35]
Некоторые восстановители, например сульфит и гипосульфит натрия, разрушают хромофорную группу эриохромцианина, но эта реакция обратима. Избыток перекиси водорода восстанавливает хромофорные свойства реагента. Другие восстановители — тиогликолевая и аскорбиновая кислоты, гидроксиламин и сероводород — не действуют на эриохромцианин.
[36]
Другие восстановители — тиогликолевая и аскорбиновая кислоты, гидроксиламин и сероводород — не действуют на эриохромцианин.
[36]
Изучение реакций, протекающих при получении гипосульфита натрия при взаимодействии сероводорода с раствором сульфита и бисульфита натрия, Отч. [37]
Разница в миллилитрах между количеством раствора гипосульфита натрия, израсходованного на титрование чистого раствора бихромата, и раствора, содержащего эфир, умноженная на 9 265, является количеством миллиграммов эфира в исследуемом образце. [38]
К — поправка на титр раствора гипосульфита натрия; 0 00062046 — количество этиленгликоля в граммах, соответствующее 1 мл 0 1 N раствора гипосульфита натрия. [39]
Более важным примером нам представляется сушка гипосульфита натрия. Пусть этот продукт, находящийся в кристаллической форме, желательно привести в безводную форму. Во избежание быстрого расплавления, необходимо ограничить облучение с тем, чтобы температура не превышала 40 С. Операция заканчивается, когда продукт с начальной кристаллической структурой теряет 40 % своего веса. [40]
В присутствии двуокиси углерода ( СО2) гипосульфит натрия разлагается, поэтому воду, предназначенную для приготовления раствора, кипятят в течение 2 ч для полного удаления СО2, а затем, закрыв колбу пробкой с хлоркальциевой трубкой, охлаждают до комнатной температуры и используют для приготовления раствора. Раствор хранят в склянке из темного стекла, закрытой пробкой, в которую вставлены сифон для отбора раствора в бюретку и хлоркальцие-вая трубка. [41]
В качестве маскирующего реагента чаще всего применяется гипосульфит натрия. При рН 4 0 — 5 5 ( среда ацетатного буфера) гипосульфит образует прочные комплексы с Gu, Ag, Hg, Bi, Pb и Cd, чем и препятствует реакции ионов этих металлов с дитизоном. Гипосульфит маскирует также сравнительно небольшие количества ионов никеля и кобальта. При больших концентрациях этих металлов рекомендуется добавлять в качестве маскирующего средства немного цианида.
[42]
При рН 4 0 — 5 5 ( среда ацетатного буфера) гипосульфит образует прочные комплексы с Gu, Ag, Hg, Bi, Pb и Cd, чем и препятствует реакции ионов этих металлов с дитизоном. Гипосульфит маскирует также сравнительно небольшие количества ионов никеля и кобальта. При больших концентрациях этих металлов рекомендуется добавлять в качестве маскирующего средства немного цианида.
[42]
Особенно активными восстановителями являются бисульфит натрия, гипосульфит натрия ( ронгалит) и сероводород. Многие другие вещества обладают хотя и более слабым, по все же ясно выраженным действием, например, гидроксиламип, соли различных тяжелых металлов, тонкоизмельченные металлы, а также гидрохинон, пирокатехин и пирогаллол. [43]
В связи с накоплением в поглотительном растворе гипосульфита натрия, а в случае очистки газа, содержащего HCN, и роданистого натрия удельный вес и вязкость раствора возрастают вследствие чего очистка газа начинает ухудшаться, и по достижении в растворе концентрации jNa S2O3 200 — 250 s / л часть раствора выводят из цикла и подвергают нейтрализации серной кислотой с целью перевода мышьяка из растворимой формы в нерастворимую. При нейтрализации выпадают в осадок As2S5 и As2S3 и некоторое количество серы, получающейся при частичном разложении гипосульфита серной кислоты, избыток которой необходим для полноты высаживания сернистого мышьяка. [44]
Раствор в 1 л воды 30 в гипосульфита натрия, 60 г углекислой соды и 5 г едкого натра нейтрализует хлор, фосген и бромбензилцианид. Раствор в 1 л воды 24 г серной печени и 14 ел3 мыльного щелока нейтрализует дифосген и хлорпикрин. Холодная вода очень медленно гидролизует иприт; при ее подогревании гидролиз ускоряется. Кипячением в воде дегазируют одежду из легких тканей, изделия из резины и мелкие металлич. Горячий воздух быстро испаряет иприт. Горючие вещества при горении создают на дегазируемой поверхности высокую темп-ру, к-рая вызывает разложение и испарение иприта. Огнем дегазируют грубые предметы из металла, почву и асфальтовые дороги. Хорошими растворителями иприта являются четыреххлористый углерод, дихлорэтан, ацетон, спирт, бензин, керосин и ряд других веществ.
[45]
Горючие вещества при горении создают на дегазируемой поверхности высокую темп-ру, к-рая вызывает разложение и испарение иприта. Огнем дегазируют грубые предметы из металла, почву и асфальтовые дороги. Хорошими растворителями иприта являются четыреххлористый углерод, дихлорэтан, ацетон, спирт, бензин, керосин и ряд других веществ.
[45]
Страницы: 1 2 3 4
Натрия тиосульфат р-р д/ин 30% 10 мл x10
Торговое название: Натрия тиосульфат (Sodium thiosulfate)Международное название: Натрия тиосульфат& (Sodium thiosulfate)
Фармакологическая группа: комплексообразующее средство
Фармакологическая группа по АТХ: V03AB06. Натрия тиосульфат
Фармакологическое действие: дезинтоксикационное, десенсибилизирующее, комплексообразующее, противовоспалительное местное, противопаразитарное, противочесоточное
Фармакодинамика:
Комплексообразующее средство. Оказывает дезинтоксикационное действие. При отравлении соединениями As, Hg, Pb образует неядовитые сульфиты. При отравлении цианидами образует менее ядовитые роданистые соединения.
Показания к применению:
Отравления As, Hg, Pb, синильной кислотой, солями йода, брома.
Противопоказания:
Гиперчувствительность.
Режим дозирования:
В/в, по 5-50 мл 30% раствора (в зависимости от вида и тяжести интоксикации).
Побочные действия:
Аллергические реакции.
Особые указания:
При отравлении цианидами рекомендуют одновременное назначение натрия гипосульфита и натрия нитрита.
Производитель: Би Пром ООО, Россия
Владелец регистрационного удостоверения: Биннофарм ЗАО, Россия
Формы выпуска: раствор для внутривенного введения 300 мг/мл, ампулы
Принадлежит к ЖНВЛП
Условия отпуска: по рецепту
Данные о регистрации: ЛСР-000866/10 от 10.02.2010
Состояние регистрационного удостоверения: действующее
Номер фармстатьи: ЛСР-000866/10-100210
Производитель: Мосхимфармпрепараты им. Н.А.Семашко ОАО, Россия
Н.А.Семашко ОАО, Россия
Владелец регистрационного удостоверения: Мосхимфармпрепараты им.Н.А.Семашко ОАО, Россия
Формы выпуска: раствор для внутривенного введения 300 мг/мл, ампулы, раствор для внутривенного введения 300 мг/мл, ампула, раствор для внутривенного введения 300 мг/мл, ампула 5 — контурная ячейковая упаковка
Состав: натрия тиосульфат 300 г — 1 л
Принадлежит к ЖНВЛП
Условия отпуска: по рецепту
Срок годности: 5 лет
Данные о регистрации: ЛС-002498 от 30.12.2011, 29.12.2006
Состояние регистрационного удостоверения: действующее
Номер фармстатьи: ФС 42-3793-99, ФСП 42-0002-6407-06, ФСП 42-0002-6407-06
Производитель: Новосибхимфарм ОАО, Россия
Владелец регистрационного удостоверения: Новосибхимфарм ОАО, Россия
Формы выпуска: раствор для внутривенного введения 300 мг/мл, ампулы, раствор для внутривенного введения 300 мг/мл, ампулы нейтрального стекла
Состав: натрия тиосульфат 300 г — 1 л
Принадлежит к ЖНВЛП
Условия отпуска: по рецепту
Срок годности: 5 лет
Данные о регистрации: Р N002800/01 от 08.08.2008
Состояние регистрационного удостоверения: действующее
Номер фармстатьи: Р N002800/01-080808, ФС 42-3793-99, ФСП 42-0119-3968-03, ФСП 42-3968-07
Производитель: Фармстандарт-Уфимский витаминный завод ОАО, Россия
Владелец регистрационного удостоверения: Фармстандарт-Уфимский витаминный завод ОАО, Россия
Формы выпуска: раствор для внутривенного введения 300 мг/мл, ампулы
Состав: натрия тиосульфат 300 мг — 1 мл
Принадлежит к ЖНВЛП
Условия отпуска: по рецепту
Срок годности: 5 лет
Данные о регистрации: ЛСР-006482/08 от 13.08.2008
Состояние регистрационного удостоверения: действующее
Номер фармстатьи: ФС 42-3793-99, ФСП 42-8051-06
Производитель: Эском НПК ОАО Ставрополь
Владелец регистрационного удостоверения: Эском НПК ОАО Ставрополь, Россия
Формы выпуска: раствор для внутривенного введения 300 мг/мл, ампулы
Состав: натрия тиосульфата пентагидрат 300 мг — 1 мл
Принадлежит к ЖНВЛП
Условия отпуска: по рецепту
Срок годности: 5 лет
Данные о регистрации: ЛСР-005204/09 от 29. 06.2009
06.2009
Состояние регистрационного удостоверения: действующее
Номер фармстатьи: ЛСР-005204/09-290609
Владелец регистрационного удостоверения: Екатеринбургская фармфабрика ОАО, Россия
Формы выпуска: субстанция-порошок, мешки полиэтиленовые
Данные о регистрации: 64/228/171 от 30.04.1964
Состояние регистрационного удостоверения: действующее
Производитель: Химический завод им. Л.Я.Карпова ОАО, Россия
Владелец регистрационного удостоверения: Химический завод им. Л.Я.Карпова ОАО, Россия
Формы выпуска: субстанция-порошок, пакеты полиэтиленовые, субстанция-порошок, мешки полиэтиленовые, субстанция-порошок, мешки бумажные ламинированные
Данные о регистрации: Р N002645/01 от 13.08.2008
Состояние регистрационного удостоверения: действующее
Номер фармстатьи: ФС 42-2871-92, ФС 42-2871-98, ФСП 42-0006-4256-03, ФСП 42-4256-08
Натрия Тиосульфат — «Безусловно рекомендую!!! Отзыв 2 в 1.Чистка + диета »
Не давно наткнулась на отзывы об удивительном средстве «Натрия тиосульфат».
Я люблю все испытывать на себе и решила тоже попробывать данное средство!
Мне 28 лет, особых проблем со здоровьем нет. Единственная моя проблема и головная боль это лишний вес. При росте 165 , весила 80 кг. Поэтому любые отзывы о быстром похудении и очищении организма, меня очень привлекают.
Я решила почистить свой организм с помощью данного средства, а также во время чистки сесть на диету. Диету я выбрала очень строгую.
Опишу вкратце о приеме тиосульфат натрия во внутрь.
Чистка рассчитана на 10 дней.
В упаковке как раз 10 ампул. Кстати стоимость на 2020 г, около 80 р.
Итак, как я чистила свой организм с помощью данного средства :
За 2 недели до чистки я сидела на правильном питании и мне удалось похудеть на 4 кг.
В момент чистки, я села на строгую геркулесовую диету.
Ежедневное меню моей диеты на завтрак обед и ужин это был запаренный Геркулес на воде + любой фрукт,а вечером перед сном принимала тиосульфат натрия .
Ампулы открывать не удобно, об этом пишут все. Так что будьте аккуратнее!!!!
После вскрытия ампулы, вливаете содержимое в стакан воды около 50 — 100 мл и запиваете. Вкус горьковатый , но терпимый. Можно закусить долькой лимона, чтобы перебить вкус.
Мой стартовый вес на момент чистки и диеты составил 76 кг. ( до диеты при правильном питании ушло 4 кг)
Мои ощущения в первые 3 дня чистки и диеты:
В первый же день, я почувствовала эффект легкости и бодрости!!! Диета переносилась нормально, отвес на весах на 3 день составил 1.5 кг
В туалет бегала постоянно,но само средство действовало очень мягко,я просто чувствовала не большой позыв в туалет и все … Насчет туалета это отдельная песня… ДА, ДЕЙСТВИТЕЛЬНО,ЗАПАХ ЕСТЬ!!!!!!!!!!!! Поэтому во время чистки, лучше всего изолировать себя от людей😂😂😂😂
Правда, этот запах прошел у меня уже на 4 день и все нормализовалось …
С 4 по 6 день были проблемы с туалетом, но тут я грешу на диету. Из за ограничений в еде, я просто не могла сходить в туалет… Вес стоял…
С 6 по 10 день приема, все было как обычно. Стул нормализовался, а отвес составил -2 кг.
Тиосульфат натрия, не использовала в качестве средства для похудения. Меня интересовала сама чистка организма.
Из результатов :
— Ощущается прилив энергии
— Чувство легкости
— Белки глаз становятся чище , но не ВАУ, как это описывались в других отзывах
— Хорошая чистка кишечника
— Стрессоустойчивость ( в дни приема тиосульфата натрия, я была предельно спокойна, не смотря на стрессы и проблемы на работе)
В результат не буду писать отвес сброшенного веса .Да во время чистки при правильном питании от вас уйдет 1.5 кг лишняя жидкость и т. д,но это не средство для похудения!!!!!
Теперь насчет диеты :
Остановилась я на геркулесовой диете, так как решила полностью почистить свой организм. Ведь Геркулес это некий скраб для желудка и тела.
В течении всей диеты и чистки я пила зеленый чай+ воду.
В целом диету перенесла нормально, но при моем избыточным весе, хотелось больших результатов…
В целом, результаты меня устраивают!!!
Рекомендую чистку и диету тем, у кого нет проблем со здоровьем!!!!
Спасибо за внимание 😊
P. S Возможно свой отзыв обновлю и добавлю пару других диет и чисток. Фото»до»имеется,хочется поскорее уже «после»)))
Всем 👋
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Тиосульфат натрия | CAS 7772-98-7 | SCBT
Тиосульфат натрия | CAS 7772-98-7 | SCBT — Santa Cruz Biotechnology Тиосульфат натрия CAS: 7772-98-7MF: Na2S2O3
MW: 158,11
Широко применяемый биохимический препарат с тиосульфатом, используемый для синтеза различных комплексов диамин-CuCN.
- Дом
- Химические вещества
- Прочие химические вещества
- Неорганические вещества org/ListItem»> Тиосульфат натрия
Альтернативные имена: Гипосульфит натрия
Заявление: Тиосульфат натрия является широко используемым биохимическим веществом с участием тиосульфата, используемым для синтеза различных комплексов диамин-CuCN.Количество CAS: 7772-98-7
Чистота: 99%
Молекулярный вес: 158.11
Молекулярная формула: Na 2 S 2 O 3
Только для исследовательского использования. Не предназначено для диагностического или терапевтического использования.
* Данные по партии (включая содержание воды) см. В Сертификате анализа.Нажмите на изображение или кнопку увеличения, чтобы увеличить
Закрыть
Тиосульфат натрия применяется в широко используемом биохимическом препарате с применением тиосульфата, который используется для синтеза различных комплексов диамин-CuCN.
Ссылки
1. Stocker, F.B. и другие. Неорг. Chem. 38, 984, (1999)
Появление :
Порошок или кристаллический
Растворимость :
100 мг / мл в ч3O
Место хранения :
Хранить при комнатной температуре
Температура плавления :
52 ° C (разл.)
Плотность :
1,667 г / см 3 при 20 ° C
Только для исследовательского использования. Не предназначено для диагностического или терапевтического использования.
Номер в леях :
MFCD00003499
Улыбки :
[O-] S (= O) (= S) [O-].[Na +]. [Na +]
Adobe Acrobat Reader требуется для надежного просмотра,
печати и комментирования PDF-документов.
Дата выпуска: 2015-06-05
Santa Cruz Biotechnology, Inc.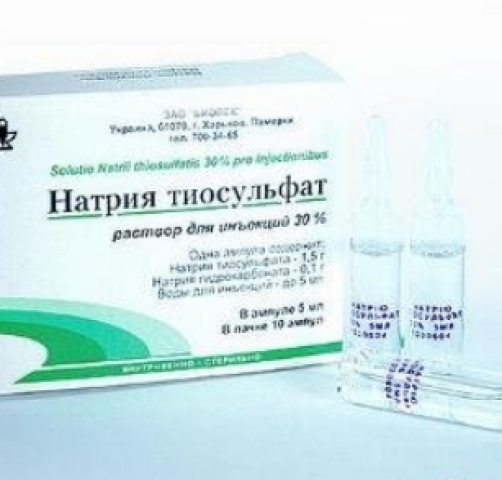 — мировой лидер в разработке продуктов для рынка биомедицинских исследований. Позвоните нам по бесплатному телефону 1-800-457-3801 .
— мировой лидер в разработке продуктов для рынка биомедицинских исследований. Позвоните нам по бесплатному телефону 1-800-457-3801 .
Copyright © 2007-2021 Santa Cruz Biotechnology, Inc. Все права защищены. «Santa Cruz Biotechnology» и логотип Santa Cruz Biotechnology, Inc., «Santa Cruz Animal Health», «San Juan Ranch», «Дополнение чемпионов», логотип San Juan Ranch, «Ultracruz», «Chemcruz», » Immunocruz «,» Exactacruz «и» EZ Touch «являются зарегистрированными товарными знаками Santa Cruz Biotechnology, Inc.
Все товарные знаки являются собственностью соответствующих владельцев.
Получена ваша подписка на рассылку новостей и объявлений по электронной почте. Регистрируясь, вы подтверждаете, что прочитали и согласны с условиями нашей политики конфиденциальности. Вы имеете право отказаться от подписки в любое время, щелкнув ссылку «отказаться от подписки» в любом полученном вами электронном письме с новостями и объявлениями.
Чтобы разместить заказ с использованием юаней или отправить товар в континентальный Китай, посетите сайт www.scbio.cn
Тиосульфат натрия: мифическое лечение загадочной болезни?
Кальцификация медиального слоя артерий, часто называемая артериосклерозом Монкеберга , часто встречается при ХБП и присутствует у большинства пациентов с ТПН (1).Хотя это, вероятно, имеет пагубные долгосрочные последствия, обычно это хроническое бессимптомное состояние. Однако у некоторых пациентов медиальная кальцификация приводит к окклюзии мелких артерий и артериол, что приводит к острому, опасному для жизни проявлению кожи и подкожному некрозу, ранее известному как кальцифилаксия, но теперь более точно называемому кальцифицирующей уремической артериолопатией (CUA). Это заболевание продолжает сбивать с толку исследователей и бросать вызов врачам, которым приходится полагаться на методы лечения, которые являются скорее мифическими, чем основанными на доказательствах.Есть надежда, что недавно созданная международная сеть сотрудничества (2) предоставит более объективные данные в будущем.
Это заболевание продолжает сбивать с толку исследователей и бросать вызов врачам, которым приходится полагаться на методы лечения, которые являются скорее мифическими, чем основанными на доказательствах.Есть надежда, что недавно созданная международная сеть сотрудничества (2) предоставит более объективные данные в будущем.
Почему CUA развивается только у очень небольшого процента пациентов с ESRD, несмотря на преобладание кальцификации медиальной артерии у этих пациентов, неясно. Окклюзия сосудов, по-видимому, включает гиперплазию интимы, воспаление и тромбоз (3,4), но что является исходным событием и как это связано с неизменно присутствующей медиальной кальцификацией, остается неизвестным.Исследования «случай-контроль» предоставили несколько конкретных ключей к разгадке, кроме изменения минерального метаболизма (5–7). Однако недавнее исследование, проведенное в Японии, определило терапию варфарином как мощный фактор риска (7), подтвердив подозрения многих исследователей (4). Варфарин может способствовать CUA, блокируя карбоксилирование и активность матричного белка gla, мощного ингибитора кальцификации сосудов (8), и антикоагулянтных белков C и S. На основании этих исследований лечение обычно состоит из коррекции гиперфосфатемии, снижения уровня кальция в сыворотке. (путем паратиреоидэктомии или добавления цинакальцета, прекращения приема соединений витамина D и снижения концентрации кальция в диализате) и прекращения приема варфарина в дополнение к агрессивной терапии ран.
Неопределенный патогенез и отсутствие рандомизированных контролируемых исследований заставляют врачей выбирать методы лечения, основанные на механистических предположениях и небольших отчетах о случаях заболевания. Одной из таких терапий, которая сейчас широко используется при CUA, является тиосульфат натрия (STS). Эта терапия основана на наблюдениях, опубликованных более 3 десятилетий назад, о том, что STS может предотвратить повторное образование камней в почках (9). Впоследствии его было предложено использовать при опухолевом кальцинозе при почечной недостаточности (10), а первое сообщение о его применении при CUA появилось почти десять лет назад (11). За этим последовало несколько отчетов о случаях и небольших серий с неоднозначными результатами с точки зрения пользы. Хотя нет данных, подтверждающих эффективность STS при CUA у людей, STS действительно снижает кальцификацию медиальной артерии в модели кальцификации уремических сосудов у крыс (12) и в модели ex vivo кальцификации в культивируемых аортах крыс (13). Однако ни то, ни другое не является моделью CUA.
За этим последовало несколько отчетов о случаях и небольших серий с неоднозначными результатами с точки зрения пользы. Хотя нет данных, подтверждающих эффективность STS при CUA у людей, STS действительно снижает кальцификацию медиальной артерии в модели кальцификации уремических сосудов у крыс (12) и в модели ex vivo кальцификации в культивируемых аортах крыс (13). Однако ни то, ни другое не является моделью CUA.
Как тиосульфат может обратить вспять CUA, неясно, и был предложен ряд механизмов, в первую очередь включающих комплексообразование с ионами кальция или растворение отложений кальция.Несмотря на широко распространенное мнение об обратном, тиосульфат не хелатирует ионы кальция, не ингибирует образование гидроксиапатита и не растворяет кальцификаты сосудов in vitro (13). Образование гидроксиапатита и кальцификация сосудов зависят от pH в патофизиологическом диапазоне, при этом алкалоз способствует кальцификации (14), а ацидоз снижает кальцификацию артерий у уремических животных (15). Однако тиосульфат не является кислотой и не изменяет pH при добавлении в кровь ex vivo (12), а ингибирование кальцификации в культуральных сосудах происходило без изменения pH культуральной среды (13).Расширенный ацидоз, который действительно производит STS in vivo , слишком слаб, чтобы оказывать значительное влияние на кальцификацию (12). Наконец, было предложено антиоксидантное действие, направленное на воспаление и гиперплазию интимы, основанное на том факте, что тиосульфат может окисляться до сульфата. Однако сульфат был так же эффективен, как и тиосульфат, в ингибировании кальцификации в сосудах для культивирования (13), тем самым исключая антиоксидантный эффект.
Несмотря на отсутствие данных об эффективности у людей, неопределенный механизм и неизвестную безопасность, STS продолжает использоваться для лечения CUA.Это возможно, потому что STS одобрен и доступен для лечения отравления цианидом. В этом выпуске CJASN , Nigwekar et al.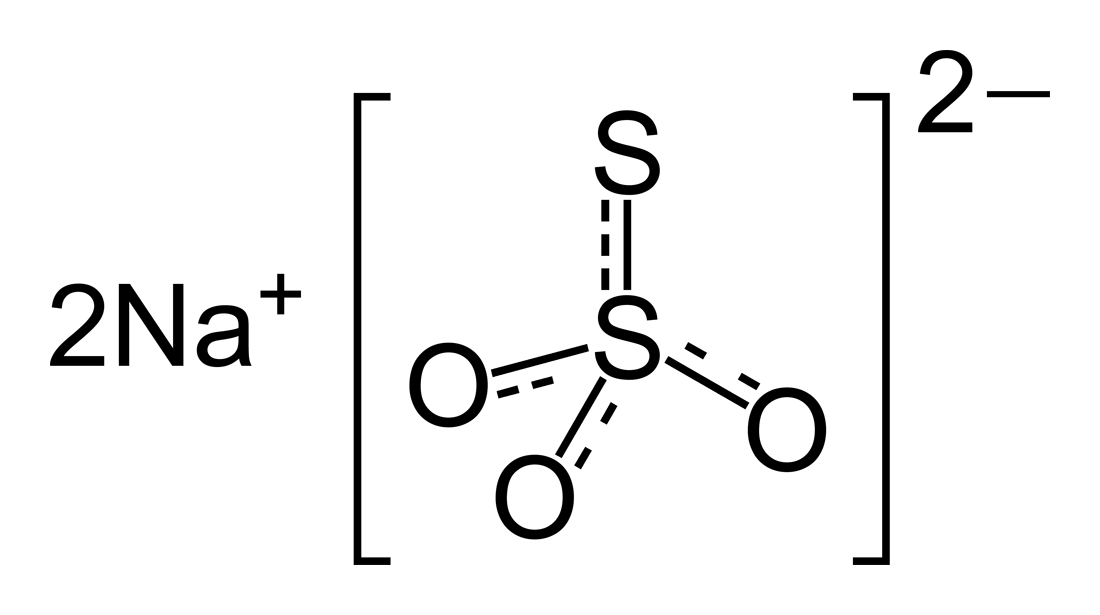 представляют собой большую серию из 147 пациентов, завершивших лечение с помощью STS для CUA, что на сегодняшний день является крупнейшим на сегодняшний день, что помогает заполнить этот информационный пробел (16). Хотя подробная информация была доступна только по 43 пациентам, это исследование все же в несколько раз больше, чем любое предыдущее исследование. Основным выводом этого исследования было то, что лечение было безопасным и хорошо переносимым, с оговоркой, что не было контрольной группы.Лабораторные данные показали ожидаемое увеличение сывороточного анионного разрыва, а также снижение сывороточного кальция. Последнее сохранялось после терапии и, предположительно, отражает другие меры, которые были предприняты, такие как снижение потребления кальция, снижение концентрации кальция в диализате, прекращение приема соединений витамина D, начало цинакальцета и паратиреоидэктомия. Снижение уровня паратиреоидного гормона в сыворотке крови, которое имело пограничное значение, неудивительно, учитывая, что 72% пациентов либо перенесли паратиреоидэктомию, либо начали принимать цинакальцет.Наблюдалось снижение веса после диализа, которое сохранялось после терапии и, скорее всего, отражает болезнь пациентов, а не эффект STS. Тошнота и рвота наблюдались примерно у трети пациентов, но они редко были неизлечимыми, а смертельные исходы не были связаны с STS.
представляют собой большую серию из 147 пациентов, завершивших лечение с помощью STS для CUA, что на сегодняшний день является крупнейшим на сегодняшний день, что помогает заполнить этот информационный пробел (16). Хотя подробная информация была доступна только по 43 пациентам, это исследование все же в несколько раз больше, чем любое предыдущее исследование. Основным выводом этого исследования было то, что лечение было безопасным и хорошо переносимым, с оговоркой, что не было контрольной группы.Лабораторные данные показали ожидаемое увеличение сывороточного анионного разрыва, а также снижение сывороточного кальция. Последнее сохранялось после терапии и, предположительно, отражает другие меры, которые были предприняты, такие как снижение потребления кальция, снижение концентрации кальция в диализате, прекращение приема соединений витамина D, начало цинакальцета и паратиреоидэктомия. Снижение уровня паратиреоидного гормона в сыворотке крови, которое имело пограничное значение, неудивительно, учитывая, что 72% пациентов либо перенесли паратиреоидэктомию, либо начали принимать цинакальцет.Наблюдалось снижение веса после диализа, которое сохранялось после терапии и, скорее всего, отражает болезнь пациентов, а не эффект STS. Тошнота и рвота наблюдались примерно у трети пациентов, но они редко были неизлечимыми, а смертельные исходы не были связаны с STS.
Поскольку пациентов можно идентифицировать только с помощью STS, а не с помощью диагностики CUA, к сожалению, не существует контрольной группы. Поскольку маловероятно, что когда-либо будет проведено рандомизированное контролируемое исследование, любые доказательства эффективности должны быть получены из исторических сравнений.Это всегда проблематично, особенно потому, что CUA теперь распознается раньше, используется более агрессивная терапия ран и теперь доступен цинакальцет. Хотя годичная смертность была ниже в текущей серии (35%) по сравнению с ранее опубликованной серией пациентов, не получавших STS (55%) (5), не было никакой разницы при сравнении пациентов с аналогичным, более легким заболеванием, что позволяет предположить никакой пользы. Есть и другие ограничения, которые также влияют на анализ данных. Поскольку гистологический диагноз был поставлен менее чем у половины пациентов, у некоторых из них CUA могла не присутствовать.Кроме того, потенциальное исключение госпитализированных (и предположительно более больных) пациентов могло внести систематическую ошибку отбора. Таким образом, это исследование не дает ответа на вопрос об эффективности STS и все еще остается под вопросом.
Есть и другие ограничения, которые также влияют на анализ данных. Поскольку гистологический диагноз был поставлен менее чем у половины пациентов, у некоторых из них CUA могла не присутствовать.Кроме того, потенциальное исключение госпитализированных (и предположительно более больных) пациентов могло внести систематическую ошибку отбора. Таким образом, это исследование не дает ответа на вопрос об эффективности STS и все еще остается под вопросом.
Несмотря на ограниченность этого исследования, следует поздравить авторов с этим трудным делом и предоставлением нам полезных данных из самых крупных на сегодняшний день серий. Хотя в этом исследовании эффективность не установлена, авторы четко демонстрируют, что лечение безопасно и хорошо переносится.В отсутствие контролируемых испытаний и четкого понимания его патофизиологии лечение CUA останется в сфере мифологии. Хотя мы не знаем, работает ли STS и с помощью какого механизма, мы, по крайней мере, можем быть уверены, что это безопасно.
Раскрытие информации
W.C.O. получил гранты от Amgen, Genzyme и Synageva, а также гранты и гонорары от Baxter Healthcare.
Сноски
Публикуется в Интернете перед печатью. Дата публикации доступна на сайте www.cjasn.org.
См. Статью по теме «Терапия тиосульфатом натрия при кальцифицирующей уремической артериолопатии» на страницах 1162–1170.
- Авторские права © 2013 Американского общества нефрологов
Тиосульфат натрия для лечения кальциноза, связанного с ювенильным и взрослым дерматомиозитом — Просмотр полного текста
Кальциноз, серьезное осложнение дерматомиозита, включает отложение кальция (карбонат апатита). ) в мягких тканях и может отрицательно сказаться на качестве жизни и физических функциях.На сегодняшний день не существует известных эффективных методов лечения, одобренных для лечения кальциноза, связанного с дерматомиозитом, и в медицинском сообществе нет единого мнения об оптимальной стратегии лечения этого часто изнурительного состояния.
Несколько сообщений в литературе описывают успехи лечения с помощью различных терапевтических средств; однако эти данные взяты из отдельных отчетов или серий случаев и, таким образом, предоставляют ограниченные научные доказательства эффективности. Недавно опубликованные отчеты, а также личные наблюдения в нашей группе показали, что внутривенное лечение тиосульфатом натрия может принести пользу пациентам с кальцинозом.Чтобы собрать более надежные данные о полезности этого препарата при лечении кальциноза, связанного с дерматомиозитом взрослых и подростков, мы предлагаем оценить его эффекты в контексте проспективного клинического исследования.
Мы планируем включить участников из одного центра в открытое исследование с одной группой, общей целью которого является оценка эффективности и безопасности внутривенного применения тиосульфата натрия у пациентов с умеренным и тяжелым обширным кальцинозом, связанным с ювенильным и взрослым дерматомиозитом. .
В полном исследовании будет участвовать не более 18 участников в течение 4 лет, но до 250 пациентов могут пройти скрининг для включения в исследование. Соответствующие критериям пациенты будут в возрасте 7 лет и старше, и будут иметь обширный кальциноз (определяемый как кальциноз туловища или двух конечностей) и умеренный или тяжелый кальциноз (на что указывает оценка визуальной аналоговой шкалы активности кальциноза, превышающая или равная 3,5 см от 10 см).
Две отдельные оценки, выполненные в NIH до начала терапии, будут использоваться в качестве исходных данных для попарного сравнения с изменением оценок после лечения тиосульфатом натрия, когда все другие лекарства останутся стабильными.Исследуемое лечение будет представлять собой 16 г / м2 тиосульфата натрия, вводимого 3 раза в неделю в течение 10 недель в Национальном институте здравоохранения. Субъекты, завершившие 10 недель лечения или достигшие основной конечной точки к 6 неделе, будут считаться завершившими лечение. После периода лечения все участники вернутся в NIH для оценки на 24-й и 62-й неделе.
Первичным результатом будет изменение баллов по визуальной аналоговой шкале активности кальциноза от недели 0 до 10 недели лечения по сравнению с исходным изменением баллов по визуальной аналоговой шкале активности кальциноза от недели -10 до недели 0 до лечения.Вторичные меры будут оценивать безопасность и изменения в компонентах инструмента оценки кальциноза, клинические оценки кальциноза, анкеты по кальцинозу Модсли, качество жизни, функциональную инвалидность, мышечное тестирование (ручное и количественное), лабораторные параметры (мышечные ферменты, маркеры воспаления и эндотелиальный индекс). маркеры активации), экспрессия генов, патогенез кальцификации, время до улучшения и визуализация. Активность и повреждение миозитов также будут оцениваться с помощью проверенных мер.
В это клиническое испытание будет включен ряд научных исследований с целью понять иммунологические маркеры, связанные с кальцификацией при дерматомиозите, а также иммунологические эффекты лечения тиосульфатом натрия.
| | Loes ModdermanТиосульфат натрияТакже называемая гипосульфитом натрия или гипо , эта неорганическая соль играет центральную роль в фотографии из-за ее полезности для растворения солей серебра во время проявления пленочных эмульсий.Тиосульфат натрия также широко используется в кожевенной промышленности и в качестве промежуточного химического вещества или реагента для синтеза других, более сложных химических веществ. Производимый в основном из побочных продуктов, образующихся при производстве сульфида натрия и серных красителей, тиосульфат натрия также может быть синтезирован из карбоната натрия, диоксида серы и серы с помощью многостадийного процесса. В качестве фармацевтического агента тиосульфат натрия полезен при лечении ранних стадий активного ревматоидного артрита, а также используется для лечения красной волчанки.Однако наиболее важным лекарственным средством является противоядие от отравления цианидом. Тиосульфат натрия имеет формульную массу 248,17 и хорошо растворяется в воде, но не растворяется в этаноле. НАЗАД В ГАЛЕРЕЮ LOES MODDERMAN Вопросы или комментарии? Отправить нам письмо.Микрофотографии © 2000-2021 Loes Modderman.Все права защищены законом об авторском праве. © 1995-2021, автор — Майкл В.Дэвидсон и Государственный университет Флориды. Все права защищены. Никакие изображения, графика, программное обеспечение, сценарии или апплеты не могут быть воспроизведены или использованы каким-либо образом без разрешения правообладателей. Использование этого веб-сайта означает, что вы соглашаетесь со всеми юридическими положениями и условиями, изложенными владельцами.Этот веб-сайт поддерживается нашимКоманда графического и веб-программирования в сотрудничестве с оптической микроскопией в Национальной лаборатории сильного магнитного поля . Последнее изменение: пятница, 13 ноября 2015 г., 14:18Счетчик доступа с 15 февраля 2002 г .: 12950Микроскопы предоставлены: |
Оценка нейтрализующего действия тиосульфата натрия на микротвердость дентина, обработанного гипохлоритом натрия | BMC Oral Health
Haikel Y, Gorce F, Allemann C, VOEGEL JC. Эффективность растворов для эндодонтического орошения на десорбцию белка in vitro.Инт Эндод Дж. 1994; 27 (1): 16–20.
Pascon FM, Kantovitz KR, Sacramento PA, Nobre-dos-Santos M, Puppin-Rontani RM. Влияние гипохлорита натрия на механические свойства дентина: обзор. J Dent. 2009. 37 (12): 903–8.
Артикул Google Scholar
Сахеби С., Моазами Ф., Эбботт П. Влияние кратковременного применения гидроксида кальция на прочность дентина. Dent Traumatol. 2010. 26 (1): 43–6.
Артикул Google Scholar
Сахеби С., Набавизаде М., Долатхах В., Джамшиди Д. Кратковременное влияние гидроксида кальция, минерального заполнителя триоксида и обогащенной кальцием смеси цемента на прочность дентина корня крупного рогатого скота. Иранский эндодонтический журнал. 2012; 7 (2): 68.
Google Scholar
Моазами Ф., Сахеби С., Джамшиди Д., Алави А. Долгосрочное влияние гидроксида кальция, обогащенной кальцием смеси цемента и минерального триоксидного заполнителя на прочность дентина.Иран Эндод Дж. 2014; 9 (3): 185.
PubMed PubMed Central Google Scholar
Byström A, Sundqvist G. Бактериологическая оценка эффекта 0,5% гипохлорита натрия в эндодонтической терапии. Oral Surg Oral Med Oral Pathol. 1983; 55 (3): 307–12.
Гроссман Л.И., Мейман Б.В. Растворение ткани пульпы химическими агентами. J Am Dent Assoc. 1941; 28 (2): 223–5.
Артикул Google Scholar
Ли Б-С, Се Т-Т, Чи DC-Х, Лань Ш-Х, Лин Ц-П. Роль органических тканей на прочность человеческого дентина на сдвиг. J Dent. 2004. 32 (2): 101–7.
Souza EM, Calixto AM, e Lima CN, Pappen FG, De-Deus G. Аналогичное влияние стабилизированных щелочных и нейтральных растворов гипохлорита натрия на сопротивление переломам коровьих зубов, обработанных корневыми каналами. Дж. Эндод. 2014. 40 (10): 1600–3.
Соуза Е.М., Квадрос JdRP, Сильва Е.Дж., Де-Деус Дж., Белладонна Ф.Г., Майя-Филхо Е.М.Объем и / или время NaOCl влияет на прочность на излом коровьих зубов, подвергнутых эндодонтическому лечению. Браз Дент Дж. 2019; 30 (1): 31–5.
Чжан К., Ким Ю.К., Каденаро М., Брайан Т.Э., Сидоу С.Дж., Лушин Р.Дж. и др. Влияние различной продолжительности воздействия и концентраций гипохлорита натрия / этилендиаминтетрауксусной кислоты на структурную целостность минерализованного дентина. Дж. Эндод. 2010. 36 (1): 105–9.
Артикул Google Scholar
Zhang K, Tay FR, Kim YK, Mitchell JK, Kim JR, Carrilho M, et al. Влияние первоначального орошения двумя различными концентрациями гипохлорита натрия на эрозию инструментального корешкового дентина. Dent Mater. 2010. 26 (6): 514–23.
Артикул Google Scholar
Hu X, Peng Y, Sum C-p, Ling J. Влияние концентраций и времени воздействия гипохлорита натрия на депротеинизацию дентина: исследование инфракрасной спектроскопии с преобразованием Фурье с ослабленным полным отражением.Дж. Эндодо. 2010; 36 (12): 2008–11.
Сантос Дж. Н., де Оливейра Каррильо М. Р., Де Гус М. Ф., Зайя А. А., де Алмейда Гомес БПФ, де Соуза-Филью Ф. Дж. И др. Влияние химических ирригантов на прочность сцепления самопротравливающего клея с дентином пульпарной камеры. Дж. Эндод. 2006. 32 (11): 1088–90.
Артикул Google Scholar
Фарина А.П., Чеккин Д., Барбизам Дж. В., Карлини-Джуниор Б. Влияние эндодонтических ирригантов на прочность сцепления самопротравливающегося клея.Ост Эндод Дж. 2011; 37 (1): 26–30.
Артикул Google Scholar
Моррис, доктор медицины, Ли К.В., Эйджи К.А., Буйлаге С., Пэшли Д.Х. Влияние гипохлорита натрия и RC-преп на прочность сцепления полимерного цемента с эндодонтическими поверхностями. Дж. Эндод. 2001. 27 (12): 753–7.
Артикул Google Scholar
Erdemir A, Ari H, Güngüneş H., Belli S. Влияние лекарств для лечения корневых каналов на адгезию к дентину корневого канала.Дж. Эндод. 2004. 30 (2): 113–6.
Артикул Google Scholar
Лай С., Мак И, Чунг Дж., Осорио Р., Толедано М., Карвалью Р. и др. Восстановление нарушенной адгезии к окисленному протравленному дентину. J Dent Res. 2001. 80 (10): 1919–24.
Артикул Google Scholar
Francescantonio MD, Nurrohman H, Takagaki T., Nikaido T., Tagami J, Giannini M. Влияние гипохлорита натрия на прочность адгезии дентина и образование кислотно-щелочной зоны адгезивными системами.Braz J Oral Sci. 2015; 14 (4): 334–40.
Артикул Google Scholar
Алькхудхайри Ф.И., Яман П., Деннисон Дж., Макдональд Н., Эрреро А., Бин-Шувайш М.С. Влияние различных растворов для орошения на прочность сцепления столбиков из цементированного волокна. Clin Cosmet Investig Dent. 2018; 10: 221.
Артикул Google Scholar
Могхаддас М.Дж., Моосави Х., Гавамнасири М.Оценка микроподтекания адгезивных систем после орошения пульповой камеры гипохлоритом натрия. J Dent Res Dent Clin Dent Перспективы. 2014; 8 (1): 21.
PubMed PubMed Central Google Scholar
Вонгпхан Н., Сенавонгсе П., Сомсири В., Харнираттисаи С. Влияние аскорбата натрия на прочность сцепления адгезивной системы полного травления с дентином, обработанным NaOCl, при микропрочном растяжении. J Dent. 2005. 33 (8): 689–95.
Артикул Google Scholar
Weston CH, Ito S, Wadgaonkar B, Pashley DH. Влияние времени и концентрации аскорбата натрия на обратное снижение прочности связи, вызванное NaOCl. Дж. Эндод. 2007. 33 (7): 879–81.
Артикул Google Scholar
Прасансуттипорн Т., Накадзима М., Кунавароте С., Фокстон Р.М., Тагами Дж. Влияние восстановителей на прочность сцепления с дентином, обработанным NaOCl. Dent Mater. 2011. 27 (3): 229–34.
Артикул Google Scholar
Corrêa ACP, Cecchin D, de Almeida JFA, de Almeida Gomes BPF, Zaia AA, Ferraz CCR. Тиосульфат натрия для восстановления прочности сцепления с дентином, обработанным гипохлоритом натрия. Дж. Эндод. 2016; 42 (2): 284–8.
Артикул Google Scholar
Aruoma OI, Cuppett SL. Антиоксидантная методология: концепции in vivo и in vitro: Американское общество химиков масел; 1997.
Йост Дж., Баханс К., Курбебайс М., Тран Т.-А, Лингларт А., Бенистан К. и др.Тиосульфат натрия для местного применения: лечение кальцификатов при гиперфосфатемическом семейном опухолевом кальцинозе? J Clin Endocrinol Metab. 2016; 101 (7): 2810–5.
Артикул Google Scholar
Pasch A, Schaffner T, Huynh-Do U, Frey BM, Frey FJ, Farese S. Тиосульфат натрия предотвращает кальцификацию сосудов у уремических крыс. Kidney Int. 2008. 74 (11): 1444–53.
Артикул Google Scholar
Nasi S, Ea H-K, Lioté F, So A, Busso N. Тиосульфат натрия предотвращает минерализацию хондроцитов и снижает тяжесть остеоартрита у мышей. PLoS ONE. 2016; 11 (7): e0158196.
Артикул Google Scholar
Massoud SF, Moussa SM, Hanafy SA, El Backly RM. Оценка микротвердости дентина корневого канала после различных протоколов ирригации (исследование in vitro). Алекс Дент Дж. 2017; 42 (1): 73–9.
Артикул Google Scholar
Кокрейн С., Берроу М., Парашос П. Влияние внутриканальных лекарственных препаратов и ирригантов на механические свойства дентина человека и крупного рогатого скота. Aust Dent J. 2019; 64 (1): 35–42.
Артикул Google Scholar
Марселино APM, Бруниера Дж. Ф., Рейчел-Юниор FA, Сильва SRCd, Мессиас, округ Колумбия. Влияние химических средств для обработки поверхности на микротвердость и прочность на изгиб корневого дентина. Braz Oral Res. 2014; 28 (1): 1–6.
Aslantas EE, Buzoglu HD, Altundasar E, Serper A. Влияние ЭДТА, гипохлорита натрия и хлоргексидина глюконата с модификаторами поверхности или без них на микротвердость дентина. Дж. Эндод. 2014; 40 (6): 876–9.
Артикул Google Scholar
Гарсия А.Дж., Куга М.С., Пальма-Дибб Р.Г., Со М.В., Мацумото М.А., Фариа Г. и др. Влияние гипохлорита натрия в нескольких составах на микротвердость дентина корневого канала. J Исследование Clin Dent.2013. 4 (4): 229–32.
Артикул Google Scholar
Слуцки-Гольдберг И., Мари М., Либерман Р., Хелинг И. Влияние гипохлорита натрия на микротвердость дентина. Дж. Эндод. 2004. 30 (12): 880–2.
Артикул Google Scholar
Тиосульфат натрия 0,0500 N (N / 20) в водном растворе
Положения и условия
Спасибо, что посетили наш сайт.Эти условия использования применимы к веб-сайтам США, Канады и Пуэрто-Рико (далее «Веб-сайт»), которыми управляет VWR («Компания»). Если вы заходите на веб-сайт из-за пределов США, Канады или Пуэрто-Рико, пожалуйста, посетите соответствующий международный веб-сайт, доступный по адресу www.vwr.com, для ознакомления с применимыми условиями. Все пользователи веб-сайта подчиняются следующим условиям использования веб-сайта (эти «Условия использования»). Пожалуйста, внимательно прочтите эти Условия использования перед доступом или использованием любой части веб-сайта. Заходя на веб-сайт или используя его, вы соглашаетесь с тем, что прочитали, поняли и соглашаетесь соблюдать настоящие Условия использования с поправками, которые время от времени вносятся, а также Политику конфиденциальности компании, которая настоящим включена в настоящие Условия. использования. Если вы не желаете соглашаться с настоящими Условиями использования, не открывайте и не используйте какие-либо части веб-сайта.
Компания может пересматривать и обновлять настоящие Условия использования в любое время без предварительного уведомления, разместив измененные условия на веб-сайте. Продолжение использования вами веб-сайта означает, что вы принимаете и соглашаетесь с пересмотренными Условиями использования.Если вы не согласны с Условиями использования (с внесенными время от времени поправками) или недовольны Веб-сайтом, ваше единственное и исключительное средство правовой защиты — прекратить использование Веб-сайта.
Использование сайта
Информация, содержащаяся на этом веб-сайте, предназначена только для информационных целей. Хотя считается, что информация верна на момент публикации, вам следует самостоятельно определить ее пригодность для вашего использования. Не все продукты или услуги, описанные на этом веб-сайте, доступны во всех юрисдикциях или для всех потенциальных клиентов, и ничто в настоящем документе не предназначено как предложение или ходатайство в любой юрисдикции или какому-либо потенциальному покупателю, где такое предложение или продажа не соответствует требованиям.
Покупка товаров и услуг
Настоящие Условия и положения распространяются только на использование веб-сайта. Обратите внимание, что условия, касающиеся обслуживания, продаж продуктов, рекламных акций и других связанных мероприятий, можно найти по адресу https://us.vwr.com/store/content/externalContentPage.jsp?path=/en_US/about_vwr_terms_and_conditions.jsp , и эти условия регулируют любые покупки продуктов или услуг у Компании.
Интерактивные функции
Веб-сайт может содержать службы досок объявлений, области чата, группы новостей, форумы, сообщества, личные веб-страницы, календари и / или другие средства сообщения или связи, предназначенные для того, чтобы вы могли общаться с общественностью в целом или с группой ( вместе «Функция сообщества»).Вы соглашаетесь использовать функцию сообщества только для публикации, отправки и получения сообщений и материалов, которые являются надлежащими и относятся к конкретной функции сообщества. Вы соглашаетесь использовать веб-сайт только в законных целях.
A. В частности, вы соглашаетесь не делать ничего из следующего при использовании функции сообщества:
1. Оскорблять, оскорблять, преследовать, преследовать, угрожать или иным образом нарушать законные права (например, право на неприкосновенность частной жизни и гласность) других.
2. Публиковать, размещать, загружать, распространять или распространять любую неуместную, непристойную, дискредитирующую, нарушающую авторские права, непристойную, непристойную или незаконную тему, название, материал или информацию.
3. Загружайте файлы, содержащие программное обеспечение или другие материалы, защищенные законами об интеллектуальной собственности (или правами на неприкосновенность частной жизни), если вы не владеете или не контролируете права на них или не получили всех необходимых разрешений.
4. Загрузите файлы, содержащие вирусы, поврежденные файлы или любое другое подобное программное обеспечение или программы, которые могут повредить работу чужого компьютера.
5. Перехватить или попытаться перехватить электронную почту, не предназначенную для вас.
6. Рекламировать или предлагать продавать или покупать какие-либо товары или услуги для любых деловых целей, если такая функция сообщества специально не разрешает такие сообщения.
7. Проводите или рассылайте опросы, конкурсы, финансовые пирамиды или письма счастья.
8. Загрузите любой файл, опубликованный другим пользователем функции сообщества, который, как вы знаете или разумно должен знать, не может распространяться на законных основаниях таким образом или что у вас есть договорное обязательство сохранять конфиденциальность (несмотря на его доступность на веб-сайте).
9. Подделывать или удалять любые ссылки на автора, юридические или другие надлежащие уведомления, обозначения собственности или ярлыки происхождения или источника программного обеспечения или других материалов, содержащихся в загружаемом файле.
10. Представление ложной информации о принадлежности к какому-либо лицу или организации.
11. Участвовать в любых других действиях, которые ограничивают или препятствуют использованию веб-сайта кем-либо или которые, по мнению Компании, могут нанести вред Компании или пользователям веб-сайта или подвергнуть их ответственности.
12. Нарушать любые применимые законы или постановления или нарушать любой кодекс поведения или другие правила, которые могут быть применимы к какой-либо конкретной функции Сообщества.
13. Собирать или иным образом собирать информацию о других, включая адреса электронной почты, без их согласия.
B. Вы понимаете и признаете, что вы несете ответственность за любой контент, который вы отправляете, вы, а не Компания, несете полную ответственность за такой контент, включая его законность, надежность и уместность. Если вы публикуете сообщения от имени или от имени вашего работодателя или другой организации, вы заявляете и гарантируете, что у вас есть на это право. Загружая или иным образом передавая материалы в любую часть веб-сайта, вы гарантируете, что эти материалы являются вашими собственными или находятся в общественном достоянии или иным образом свободны от проприетарных или иных ограничений, и что вы имеете право размещать их на веб-сайте.Кроме того, загружая или иным образом передавая материалы в любую область веб-сайта, вы предоставляете Компании безотзывное, бесплатное право во всем мире на публикацию, воспроизведение, использование, адаптацию, редактирование и / или изменение таких материалов любым способом, в любые и все средства массовой информации, известные в настоящее время или обнаруженные в будущем, во всем мире, в том числе в Интернете и World Wide Web, для рекламных, коммерческих, торговых и рекламных целей, без дополнительных ограничений или компенсации, если это не запрещено законом, и без уведомления, проверки или одобрения.
C. Компания оставляет за собой право, но не принимает на себя никакой ответственности (1) удалить любые материалы, размещенные на веб-сайте, которые Компания по своему собственному усмотрению сочтет несовместимыми с вышеуказанными обязательствами или иным образом неприемлемыми по любой причине ; и (2) прекратить доступ любого пользователя ко всему или части веб-сайта. Однако Компания не может ни просмотреть все материалы до того, как они будут размещены на веб-сайте, ни обеспечить быстрое удаление нежелательных материалов после их размещения.Соответственно, Компания не несет ответственности за какие-либо действия или бездействие в отношении передач, сообщений или контента, предоставленных третьими сторонами. Компания оставляет за собой право предпринимать любые действия, которые она сочтет необходимыми для защиты личной безопасности пользователей этого веб-сайта и общественности; тем не менее, Компания не несет ответственности перед кем-либо за выполнение или невыполнение действий, описанных в этом параграфе.
D. Несоблюдение вами положений пунктов (A) или (B) выше может привести к прекращению вашего доступа к веб-сайту и может подвергнуть вас гражданской и / или уголовной ответственности.
Особое примечание о содержании функций сообщества
Любой контент и / или мнения, загруженные, выраженные или отправленные через любую функцию сообщества или любой другой общедоступный раздел веб-сайта (включая области, защищенные паролем), а также все статьи и ответы на вопросы, кроме контента, явно разрешенного Компания, являются исключительно мнениями и ответственностью лица, представляющего их, и не обязательно отражают мнение Компании.Например, любое рекомендованное или предлагаемое использование продуктов или услуг, доступных от Компании, которое публикуется через функцию сообщества, не является признаком одобрения или рекомендации со стороны Компании. Если вы решите следовать какой-либо такой рекомендации, вы делаете это на свой страх и риск.
Ссылки на сторонние сайты
Веб-сайт может содержать ссылки на другие веб-сайты в Интернете. Компания не несет ответственности за контент, продукты, услуги или методы любых сторонних веб-сайтов, включая, помимо прочего, сайты, связанные с Веб-сайтом или с него, сайты, созданные на Веб-сайте, или стороннюю рекламу, и не делает заявлений относительно их качество, содержание или точность.Наличие ссылок с веб-сайта на любой сторонний веб-сайт не означает, что мы одобряем, поддерживаем или рекомендуем этот веб-сайт. Мы отказываемся от всех гарантий, явных или подразумеваемых, в отношении точности, законности, надежности или действительности любого контента на любых сторонних веб-сайтах. Вы используете сторонние веб-сайты на свой страх и риск и в соответствии с условиями использования таких веб-сайтов.
Права собственности на контент
Вы признаете и соглашаетесь с тем, что все содержимое веб-сайта (включая всю информацию, данные, программное обеспечение, графику, текст, изображения, логотипы и / или другие материалы) и его дизайн, выбор, сбор, расположение и сборка являются являются собственностью Компании и защищены законами США и международными законами об интеллектуальной собственности.Вы имеете право использовать содержимое веб-сайта только в личных или законных деловых целях. Вы не можете копировать, изменять, создавать производные работы, публично демонстрировать или исполнять, переиздавать, хранить, передавать, распространять, удалять, удалять, дополнять, добавлять, участвовать в передаче, лицензировать или продавать какие-либо материалы в Интернете. Сайт без предварительного письменного согласия Компании, за исключением: (а) временного хранения копий таких материалов в ОЗУ, (б) хранения файлов, которые автоматически кэшируются вашим веб-браузером для улучшения отображения, и (в) печати разумного количество страниц веб-сайта; в каждом случае при условии, что вы не изменяете и не удаляете какие-либо уведомления об авторских правах или других правах собственности, включенные в такие материалы.Ни название, ни какие-либо права интеллектуальной собственности на любую информацию или материалы на веб-сайте не передаются вам, а остаются за Компанией или соответствующим владельцем такого контента.
Товарные знаки
Название и логотип компании, а также все связанные названия, логотипы, названия продуктов и услуг, появляющиеся на веб-сайте, являются товарными знаками компании и / или соответствующих сторонних поставщиков. Их нельзя использовать или повторно отображать без предварительного письменного согласия Компании.
Отказ от ответственности
Компания не несет никакой ответственности за материалы, информацию и мнения, предоставленные или доступные через Веб-сайт («Контент сайта»). Вы полагаетесь на Контент сайта исключительно на свой страх и риск. Компания не несет никакой ответственности за травмы или убытки, возникшие в результате использования любого Контента Сайта.
ВЕБ-САЙТ, СОДЕРЖАНИЕ САЙТА И ПРОДУКТЫ И УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ ИЛИ ДОСТУПНЫЕ ЧЕРЕЗ САЙТ, ПРЕДОСТАВЛЯЮТСЯ НА УСЛОВИЯХ «КАК ЕСТЬ» И «ПО ДОСТУПНОСТИ», СО ВСЕМИ ОШИБКАМИ.КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ДАЕТ НИКАКИХ ГАРАНТИЙ ИЛИ ЗАЯВЛЕНИЙ В ОТНОШЕНИИ КАЧЕСТВА, ТОЧНОСТИ ИЛИ ДОСТУПНОСТИ ВЕБ-САЙТА. В частности, НО БЕЗ ОГРАНИЧЕНИЯ ВЫШЕИЗЛОЖЕННОГО, НИ КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ГАРАНТИРУЕТ ИЛИ ЗАЯВЛЯЕТ, ЧТО ВЕБ-САЙТ, СОДЕРЖАНИЕ САЙТА ИЛИ УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ НА САЙТЕ ИЛИ ЧЕРЕЗ САЙТ, БУДУТ ТОЧНЫМИ, НАДЕЖНЫМИ ИЛИ БЕСПЛАТНЫМИ ИЛИ БЕСПЛАТНЫМИ ЧТО ДЕФЕКТЫ БУДУТ ИСПРАВЛЕНЫ; ЧТО ВЕБ-САЙТ ИЛИ СЕРВЕР, ДЕЛАЮЩИЙ ЕГО ДОСТУПНЫМ, НЕ СОДЕРЖИТ ВИРУСОВ ИЛИ ДРУГИХ ВРЕДНЫХ КОМПОНЕНТОВ; ИНАЧЕ ВЕБ-САЙТ ОТВЕЧАЕТ ВАШИМ ПОТРЕБНОСТЯМ ИЛИ ОЖИДАНИЯМ.КОМПАНИЯ ОТКАЗЫВАЕТСЯ ОТ ВСЕХ ГАРАНТИЙ, ЯВНЫХ ИЛИ ПОДРАЗУМЕВАЕМЫХ, ВКЛЮЧАЯ ЛЮБЫЕ ГАРАНТИИ КОММЕРЧЕСКОЙ ЦЕННОСТИ, ПРИГОДНОСТИ ДЛЯ ОПРЕДЕЛЕННОЙ ЦЕЛИ И НЕ НАРУШЕНИЯ.
НИ ПРИ КАКИХ ОБСТОЯТЕЛЬСТВАХ КОМПАНИЯ ИЛИ ЕЕ ЛИЦЕНЗИАРЫ ИЛИ ПОДРЯДЧИКИ НЕ НЕСЕТ ОТВЕТСТВЕННОСТИ ЗА ЛЮБЫЕ УБЫТКИ ЛЮБОГО РОДА, ПРИ КАКИХ-ЛИБО ЮРИДИЧЕСКИХ ТЕОРИЯХ, ВЫЗВАННЫЕ ИЛИ В СВЯЗИ С ИСПОЛЬЗОВАНИЕМ ВАМИ ИЛИ НЕВОЗМОЖНОСТЬЮ ИСПОЛЬЗОВАТЬ ВЕБ-САЙТ, СОДЕРЖИМОЕ САЙТА, ЛЮБЫЕ УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ НА САЙТЕ ИЛИ ЧЕРЕЗ ВЕБ-САЙТ ИЛИ ЛЮБОЙ САЙТ, ВКЛЮЧАЮЩИЙ ПРЯМЫЕ, КОСВЕННЫЕ, СЛУЧАЙНЫЕ, СПЕЦИАЛЬНЫЕ, КОСВЕННЫЕ ИЛИ КАРАТНЫЕ УБЫТКИ, ВКЛЮЧАЯ, НО НЕ ОГРАНИЧИВАЯСЯ, ЛИЧНЫЕ ТРАВМЫ, ПОТЕРЯ ПРИБЫЛИ ИЛИ УБЫТКОВ , ВИРУСЫ, УДАЛЕНИЕ ФАЙЛОВ ИЛИ ЭЛЕКТРОННЫХ СООБЩЕНИЙ, ИЛИ ОШИБКИ, УПУЩЕНИЯ ИЛИ ДРУГИЕ НЕТОЧНОСТИ НА ВЕБ-САЙТЕ ИЛИ СОДЕРЖАНИИ САЙТА ИЛИ УСЛУГ, БЕЗОПАСНОСТЬ ИЛИ НЕОБХОДИМОСТЬ КОМПАНИИ И ПРЕДОСТАВЛЯЛА ЛИ КОМПАНИЯ ПРЕДОСТАВЛЕНИЕ ВОЗМОЖНОСТИ ЛЮБЫЕ ТАКИЕ УБЫТКИ, ЕСЛИ НЕ ЗАПРЕЩЕНЫ ПРИМЕНИМЫМ ЗАКОНОДАТЕЛЬСТВОМ.
Компенсация
Вы соглашаетесь возместить и обезопасить Компанию и ее должностных лиц, директоров, агентов, сотрудников и других лиц, участвующих в работе веб-сайта, от любых обязательств, расходов, убытков и издержек, включая разумные гонорары адвокатам, возникающих в результате любое нарушение вами настоящих Условий использования, использование вами Веб-сайта или любых продуктов, услуг или информации, полученных с Веб-сайта или через него, ваше подключение к Веб-сайту, любой контент, который вы отправляете на Веб-сайт через любые Функция сообщества или нарушение вами каких-либо прав другого лица.
Применимое право; Международное использование
Настоящие условия регулируются и толкуются в соответствии с законами штата Пенсильвания без учета каких-либо принципов коллизионного права. Вы соглашаетесь с тем, что любые судебные иски или иски, вытекающие из настоящих Условий использования или связанные с ними, будут подаваться исключительно в суды штата или федеральные суды, расположенные в Пенсильвании, и вы тем самым соглашаетесь и подчиняетесь личной юрисдикции таких судов для цели судебного разбирательства по любому подобному действию.
Настоящие Условия использования применимы к пользователям в США, Канаде и Пуэрто-Рико. Если вы заходите на веб-сайт из-за пределов США, Канады или Пуэрто-Рико, пожалуйста, посетите соответствующий международный веб-сайт, доступный по адресу www.vwr.com, для ознакомления с применимыми условиями. Если вы решите получить доступ к этому веб-сайту из-за пределов указанных юрисдикций, а не использовать доступные международные сайты, вы соглашаетесь с настоящими Условиями использования и тем, что такие условия будут регулироваться и толковаться в соответствии с законами США и штата. Пенсильвании и что мы не делаем никаких заявлений о том, что материалы или услуги на этом веб-сайте подходят или доступны для использования в этих других юрисдикциях.В любом случае все пользователи несут ответственность за соблюдение местных законов.
Общие условия
Настоящие Условия использования, в которые время от времени могут вноситься поправки, представляют собой полное соглашение и понимание между вами и нами, регулирующее использование вами Веб-сайта. Наша неспособность реализовать или обеспечить соблюдение какого-либо права или положения Условий использования не означает отказ от такого права или положения. Если какое-либо положение Условий использования будет признано судом компетентной юрисдикции недействительным, вы, тем не менее, соглашаетесь с тем, что суд должен попытаться реализовать намерения сторон, отраженные в этом положении и других положениях Условия использования остаются в силе.Ни ваши деловые отношения, ни поведение между вами и Компанией, ни какая-либо торговая практика не может считаться изменением настоящих Условий использования. Вы соглашаетесь с тем, что независимо от какого-либо закона или закона об обратном, любые претензии или основания для иска, вытекающие из или связанные с использованием Сайта или Условий использования, должны быть поданы в течение одного (1) года после такой претензии или причины. иска возникла или будет навсегда запрещена. Любые права, прямо не предоставленные в настоящем документе, сохраняются за Компанией.Мы можем прекратить ваш доступ или приостановить доступ любого пользователя ко всему сайту или его части без предварительного уведомления за любое поведение, которое мы, по нашему собственному усмотрению, считаем нарушением любого применимого законодательства или наносящим ущерб интересам другого пользователя. , стороннего поставщика, поставщика услуг или нас. Любые вопросы, касающиеся настоящих Условий использования, следует направлять по адресу [email protected].
Жалобы на нарушение авторских прав
Мы уважаем интеллектуальную собственность других и просим наших пользователей поступать так же.

 678:006.354
678:006.354