Этапы обмена веществ таблица: обмен веществ и энергии в клетке кратко, процессы (Таблица, схема)
обмен веществ и энергии в клетке кратко, процессы (Таблица, схема)
Метаболизм — это обмен веществ и превращение энергии в клетке, сложная цепь превращений веществ в организме начиная с момента их поступления из внешней среды и кончая удалением продуктов распада. В процессе обмена организм получает вещества для построения клеток и энергию для жизненных процессов. Поэтому выделяются два вида обмена: пластический и энергетический.
Пластическим обменом (анаболизм или ассимиляция) — это совокупность реакций, способствующих построению клетки и обновлению ее состава.
Энергетический обмен (катаболизм, диссимиляция) — совокупность реакций, обеспечивающих клетку энергией.
Метаболизм его процессы катаболизм и анаболизм таблица
|
Признаки |
Катаболизм (диссимиляция) |
Анаболизм (ассимиляция) |
|
Определение |
Катаболизм — это совокупность ферментативных реакций в живом организме, направленных на расщепление сложных органических веществ (белков, липидов, углеводов, нуклеиновых кислот), поступающих с пищей или запасенных в самом организме. |
Анаболизм — это совокупность химических процессов в живом организме, направленных на образование и обновление структурных частей клеток и тканей. При этом идет синтез сложных молекул (белков, жиров, углеводов) из более простых с накоплением энергии. |
|
Вид обмена |
Энергетический обмен |
Пластический обмен |
|
Энергии |
— Освобождает энергию АТФ — Потенциальная энергия, превращенная в кинетическую энергию |
— Требуется энергия от распада АТФ, окисления неорганических веществ, солнечного света — Кинетическая энергия, превращенная в потенциальную энергию |
|
АТФ |
образуется, накапливается |
расходуется |
|
Тип реакции |
экзэргонических |
эндергонических |
|
Гормоны |
Адреналин, глюкагон, цитокины, кортизол |
Эстроген, тестостерон, гормон роста, инсулин |
|
Значение |
— Обеспечивает энергию для анаболизма — нагревает тело — Позволяет сокращать мышцы |
— Поддерживает новый рост клеток — Поддерживает хранение энергии — Техобслуживание тканей |
|
Кислород |
Использует кислород |
Не использует кислород |
|
Процессы (примеры) |
К катаболическим процессам относятся реакции биологического окисления: — Дыхание клеток — Гликолиз — Брожение — Пищеварение — Экскреция |
К анаболическим процессам относятся: — Биосинтез белка — Хемосинтез — Фотосинтез растений — Ассимиляция у животных |
Схема обмен веществ и энергии в клетке — метаболизм
Схема метаболизма (вариант 2)
_______________
Источник информации:
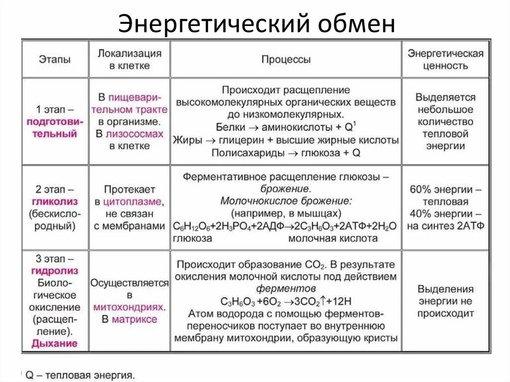 — 2004.
— 2004.Этапы энергетического обмена – Российский учебник
Живой организм построен из клеток. А некоторые, например, амеба или инфузория, состоят из одной клетки. Сложные многоклеточные особи представлены сочетаниями клеток, которые образуют различные системы организма: дыхательную или пищеварительную. Весь организм пронизан клетками нервной ткани, которые обеспечивают регуляцию и управление макроорганизмом.
Живая клетка от неживой отличается тем, что в ней постоянно и непрерывно протекает два разнонаправленных процесса:
- катаболизм, или разрушение питательных элементов с образованием энергии (энергетический обмен или диссимиляция)
В живых особях баланс между ассимиляцией и диссимиляцией поддерживается не всегда. Если наблюдать за жизнью организма, можно заметить, что сначала тело становится больше по размерам, крепче и выносливее.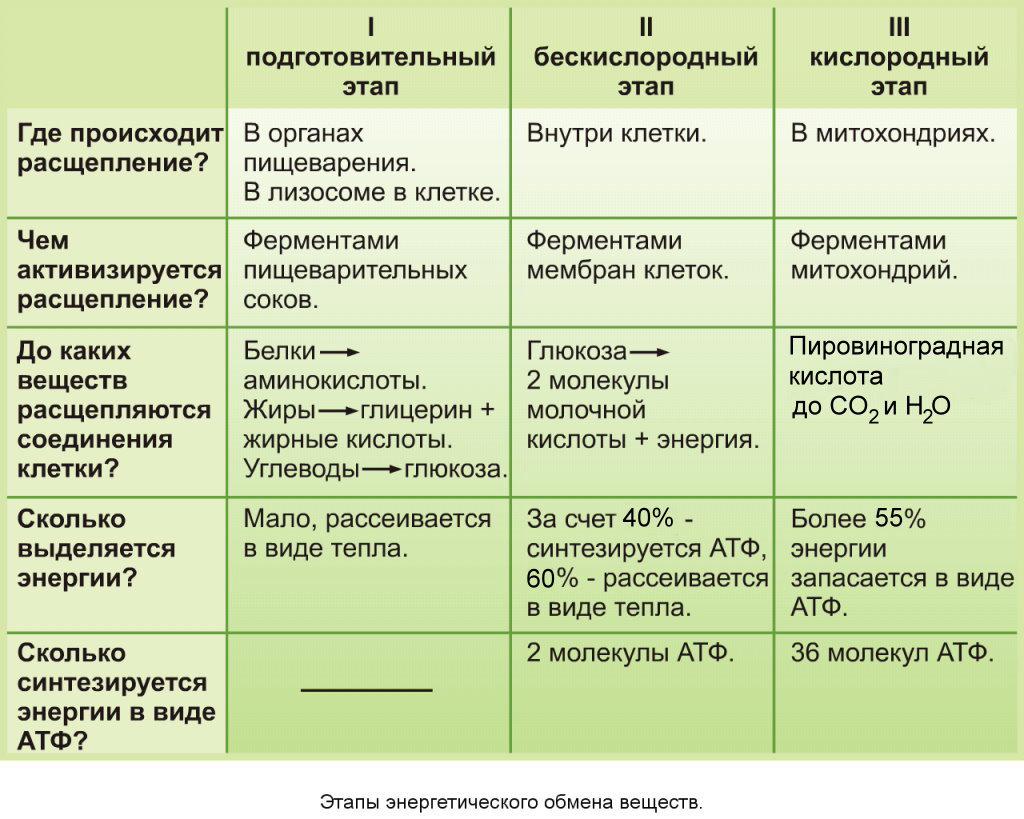 Чем старше становится организм, тем меньше заметен рост, а в старости начинают преобладать процессы распада, организм не успевает восстанавливаться и погибает.
Чем старше становится организм, тем меньше заметен рост, а в старости начинают преобладать процессы распада, организм не успевает восстанавливаться и погибает.
Чтобы машина ехала, ей нужен бензин. А бензин делают из нефти. Чтобы макроорганизм существовал, ему нужна энергия. В учебниках биологии часто можно встретить фразу глюкоза — ресурс энергии для клетки. Это так. Но глюкоза — как нефть для автомобиля. Поэтому сначала глюкозу нужно превратить в бензин. И таким бензином для клетки будет молекула АТФ.
Молекула АТФ известна миру довольно давно. Через десять лет, в 2029 году отпразднует сто лет со дня открытия вещество, благодаря которому в живой клетке поддерживается упорядоченность структур и она может противостоять хаосу и растущей энтропии (почему так происходит, подробно рассказано на странице 30 учебника «Естествознание 11 класс» под редакцией Титова С.А.).
В 1929 году, практически одновременно, сотрудники Института биологии кайзера Вильгельма в Берлине Карл Ломан и Отто Мейергоф и ученые Гарвардской Медицинской школы Сайрус Фиске и Йеллапрагад Суббарао в Гарвардской Медицинской школе опубликовали работы, в которых описали молекулу АТФ.
В 30 годах ХХ века в лаборатории Мейергофа появился молодой ученый, Фриц Липман, который заинтересовался энергетическими аспектами клеточного метаболизма, и в 1941 году талантливый биохимик доказал, что АТФ – основной двигатель энергетических реакций в живой клетке. А в 1953 году его вклад в физиологию совместно с Х. Кребсом был удостоен Нобелевской премии.
АТФ — аденозинтрифосфат, нуклеотид, глобальный ресурс энергии для сложных реакций обмена веществ, происходящих в клетках организма. Схематично молекула АТФ представлена на странице 99 учебника «Естествознание 11 класс» под редакцией Титова С.А..
Вся суть энергетического обмена сводится к решению задачи, как энергию из сложных молекул пищи превратить в молекулу АТФ. В процессе эволюции эта задача была решена.
Так как же булочка из Макдональдса превращается в энергию макроэргических связей АТФ?
В энергетическом обмене выделяют несколько процессов, разделенных не только временем, но и протекающих в различных частях клетки:
- Подготовительный этап
- Гликолиз
- Кислородное окисление
Естествознание. 10 класс. Учебник
10 класс. Учебник
Учебник отличаются качественным современным оформлением, в нём приводятся многочисленные слайды и микрофотографии. Выполняя проблемные, поисковые и исследовательские задания, школьники не только активно усваивают материал, но и учатся мыслить, искать и анализировать информацию из разных источников, в том числе из интернета. Особое внимание уделяется практическим заданиям: ученикам предлагается проводить опыты, конструировать модели, разрабатывать проекты.
Подготовительный этап у человека и других многоклеточных макроорганизмов начинается в ротовой полости, продолжается в желудочно-кишечном тракте и представляет собой многоступенчатый процесс распада сложных полимеров белков, жиров и углеводов пищи до мономеров.
Из курса химии помним, что во время разрыва связей элементов выделяется энергия. Для образования аденозинтрифосфата этой энергии недостаточно, и она вся уходит во внешнюю среду.
Что же происходит у простых одноклеточных организмов, у которых нет ротиков и животиков? Пища, захваченная одноклеточным организмом, попадает в пищеварительную вакуоль или лизосому, где при помощи ферментов-катализаторов, способствующих пищеварению, протекает начальный этап диссимиляции.
Подготовленные во время предварительного этапа вещества переходят во второй бескислородный этап энергетического обмена, который называется гликолиз.
Два греческих слова (гликос – «сладкий» и лизис – «расщеплять») дали название второй бескислородной фазе энергетического обмена — глико́лизу.
Гликолиз является цепочкой из 10 биохимических превращений, итогом которых является трансформация стабильной молекулы глюкозы в трехуглеродные молекулы
Что ещё почитать?
«Подождите, – могут сказать дотошные ученики, – глюкоза у нас находится в пищеварительной системе. А процессы метаболизма идут в клетках по всему организму, например, на кончике носа или задней лапе. Как же попадает глюкоза в цитоплазму клетки во всем организме?».
А процессы метаболизма идут в клетках по всему организму, например, на кончике носа или задней лапе. Как же попадает глюкоза в цитоплазму клетки во всем организме?».Глюкоза всасывается в желудочно-кишечном тракте, попадает в кровоток, током крови разносится ко всем тканям и клеткам организма, и благодаря белку-переносчику инсулину попадает в клетку.
Цитоплазма отдельной клетки – место осуществления реакций гликолиза. Энергии при этом выделяется совсем немного. Ее хватает лишь на формирование 2-х молекул АТФ. Казалось бы, энергия получена, и процесс может остановиться. Так и происходит у некоторых бактерий. Но никакому нормальному многоклеточному организму таких запасов АТФ не хватит. В пировиноградной кислоте остался еще достаточный запас энергии, которую тоже хотелось бы использовать макроорганизму.
Естествознание. 11 класс. Учебник
Учебник отличаются качественным современным оформлением, в нём приводятся многочисленные слайды и микрофотографии. Выполняя проблемные, поисковые и исследовательские задания, школьники не только активно усваивают материал, но и учатся мыслить, искать и анализировать информацию из разных источников, в том числе из интернета. Особое внимание уделяется практическим заданиям: ученикам предлагается проводить опыты, конструировать модели, разрабатывать проекты.
Выполняя проблемные, поисковые и исследовательские задания, школьники не только активно усваивают материал, но и учатся мыслить, искать и анализировать информацию из разных источников, в том числе из интернета. Особое внимание уделяется практическим заданиям: ученикам предлагается проводить опыты, конструировать модели, разрабатывать проекты.
У многоклеточных тел пируват переходит в третью фазу диссимиляции — клеточное дыхание в митохондриях. Дыханием процесс называется, поскольку в ходе химических реакций в митохондриях происходит потребление кислорода и выделение углекислого газа в цитоплазму клетки, а дальше, с помощью кровообращения и дыхания, – во внешнюю среду.
Клеточное дыхание представлено двумя этапами:
- цикл Кребса, протекающий в матриксе митохондрий
- окислительное фосфорилирование, протекающее на кристах митохондрий при участии ферментов дыхательной цепи
Итогом кислородного этапа энергетического обмена является выделение количества энергии, достаточного для образования 36 молекул АТФ, воды и СО2.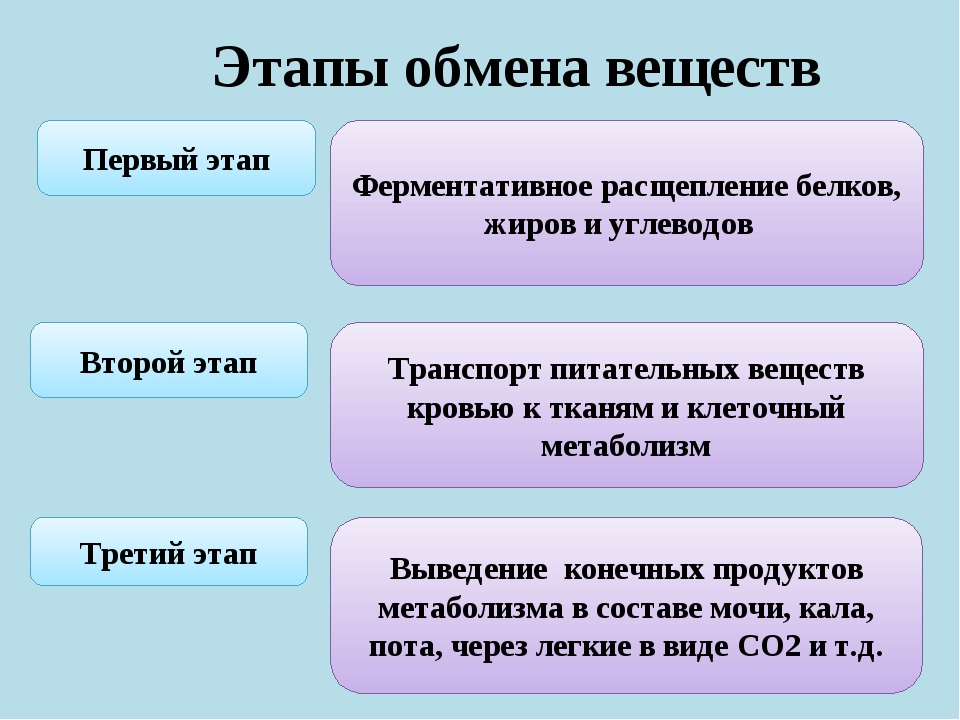 При этом нужно помнить, что аденозинтрифосфат содержит три остатка фосфата, а макроэргических связей образуется только две. Суммарное уравнение биохимических реакций, протекающих в третьей фазе диссимиляции, можно записать так:
При этом нужно помнить, что аденозинтрифосфат содержит три остатка фосфата, а макроэргических связей образуется только две. Суммарное уравнение биохимических реакций, протекающих в третьей фазе диссимиляции, можно записать так:
2C3H4O3+6O2+36H3PO4+36АДФ=6CO2+42H2O+36АТФ
В итоге этих реакций происходит накопление огромного количества энергии — 36 молекул аденозинтрифосфата против 2-х, что запасаются в процессе гликолиза. Однако поскольку эта фаза требует кислорода для своих реакций, в бескислородной среде процесс протекать не может.
При дефиците кислорода пируват окисляется до лактата. Именно ему принадлежит ощущение приятной боли после хорошей тренировки. У хорошо тренированных людей с активным кровоснабжением и хорошо развитой сетью капилляров нужно затратить большую физическую нагрузку перед тем, как начнет накапливаться молочная кислота.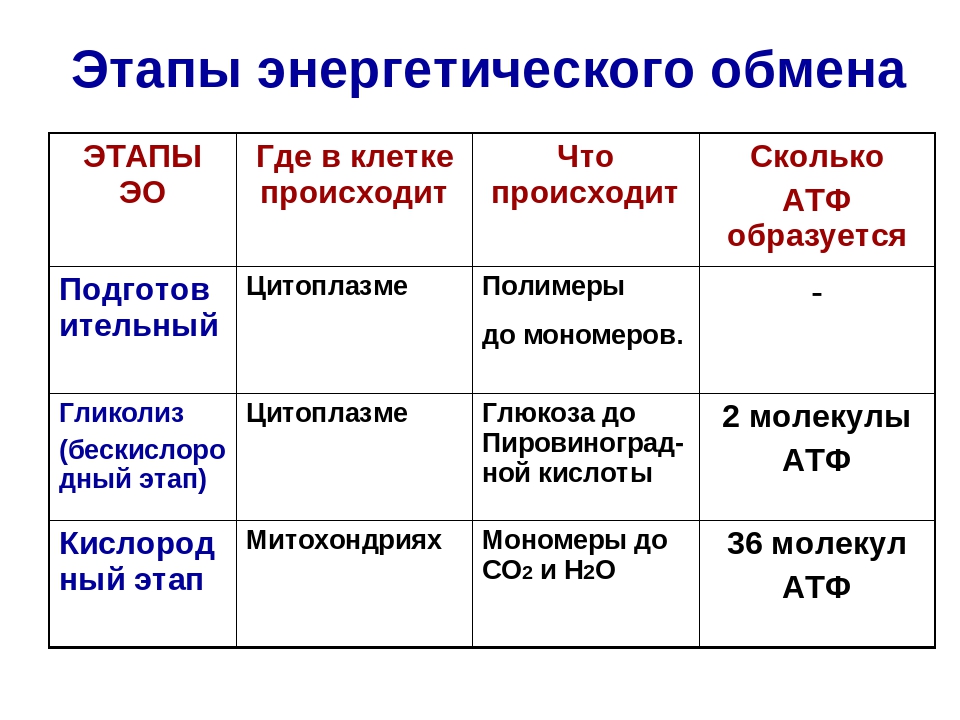
Вспомним, что еще 2 молекулы аденозинтрифосфата накапливаются на этапе гликолиза. Таким образом, при распаде одной молекулы глюкозы образуется 38 молекул АТФ.
На портале LECTA В параграфе 22 учебника «Естествознание 11 класс» под редакцией Титова С.А. внимательные ученики найдут ответ на вопрос, почему цианистый калий – любимое средство убийц в детективных романах.
Тест2. Энергетический обмен (катаболизм, диссимиляция)
Универсальным источником энергии во всех клетках служит АТФ (аденозинтрифосфат, или аденозинтрифосфорная кислота).
Все энергетические затраты любой клетки обеспечиваются за счёт универсального энергетического вещества — АТФ.
АТФ синтезируется в результате реакции фосфорилирования, то есть присоединения одного остатка фосфорной кислоты к молекуле АДФ (аденозиндифосфата):
АДФ + h4PO4+ 40 кДж = АТФ + h3O.
Энергия запасается в форме энергии химических связей АТФ. Химические связи АТФ, при разрыве которых выделяется много энергии, называются макроэргическими.
Химические связи АТФ, при разрыве которых выделяется много энергии, называются макроэргическими.
При распаде АТФ до АДФ клетка за счёт разрыва макроэргической связи получит приблизительно \(40\) кДж энергии.
Энергия для синтеза АТФ из АДФ выделяется в процессе диссимиляции.
Энергетический обмен (диссимиляция, катаболизм) — это совокупность химических реакций постепенного распада органических соединений, сопровождающихся высвобождением энергии, часть которой расходуется на синтез АТФ.
В зависимости от среды обитания организма, диссимиляция может проходить в два или в три этапа.
Процессы расщепления органических соединений у аэробных организмов происходят в три этапа: подготовительный, бескислородный и кислородный.
В результате этого органические вещества распадаются до простейших неорганических соединений.
У анаэробных организмов, обитающих в бескислородной среде и не нуждающихся в кислороде (а также у аэробных организмов при недостатке кислорода), диссимиляция происходит в два этапа: подготовительный и бескислородный.
В двухэтапном энергетическом обмене энергии запасается гораздо меньше, чем в трёхэтапном.
Первый этап — подготовительный
Подготовительный этап заключается в распаде крупных органических молекул до более простых: полисахаридов — до моносахаридов, липидов — до глицерина и жирных кислот, белков — до аминокислот.
Этот процесс называется пищеварением. У многоклеточных организмов он осуществляется в желудочно-кишечном тракте с помощью пищеварительных ферментов. У одноклеточных организмов — происходит под действием ферментов лизосом.
В ходе биохимических реакций, происходящих на этом этапе, энергии выделяется мало, она рассеивается в виде тепла, и АТФ не образуется.
Второй этап — бескислородный (гликолиз)
Второй (бескислородный) этап заключается в ферментативном расщеплении органических веществ, которые были получены в ходе подготовительного этапа. Кислород в реакциях этого этапа не участвует.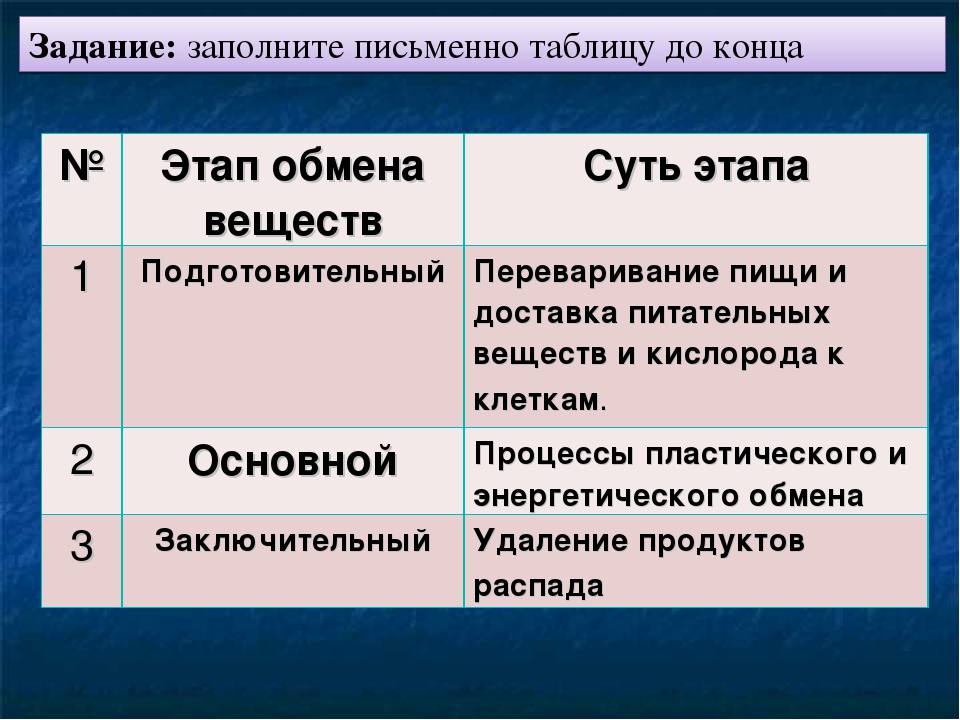
Биологический смысл второго этапа заключается в начале постепенного расщепления и окисления глюкозы с накоплением энергии в виде \(2\) молекул АТФ.
Процесс бескислородного расщепления глюкозы называется гликолиз.
Гликолиз происходит в цитоплазме клеток.
Он состоит из нескольких последовательных реакций превращения молекулы глюкозы C6h22O6 в две молекулы пировиноградной кислоты — ПВК C3h5O3 и две молекулы АТФ (в виде которой запасается примерно \(40\) % энергии, выделившейся при гликолизе). Остальная энергия (около \(60\) %) рассеивается в виде тепла.
C6h22O6+2h4PO4+2АДФ=2C3h5O3+2АТФ +2h3O.
Получившаяся пировиноградная кислота при недостатке кислорода в клетках животных, а также клетках многих грибов и микроорганизмов, превращается в молочную кислоту C3H6O3.
HOOC−CO−Ch4пировиноградная кислота→НАД⋅H+H+лактатдегидрогеназаHOOC−CHOH−Ch4молочная кислота.

В мышцах человека при больших нагрузках и нехватке кислорода образуется молочная кислота и появляется боль. У нетренированных людей это происходит быстрее, чем у людей тренированных.
При недостатке кислорода в клетках растений, а также в клетках некоторых грибов (например, дрожжей), вместо гликолиза происходит спиртовое брожение: пировиноградная кислота распадается на этиловый спирт C2H5OH и углекислый газ CO2:
C6h22O6+2h4PO4+2АДФ=2C2H5OH+2CO2+2АТФ+2h3O.
Третий этап — кислородный
В результате гликолиза глюкоза распадается не до конечных продуктов (CO2 и h3O), а до богатых энергией соединений (молочная кислота, этиловый спирт) которые, окисляясь дальше, могут дать её в больших количествах. Поэтому у аэробных организмов после гликолиза (или спиртового брожения) следует третий, завершающий этап энергетического обмена — полное кислородное расщепление, или клеточное дыхание.
Этот этап происходит на кристах митохондрий.
Третий этап, так же как и гликолиз, является многостадийным и состоит из двух последовательных процессов — цикла Кребса и окислительного фосфорилирования.
Третий (кислородный) этап заключается в том, что при кислородном дыхании ПВК окисляется до окончательных продуктов — углекислого газа и воды, а энергия, выделяющаяся при окислении, запасается в виде \(36\) молекул АТФ (\(2\) молекулы в цикле Кребса и \(34\) молекулы в ходе окислительного фосфорилирования).
Этот этап можно представить себе в следующем виде:
2C3h5O3+6O2+36h4PO4+36АДФ=6CO2+42h3O+36АТФ.
Вспомним, что ещё две молекулы АТФ запасаются в ходе бескислородного расщепления каждой молекулы глюкозы (на втором, бескислородном, этапе). Значит, суммарный результат полного окисления молекулы глюкозы составляет \(38\) молекул АТФ.
Значит, суммарный результат полного окисления молекулы глюкозы составляет \(38\) молекул АТФ.
Суммарное уравнение энергетического обмена:
C6h22O6+6O2=6CO2+6h3O+38АТФ.
В реакциях энергетического обмена используется не только глюкоза, но и липиды, белки. Но главным источником энергии в большинстве клеток являются углеводы.
16. Обмен веществ и превращение энергии. Энергетический обмен
16. Обмен веществ и превращение энергии. Энергетический обмен
Вспомните!
Что такое метаболизм?
Из каких двух взаимосвязанных процессов он состоит?
Где в организме человека происходит расщепление большей части органических веществ, поступающих с пищей?
Обмен веществ и энергии. Главным условием жизни любого организма является обмен веществ и энергии с окружающей средой. В каждой клетке непрерывно происходят сложнейшие процессы, которые направлены на поддержание и обеспечение нормальной жизнедеятельности самой клетки и организма в целом. Синтезируются сложные высокомолекулярные соединения: из аминокислот образуются белки, из простых сахаров – полисахариды, из нуклеотидов – нуклеиновые кислоты. Клетки делятся и образуют новые органоиды, из клетки и в клетку активно транспортируются различные вещества. По нервным волокнам передаются электрические импульсы, сокращаются мышцы, поддерживается постоянная температура тела – на всё это, а также на многие другие процессы, протекающие в организме, требуется энергия. Эта энергия образуется при расщеплении органических веществ. Совокупность реакций расщепления высокомолекулярных соединений, которые сопровождаются выделением и запасанием энергии, называют энергетическим обменом или диссимиляцией. В основном энергия запасается в виде универсального энергоёмкого соединения – АТФ.
Синтезируются сложные высокомолекулярные соединения: из аминокислот образуются белки, из простых сахаров – полисахариды, из нуклеотидов – нуклеиновые кислоты. Клетки делятся и образуют новые органоиды, из клетки и в клетку активно транспортируются различные вещества. По нервным волокнам передаются электрические импульсы, сокращаются мышцы, поддерживается постоянная температура тела – на всё это, а также на многие другие процессы, протекающие в организме, требуется энергия. Эта энергия образуется при расщеплении органических веществ. Совокупность реакций расщепления высокомолекулярных соединений, которые сопровождаются выделением и запасанием энергии, называют энергетическим обменом или диссимиляцией. В основном энергия запасается в виде универсального энергоёмкого соединения – АТФ.
Аденозинтрифосфорная кислота (АТФ) – нуклеотид, состоящий из азотистого основания (аденина), сахара рибозы и трёх остатков фосфорной кислоты (рис. 53). АТФ является главной энергетической молекулой клетки, своего рода аккумулятором энергии. Все процессы в живых организмах, требующие затрат энергии, сопровождаются превращением молекулы АТФ в АДФ (аденозиндифосфорную кислоту). При отщеплении остатка фосфорной кислоты высвобождается большое количество энергии – 40 кДж/моль. Таких высокоэнергетических (так называемых макроэргических) связей в молекуле АТФ две. Восстановление структуры АТФ из АДФ и фосфорной кислоты происходит в митохондриях и сопровождается поглощением энергии.
53). АТФ является главной энергетической молекулой клетки, своего рода аккумулятором энергии. Все процессы в живых организмах, требующие затрат энергии, сопровождаются превращением молекулы АТФ в АДФ (аденозиндифосфорную кислоту). При отщеплении остатка фосфорной кислоты высвобождается большое количество энергии – 40 кДж/моль. Таких высокоэнергетических (так называемых макроэргических) связей в молекуле АТФ две. Восстановление структуры АТФ из АДФ и фосфорной кислоты происходит в митохондриях и сопровождается поглощением энергии.
Запас органических веществ, которые организм расходует для получения энергии, должен постоянно пополняться или за счёт пищи, как это происходит у животных, или путём синтеза из неорганических веществ (растения). Совокупность всех процессов биосинтеза, протекающих в живых организмах, называют пластическим обменом или ассимиляцией. Пластический обмен всегда сопровождается поглощением энергии. Основными процессами пластического обмена являются биосинтез белка (§ 13) и фотосинтез (§ 17).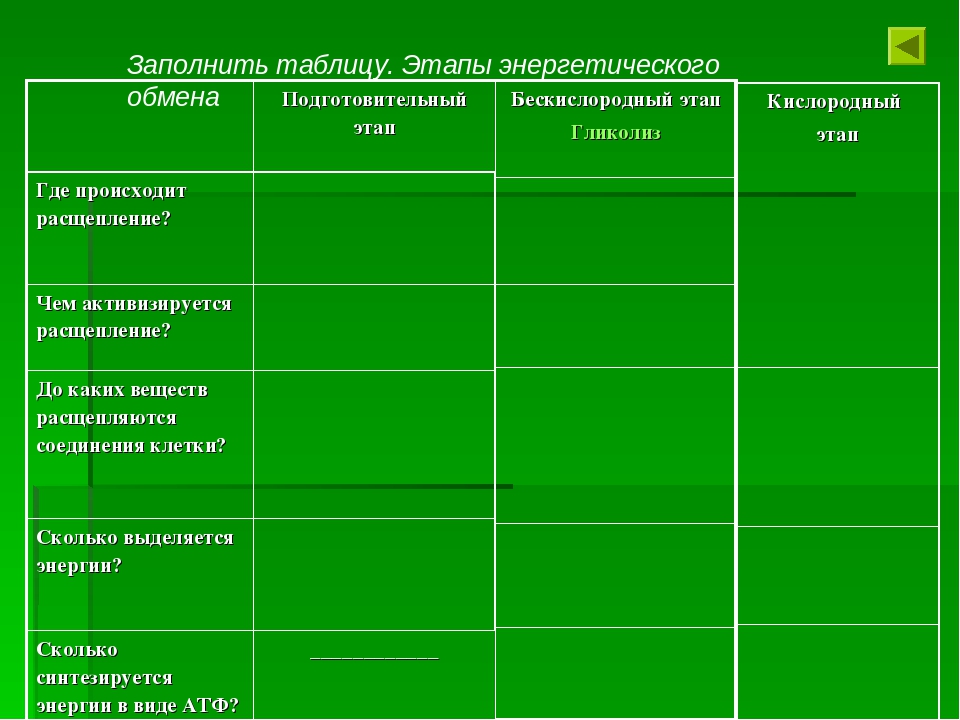
Рис. 53. Строение молекулы АТФ (знаком «~» обозначена макроэргическая связь)
Итак, в процессе энергетического обмена расщепляются органические соединения и запасается энергия, а во время пластического обмена расходуется энергия и синтезируются органические вещества. Реакции энергетического и пластического обмена находятся в неразрывной связи, образуя в совокупности единый процесс – обмен веществ и энергии, или метаболизм. Метаболизм непрерывно осуществляется во всех клетках, тканях и органах, поддерживая постоянство внутренней среды организма – гомеостаз.
Энергетический обмен. Большинству организмов на нашей планете для жизнедеятельности необходим кислород. Такие организмы называют аэробными. Энергетический обмен у аэробов происходит в три этапа: подготовительный, бескислородный и кислородный. При наличии кислорода органические вещества в процессе дыхания полностью окисляются до углекислого газа и воды, в результате чего запасается большое количество энергии.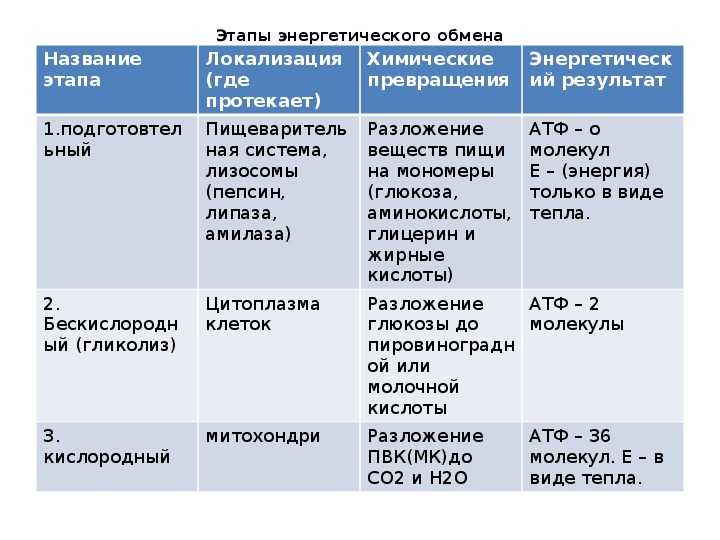
Анаэробные организмы способны обходиться без кислорода. Для некоторых из них кислород вообще губителен, поэтому они живут там, где кислорода нет совсем, как, например, возбудитель столбняка. Другие, так называемые факультативные анаэробы, могут существовать как без кислорода, так и в его присутствии. Энергетический обмен у анаэробных организмов происходит в два этапа: подготовительный и бескислородный, поэтому органические вещества окисляются не полностью и энергии запасается гораздо меньше.
Рассмотрим три этапа энергетического обмена (рис. 54).
Подготовительный этап. Этот этап осуществляется в желудочно-кишечном тракте и в лизосомах клеток. Здесь высокомолекулярные соединения под действием пищеварительных ферментов распадаются до более простых, низкомолекулярных: белки – до аминокислот, полисахариды – до моносахаридов, жиры – до глицерина и жирных кислот. Энергия, которая выделяется при этих реакциях, не запасается, а рассеивается в виде тепла. Низкомолекулярные вещества, образующиеся на подготовительном этапе, могут использоваться организмом для синтеза своих собственных органических соединений, т. е. вступать в пластический обмен или расщепляться дальше с целью запасания энергии.
Низкомолекулярные вещества, образующиеся на подготовительном этапе, могут использоваться организмом для синтеза своих собственных органических соединений, т. е. вступать в пластический обмен или расщепляться дальше с целью запасания энергии.
Рис. 54. Этапы энергетического обмена
Бескислородный этап. Второй этап протекает в цитоплазме клеток, где происходит дальнейшее расщепление простых органических веществ. Аминокислоты, образованные на первом этапе, организм не использует на следующих этапах диссимиляции, потому что они необходимы ему в качестве материала для синтеза собственных белковых молекул. Поэтому для получения энергии белки расходуются очень редко, обычно только в том случае, когда остальные резервы (углеводы и жиры) уже исчерпаны. Обычно самым доступным источником энергии в клетке является глюкоза.
Сложный многоступенчатый процесс бескислородного расщепления глюкозы на втором этапе энергетического обмена называют гликолизом (от греч. glycos – сладкий и lysis – расщепление).
glycos – сладкий и lysis – расщепление).
В результате гликолиза глюкоза расщепляется до более простых органических соединений (глюкоза С6Н12О6 ? пировиноградная кислота С3Н4О3). При этом выделяется энергия, 60 % которой рассеивается в виде тепла, а 40 % используется для синтеза АТФ. При расщеплении одной молекулы глюкозы образуется две молекулы АТФ и две молекулы пировиноградной кислоты. Таким образом, на втором этапе диссимиляции организм начинает запасать энергию.
Дальнейшая судьба пировиноградной кислоты зависит от присутствия кислорода в клетке. Если кислород есть, то пировиноградная кислота поступает в митохондрии, где происходит её полное окисление до СО2 и Н2О и осуществляется третий, кислородный этап энергетического обмена (см. ниже).
При отсутствии кислорода происходит так называемое анаэробное дыхание, которое часто называют брожением. В клетках дрожжей в процессе спиртового брожения пировиноградная кислота (ПВК) превращается в этиловый спирт (ПВК ? Этиловый спирт + СО2).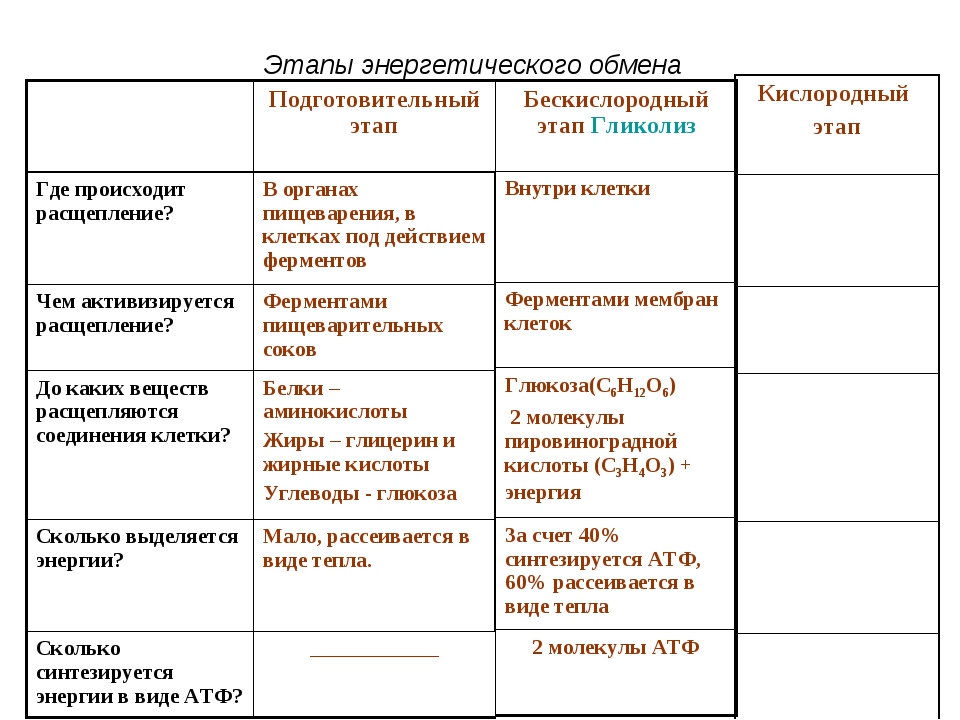
При молочнокислом брожении из ПВК образуется молочная кислота. Этот процесс может происходить не только у молочнокислых бактерий. При напряжённой физической работе в клетках мышечной ткани человека возникает нехватка кислорода, в результате чего образуется молочная кислота, накопление которой вызывает чувство усталости, боль и иногда даже судороги.
Кислородный этап. На третьем этапе продукты, образовавшиеся при бескислородном расщеплении глюкозы, окисляются до углекислого газа и воды. При этом освобождается большое количество энергии, значительная часть которой используется для синтеза АТФ. Этот процесс протекает в митохондриях и называется клеточным дыханием. В ходе клеточного дыхания при окислении двух молекул ПВК выделяется энергия, запасаемая организмом в виде 36 молекул АТФ.
Итак, в процессе энергетического обмена при полном окислении одной молекулы глюкозы до углекислого газа и воды образуется 38 молекул АТФ (2 молекулы – в процессе гликолиза и 36 – в процессе клеточного дыхания в митохондриях):
С6Н12О6 + 6О2 + 38АДФ + 38Ф 6СО2 ? 6Н2О + 38АТФ.
В анаэробных условиях эффективность энергетического обмена значительно ниже – всего 2 молекулы АТФ. Продукты брожения (этиловый спирт, молочная кислота, масляная кислота) в своих химических связях сохраняют ещё много энергии, т. е. более выгодным в энергетическом отношении является кислородный путь диссимиляции. Но исторически брожение – более древний процесс. Он мог осуществляться ещё тогда, когда в атмосфере древней Земли отсутствовал свободный кислород.
Вопросы для повторения и задания
1. Что такое диссимиляция? Перечислите её этапы.
2. В чём заключается роль АТФ в обмене веществ в клетке?
3. Какие структуры клетки осуществляют синтез АТФ?
4. Расскажите об энергетическом обмене в клетке на примере расщепления глюкозы.
5. Изобразите схематично процесс диссимиляции, сведя на одной схеме все возможные его варианты, упомянутые в тексте параграфа (в том числе брожение).
6. Синонимами слов «диссимиляция» и «ассимиляция» являются термины «катаболизм» и «анаболизм». Объясните происхождение этих терминов.
Подумайте! Выполните!
1. Объясните, почему потребление избыточного количества пищи приводит к ожирению.
2. Почему энергетический обмен не может существовать без пластического обмена?
3. Как вы считаете, почему после тяжёлой физической работы, для того чтобы быстрее снять боли в мышцах, рекомендуют принять тёплую ванну?
Работа с компьютером
Обратитесь к электронному приложению. Изучите материал и выполните задания.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРесКонспект урока по биологии» Обмен веществ и энергии.
 Энергетический обмен» ( 10 класс)
Энергетический обмен» ( 10 класс)Тема: «Обмен веществ и превращение энергии. Энергетический обмен.»
10 класс.
Цели урока: Продолжить формирование знаний об обмене веществ, раскрыв сущность энергетического обмена, подвести учащихся к выводу о значении АТФ как универсального аккумулятора энергии в клетке; познакомить учащихся с особенностями трех этапов энергетического обмена на уровне восприятия, осмысления и первичного запоминания.
Задачи:
Образовательные:
приобретение и усвоение знаний учащегося по теме “Обмен веществ и превращение энергии. Энергетический обмен клетки”;
способствовать пониманию закономерности и практической значимости обмена веществ и превращения энергии в жизни человека;
Выяснить, что является источником энергии для всех живых организмов, в результате каких процессов осуществляется образование энергии и ее аккумулирование в клетках;
совершенствовать умения решать задачи на тему «Энергетический обмен», навыки работы с научным текстом, рисунками, видеоматериалом;
Развивающие:
развивать интеллектуальные качества личности — интерес, наблюдательность, решение проблемных вопросов, умение делать выводы и обобщения.

продолжить формирование умений планировать свою деятельность, умений использовать свои предметные знания в повседневной жизни.
Воспитательные:
воспитывать умение работать в заданном темпе;
с помощью межпредметных связей способствовать формированию картины мир
Характер познавательной деятельности:
Репродуктивная — слушаю, запоминаю, работа с книгой.
Продуктивная — поисково-исследовательская — решить задачу, что-то отыскать.
Творческая — решении той или иной задачи повышенной сложности.
Тип урока: изучение нового материала с элементами исследования и практической работы (решение задач по теме)
ХОД УРОКА
I. Актуализация знаний.
Тема нашего урока «Обмен веществ и энергии. Энергетический обмен». Запишите в тетрадь.
Какие ассоциации у вас возникают с этой фразой.
 Предложите различные ассоциации.
Предложите различные ассоциации.
2. Тема состоит из трех слов: обмен, вещества и энергия. Давайте свяжем их.
3. Обмениваются чем? (Веществами и энергией)
4. Что за вещества, откуда они берутся? (Органические – белки, жиры, углеводы, из пищи)
5. Для чего нужна энергия, откуда она берется? (Для обеспечения процессов жизнедеятельности. Из пищи)
6. Что входит в состав пищи? (Белки, жиры, углеводы, вода и минеральные соли).
7. Между чем происходит обмен? (откуда поступает пища, воздух, вода?) (Организмами и наружной средой)
Таким образом, обмен веществ и энергии взаимосвязаны между собой.
Здесь проявляется закон сохранения энергии и вещества – в живом организме материя, или вещества и энергия не создаются и не исчезают, происходит лишь их изменение, поглощение и выделение.
II.Изучение нового материала
Вступление учителя: Как мы уже отмечали, одним из свойств живого является обмен веществ между организмом и окружающей средой.
Вопросы к учащимся:
Как еще научно называется этот процесс? (метаболизм)
Дать, определение этому процессу (совокупность реакций ассимиляции и диссимиляции)
Что представляет собой процесс ассимиляции веществ? (реакции синтеза)
Что представляет собой процесс диссимиляции? (химическоерасщепление – распад вегцеств до конечных продуктов)
Обмен веществ – совокупность химических превращений, происходящих в живом организме и обеспечивающие его рост, жизнедеятельность, воспроизведение и постоянный контакт с окружающей средой.
Схема на доске.
Задача нашего урока:
Выяснить, как осуществляется энергетический обмен в клетках.
Как трансформируется полученная энергия?
Где аккумулируется (запасается) полученная энергия?
Учитель:
Энергетические процессы связаны с освобождением энергии из сложных органических соединений, находящихся изначально в пищевых продуктах, поступающих в наш организм, и происходят во всех живых клетках.
ТАБЛИЦА: III этапа энергетического обмена
На какие стадии можно поделить процесс?
Любой процесс имеет начало, основную стадию и заключение. Так же и обмен веществ и энергии.
В ходе биологического окисления расщепление сложных органических веществ осуществляется поэтапно и может идти двумя принципиально различными путями:
1) бескислородное окисление органических веществ;
2) кислородное окисление органических веществ до углекислого газа и воды.
Начальные этапы обоих видов окисления протекают сходным образом.
I этап — Подготовительный
II этап — Неокислительное — бескислородное расщепление органических веществ
III этап — Окислительное О2 — кислородное расщепление органических веществ
(С6Н10О5)n —>С6Н12О6Ферменты: птиалин, амилаза, мальтаза
Итак, сейчас вам предстоит поработать в группах, и выяснить как происходит обмен веществ и энергии.
У каждой группы свое задание. Из предложенных карточек с терминами и текстами вам необходимо составить логичный текс-схему с помощью, которой вы расскажите о своем задании.
1 гр. Задание
1. описать стадии обмена веществ.
2. значение каждой стадии
3. что такое пластический обмен. Что такое энергетический обмен? Как он взаимосвязаны? (на этот вопрос вы отвечаете после выступления групп)
2 гр. Задание.
1.Из предложенного набора карточек с текстом и терминами составьте логичный текс-схему обмена веществ.
2. определите вид обмена
3.выявите взаимосвязь между веществами и энергией.
3 гр. Задание.
1.Из предложенного набора карточек с текстом и терминами составьте логичный текс-схему бескислородного этапа обмена веществ.
2. определите количество энергии, выделяемого в этом этапе.
3.выявите место локализации.
4 гр. Задание.
1.Из предложенного набора карточек с текстом и терминами составьте логичный текс-схему кислородного этапа обмена веществ.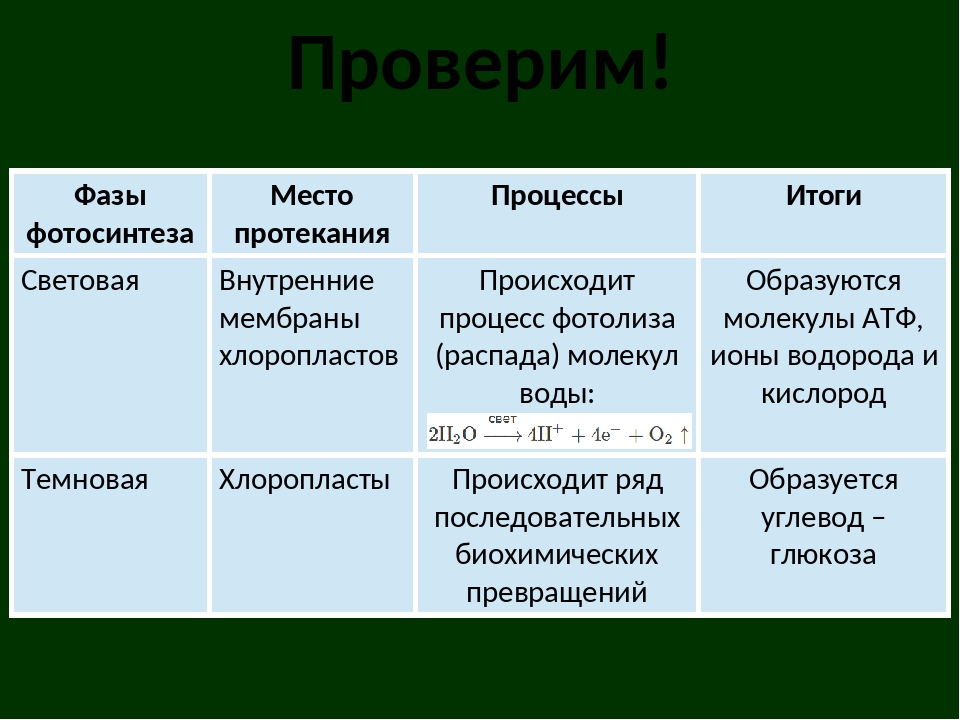
2. определите количество энергии, выделяемого в этом этапе.
3.выявите место локализации.
5 гр. Задание.
1. Рассмотрите цикл Кребса, по предложенной таблице и представьте презентацию.
В первую, подготовительную стадию, крупные молекулы распадаются на более простые: белки расщепляются до аминокислот, полисахариды – до моносахаридов; липиды – до глицерина и высших жирных кислот.
Этот процесс осуществляется в пищеварительном канале многоклеточных организмов, затем – в клетках под действием ферментов лизосом. Выделившаяся энергия в ходе превращения веществ, полностью рассеивается в виде тепла.
Какая общая функция характерна для этих веществ?
– Рационально ли тратить белки на получение энергии? Почему?
– Какие вещества являются основным источником энергии?
Считается, что ключевое место в метаболизме всех типов клеток занимают реакции с участием сахаров, например, глюкозы, поэтому на занятии мы рассмотрим путь окисления именно этого углевода.
Этапы энергетического обмена
II этап (анаэробный)
Второй этап – бескислородный, или неполное окисление. Он называется также анаэробным дыханием (гликолизом) или брожением. Термин “брожение” обычно применяют по отношению к процессам, протекающим в клетках микроорганизмов или растений.
Брожению могут подвергаться многие органические соединения, но чаще всего – углеводы, в результате чего образуются: спирт (этиловый), кислоты (молочная, масляная и др.), ацетон и другие органические соединения, углекислый газ, а в некоторых случаях и водород.
Обязательными участниками гликолиза являются АДФ и Н3РО4. Оба эти вещества всегда имеются в клетке, так как они образуются в результате её жизнедеятельности. В процессе гликолиза из одной молекулы глюкозы образуются 2 молекулы АТФ.
Гликолиз – сложный многоступенчатый процесс, состоящий из 10 следующих друг за другом реакций. Каждую реакцию катализирует свой особый фермент. В результате освобождается небольшое количество энергии порядка 200 кДж/моль глюкозы. 60% данной энергии рассеивается в виде тепла, а 40% — идет на синтез АТФ.
Каждую реакцию катализирует свой особый фермент. В результате освобождается небольшое количество энергии порядка 200 кДж/моль глюкозы. 60% данной энергии рассеивается в виде тепла, а 40% — идет на синтез АТФ.
В клетках человека и животных глюкоза расщепляется до молочной кислоты. Этот вид гликолиза присущ некоторым видам бактерий и грибков и лежит в основе приготовления кислого молока, простокваши, кефира и др. молочнокислых продуктов питания.
Дрожжевые грибки в процессе синтеза АТФ расщепляют глюкозу до этилового спирта и СО2. Происходит спиртовое брожение. Промежуточные реакции гликолиза и спиртового брожения сходны, но конечные продукты различны. На спиртовом брожении основано приготовление вина, пива, кваса. Тесто, замешанное на дрожжах, даёт пористый, вкусный хлеб.
С6Н12О6 + 2Н3РО4 + 2АДФ = 2С2Н5ОН + 2СО2 + 2Н20 + 2АТФ
II этап (анаэробный) — Гликолиз или цикл пировиноградной кислоты.Идет без О2 в цитоплазме клетки
С6Н12О6 —> 2ПВК —> 2С3Н6Оз
С6Н12О6 + 2Н3РО4 + 2АДФ —> 2С3Н6О3 + 2 АТФ + 2Н2О
У растений анаэробный гликолиз идет по типу спиртового брожения. С6Н12Об + 2Н3РО4 + 2АДФ —> 2СО2 + 2С2Н5ОН (этиловый спирт) + 2АТФ + 2Н2О
С6Н12Об + 2Н3РО4 + 2АДФ —> 2СО2 + 2С2Н5ОН (этиловый спирт) + 2АТФ + 2Н2О
Брожение отличается тем, что образуется конечное органическое соединение.
50000 Ккал
200 КДж
Большая часть глюкозы >
2 АТФ
20000 Ккал
80 КДж
> поступает в мышечные органы, т.к. >
40%
> они совершают работу.
Выполните задание:
Задание 1.
Сколько молекул глюкозы необходимо расщепить без участия кислорода, чтобы получить 18 молекул АТФ:
А) 18 Б) 36 В) 9 Г) 27
Задание 2.
На первом этапе своего расщепления глюкоза:
А) окисляется до углекислого газа и воды Б) не изменяется
В) подвергается брожению Г) расщепляется до двух трёхуглеродных молекул.
Третий этап – кислородное расщепление.
Данный этап происходит при участии кислорода и воды поэтому его ещё называют аэробное дыхание и гидролиз. Аэробное дыхание осуществляется в митохондриях. Для того, чтобы понять механизм аэробного дыхания, нужно вспомнить строение митохондрий.
Вспомните и расскажите о строении митохондрий.)
Аэробное дыхание связано с матриксом митохондрий и внутренней мембраной. В этом процессе принимают участие, кроме субстратов еще:
Основное условие нормального течения кислородного процесса — целостность митохондриальных мембран
В процессе аэробного дыхания расщеплению подвергается молочная кислота. Она проникает в митохондрии, где она полностью разрушается.
C3H6O3+3h3O=3CO2+12H
Этот процесс можно разделить на три стадии:
1) Окислительное декарбоксилирование
2) Цикл Кребса
3) Электронтранспортная цепь.
В процессе аэробного дыхания расщеплению подвергается молочная кислота. Она проникает в митохондрии, где она полностью разрушается.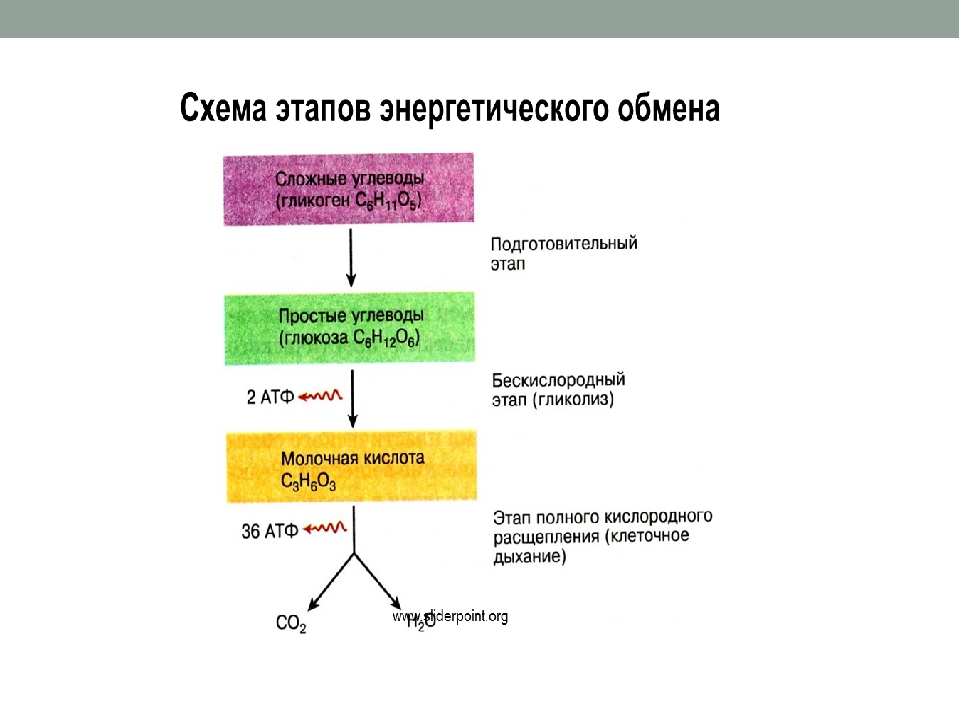
C3H6O3+3h3O=3CO2+12H
Этот процесс можно разделить на три стадии:
1) Окислительное декарбоксилирование
2) Цикл Кребса
3) Электронтранспортная цепь.
2). Цикл Кребса- цикл трикарбоновых кислот, назван в честь англ. учёного Ганса Кребса, открывшего этот процесс. Цикл Кребса протекает в матриксе митохондрий. При взаимодействии ацетил-КоА с щавелево-уксусной кислотой образуется лимонная кислота. Далее осуществляется ряд превращений, заканчивающихся образованием щавелево-уксусной кислоты для нового цикла. Кроме этого выделяется две молекулы СО2, одна молекула АТФ и четыре пары атомов Н. Водородные атомы присоединяются к НАД и попадают в дыхательную цепь.
Неповреждённая митохондриальная мембрана для ионов непроницаема, поэтому на наружной стороне мембраны нарастает концентрация ионов водорода. Вследствие увеличения концентрации протонов эта сторона приобретает положительный заряд. Электроны в свою очередь молекулами переносчиками переправляются на внутреннюю мембрану, где они соединяются с кислородом.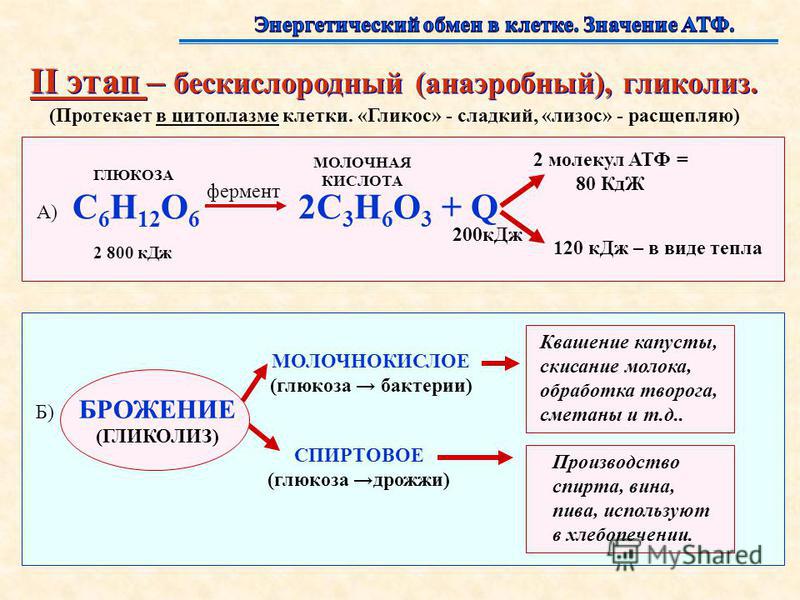 О2 + е =О2-
О2 + е =О2-
Молекулярный кислород диффундирует в митохондрии из окружающей среды. Следовательно, катионы водорода и ионы кислорода по обе стороны мембраны создают разноимённо заряженное электрическое поле.
В некоторых участках мембраны встроены молекулы фермента, синтезирующего АТФ (АТФ-синтетаза). В молекуле АТФ-синтетазы имеется канал, через который могут пройти протоны водорода. Это происходит только в том случае, если разность потенциалов достигнет порядка 200мВ. При достижении этого значения протоны силой электрического поля проталкиваются через протонный канал в молекуле АТФ-синтетазы на внутреннюю сторону мембраны.
На внутренней стороне мембраны протоны водорода взаимодействуют с ионами кислорода и образуют воду: О-2 + 4Н+ = 2 Н2О
При прохождении ионов водорода через канал в молекуле АТФ-синтетазы происходит синтез АТФ из АДФ и фосфорной кислоты.
Многие реакции кислородного расщепления сопровождаются освобождением энергии.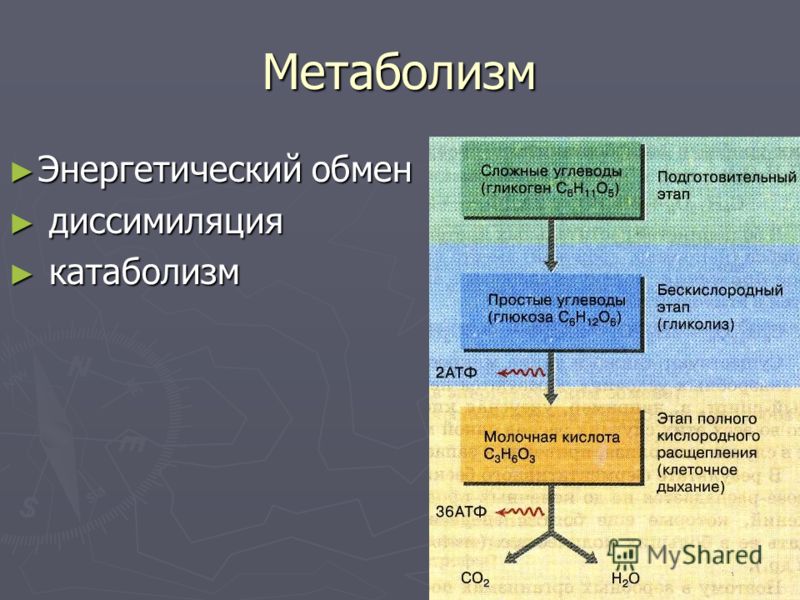 В сумме это довольно большая величина -2600кДж на каждые 2 моля молочной кислоты. 45% этой энергии рассеивается в виде теплоты, а 55% — сберегается в виде АТФ.
В сумме это довольно большая величина -2600кДж на каждые 2 моля молочной кислоты. 45% этой энергии рассеивается в виде теплоты, а 55% — сберегается в виде АТФ.
3. Электронтранспортная цепь
В митохондриях
Процесс кислородного расщепления выражается уравнением:
2С3Н6О3 + 6О2 + 36АДФ+36Н3РО4= 6СО2 +6Н2О + 36АТФ+36Н2О
Просуммировав это уравнение с уравнением гликолиза получим итоговое уравнение:
С6Н12О6 + 2АДФ + 2Н3РО4= 2С3Н6О3 + 2АТФ+2Н2О
2С3Н6О3 +6О2 +36АДФ+36Н3РО4 = 6СО2+36АТФ+42Н2О
_____________________________________________________________
С6Н12О6+6О2+38АДФ+38Н3РО4=6СО2 + 38АТФ + 44Н2О
Это уравнение показывает, что в результате полного расщепления глюкозы образуются конечные продукты распада – вода и углекислый газ, а самое главное – синтезируется 38 молекул АТФ, в которых запасается большая часть энергии.
— идет в присутствии О2 в митохондриях (дыхание)
Делится на 3 подэтапа:
1.Окислительное декарбоксилирование ПВК с отщеплением СО2 на наружной мембране
2. Цикл Кребса (англ. ученый Ганс Кребс, открыл цикл в З0-е годы 1953 г. Нобелевская премия)
З. а) цепь переноса на внутрен. мембр. электронов
б) окислительное фосфорилирование
в) дыхательная цепь открыл в 1931 г. выдающийся русский биохимик В.А.Энгельгард
2ПВК + 6О2 + 36АДФ + 36Ф —>
—> 6СО2 + 42Н2О + 36АТФ
650000 Ккал
2600КДЖ
2АТФ
34АТФ
36 АТФ
360000 Ккал
или 1440
КДж
55%
Итоговое суммарное уравнение:
1 .Упрощенный вариант:
С6Н12О6 + 6О2 —> 6СО2 + 6Н2О
2. C6H206 + 6О2 + 38АДФ + 38Н3РО4 —> 6СО2 + 44Н2О + 38 АТФ
700000 ~
2800 КДж
38 г-м АТФ
~ 1520КДж
Т.е. 55%
Каждый из этих этапов делится на отдельные звенья и представляет собой цепь биохимических процессов. Процессы строго упорядочены. Все реакции осуществляются при участии ферментов — ферментативный конвейер.
II этап (анаэробный) — Гликолиз или цикл пировиноградной кислоты. Идет без О2 в цитоплазме клеткиС6Н2О —> 2ПВК —> 2С3Н6Оз
СбН2О6 + 2Н3РО4 + 2АДФ —>
—> 2С3Н6О3 + 2 АТФ + 2Н2О
У растений анаэробный гликолиз идет по типу спиртового брожения. С6Н12Об + 2Н3РО4 + 2АДФ —> 2СО2 + 2С2Н5ОН (этиловый спирт) + 2АТФ + 2Н2О Брожение отличается тем, что образуется конечное органическое соединение.
50000 Ккал
200 КДж
Большая часть глюкозы >
2 АТФ
20000 Ккал
80 КДж
> поступает в мышечные органы, т.к. >
40%
> они совершают работу.
III этап (аэробный)
— идет в присутствии О2 в митохондриях (дыхание)
Делится на 3 подэтапа:
1.Окислительное декарбоксилирование ПВК с отщеплением СО2 на наружной мембране
2. Цикл Кребса (англ. ученый Ганс Кребс, открыл цикл в З0-е годы 1953 г. Нобелевская премия)
З. а) цепь переноса на внутрен. мембр. электронов
б) окислительное фосфорилирование
в) дыхательная цепь открыл в 1931 г. выдающийся русский биохимик В.А.Энгельгард
2ПВК + 6О2 + 36АДФ + 36Ф —>
—> 6СО2 + 42Н2О + 36АТФ
650000 Ккал
2600КДЖ
2АТФ
34АТФ
36 АТФ
360000 Ккал
или 1440
КДж
55%
Итоговое суммарное уравнение:
1 .Упрощенный вариант:
С6Н12О6 + 6О2 —> 6СО2 + 6Н2О
2. C6H206 + 6О2 + 38АДФ + 38Н3РО4 —> 6СО2 + 44Н2О + 38 АТФ
700000 ~
2800 КДж
38 г-м АТФ
~ 1520КДж
Т.е. 55%
Сравнение анаэробного и аэробного дыхания
1. Локализация в клетке.2. Скорость.
3. Формы энергии.
4. Конечные продукты.
5. Количество АТФ.
6. КПД процесса
7. Условия протекания.
цитоплазма
очень быстро, в 2-3 раза
химическая
ПВК, молочная кислота, этиловый спирт и др.
2 молекулы
32 – 40 %
отсутствие О2
митохондрии
медленнее
химическая, электрохимическая
СО2, Н2О
38 молекул
45 – 55 %
О2, дыхательные ферменты, мембрана
Дыхание
Образуется 38 молекул АТФ.
Митохондрии перекачивают около 500 г протонов Н в день.
АТФ-синтетаза производит около 40 кг АТФ.
Значение дыхания
В результате окисления сохраняется равновесие между продукцией органики и её распадом.
СО2 используется для образования карбонатов, накапливается в осадочных породах.
Сохраняется равновесие между кислородом и углекислым газом в атмосфере
Давайте подведём итоги.
Почему наряду с аэробным дыханием организмы продолжают использовать анаэробное?
Почему более сложные организмы не могли бы развиться в отсутствие кислорода?
Несмотря на то, что синтез АТФ энергетически невыгодный процесс, кпд его достаточно высок. Обратите внимание на следующие данные:
КПД парового двигателя – 12-15 %, турбины ГЭС – 20-25 %, двигателя внутреннего сгорания – 35 %.
По эффективности преобразования энергии живая клетка превосходит многие технические преобразователи.
Этапы энергетического обмена
Расщепление белков пищи до аминокислот,их всасывание
Транспорт аминокислот в клетки
Кислород
Образование белков организма;
Распад белков и образование энергии
Углекислый газ, вода, мочевина
Выделение в наружную среду
Пища
Расщепление углеводов пищи до глюкозы
Транспорт глюкозы в клетки; образование гликогена в печени
Кислород
Распад глюкозы с образованием энергии
Углекислый газ, вода
Пища
Расщепление жиров пищи до глицерина и жирных кислот;
Образование жировых молекул на ворсинках
Транспорт жировых молекул в клетки
Кислород
Распад жира с образованием энергии
Углекислый газ, вода
III. Закрепление полученных знаний путём решения задач
Практикум:
Задача1. В процессе диссимиляции произошло расщепление 7 моль глюкозы, из которых полному (кислородному) расщеплению подверглось только 2 моль. Определите:
а) сколько молей молочной кислоты и углекислого газа при этом образовано;
б) сколько молей АТФ при этом синтезировано;
в) сколько энергии и в какой форме аккумулировано в этих молекулах АТФ;
г) Сколько молей кислорода израсходовано на окисление образовавшейся при этом молочной кислоты.
Решение.
1) Из 7 моль глюкозы 2 подверглись полному расщеплению, 5 – не полому (7-2=5):
2) составляем уравнение неполного расщепления 5 моль глюкозы; 5C6H12O6 + 5•2H3PO4 + 5•2АДФ = 5•2C3H6O3 + 5•2АТФ + 5•2H2O;
3) составляет суммарное уравнение полного расщепления 2 моль глюкозы: 2С6H12O6 + 2•6O2 +2•38H3PO4 + 2•38АДФ = 2•6CO2+2•38АТФ + 2•6H2O + 2•38H2O;
4) суммируем количество АТФ: (2•38) + (5•2) = 86 моль АТФ; 5) определяем количество энергии в молекулах АТФ: 86•40кДж = 3440 кДж.
Ответ:
а) 10 моль молочной кислоты, 12 моль CO2;
б)86 моль АТФ;
в) 3440 кДж, в форме энергии химической связи макроэргических связей в молекуле АТФ;
г) 12 моль О2
Задача 2. В результате диссимиляции в клетках образовалось 5 моль молочной кислоты и 27 моль углекислого газа. Определите:
а) сколько всего молей глюкозы израсходовано;
б) сколько из них подверглось только неполному и сколько полному расщеплению;
в) сколько АТФ при этом синтезировано и сколько энергии аккумулировано;
г) сколько молей кислорода израсходовано на окисление образовавшейся молочной кислоты.
Ответ:
а) 7 моль;
б) 4,5 моль полному + 2,5 моль неполному;
в) 176 моль АТФ, 7040 кДж;
г) 27
Задача на самостоятельное решение
В процессе гликолиза образовалось 42 молекулы пировиноградной кислоты. Какое количество молекул глюкозы подверглось расщеплению и сколько молекул АТФ образуется при полном окислении?
Дано: 42 ПВК
Найти: кол-во глюкозы, кол-во АТФ при полном окислении.
Процессы окисления веществ в клетках происходят под действием кислорода.
ЛАБОРАТОРНАЯ РАБОТА.
Цель: выяснить роль кислорода в расщеплении веществ.
Энергозатраты организма с задержкой дыхания
Вопросы.
Почему после нагрузки удается задержать дыхание на меньшее время, чем в состоянии покоя?
Какой вывод можно сделать?
Таким образом можно сделать выводы:
1. Синтез АТФ в процессе гликолиза не нуждается в мембранах. Он идёт в пробирке , если имеются все необходимые субстраты и ферменты.
2. Для осуществления кислородного процесса необходимо наличие неповреждённых митохондриальных мембран
3. Расщепление в клетке 1 молекулы глюкозы до СО2 и Н2О обеспечивает синтез 38 молекул АТФ
Закрепление: Проверь себя….
Задание №1. Заполните пропуски в тексте:
Органические вещества образуются в растительных клетках из __________ и ________ в процессе ______________.
Животные получают эти вещества в __________________________.
В клетках гетеротрофных организмов при _______________________ органических веществ их энергия переходит в энергию _______________. При этом гетеротрофные организмы выделяют _____________ и __________ .
Задание №2. Укажите пункт, в котором правильно записан процесс расщепления органических веществ в организме животного:
А) белки —> нуклеотиды —> углекислый газ и вода
Б) жиры —> глицерин + жирные кислоты —> углекислый газ и вода
В) углеводы —> моносахариды —> дисахариды —> углекислый газ и вода
Г) белки —> аминокислоты —> вода и аммиак.
Задание №3. На первом этапе своего расщепления глюкоза:
А) окисляется до углекислого газа и воды
Б) не изменяется
В) подвергается брожению
Г) расщепляется до двух трёхуглеродных молекул.
Задание №4. Окисление ПВК при аэробном дыхании происходит в:
A. хлоропластах
B. цитоплазме
C. матриксе
D. Митохондриях
Задание №5. Ступенчатость окисления глюкозы позволяет:
A. Получить больше энергии
B. Предохранить клетку от перегрева
C. Экономнее расходовать кислород
D. Сократить количество получаемой энергии
Задание №6. Где протекает синтез АТФ:
A. хлоропластах
B. цитоплазме
C. матриксе
D. митохондриях
Задание №7. Анаэробный гликолиз происходит в:
А) клетках мышц при накоплении молочной кислоты
Б) митохондриях при образовании АТФ
В) эритроцитах человека
Г) хлоропластах в световой фазе
Задание №8. Получают энергию за счёт анаэробного гликолиза:
А) камбала
Б) бычий цепень
В) глюкоза
Г) воробей
IV.Рефлексия. Подведение итогов.
1.Какую цель каждый из вас сегодня ставил на начало урока.
2.Какими методами, способами и приемами вы добивались своей цели?
3.Какой основной вид деятельности на уроке вас заинтересовал?
4.Использовали ли вы ранее полученные теоретические знания в ходе исследования?
5.Какие знания и умения, которые вы получили на уроке, потребуются вам в жизни?
V. Домашнее задание (разноуровневое): на выбор учащихся.
Задание 1.
Графический диктант. Правильный ответ + Неправильный ответ —
Белки – основной строительный материал клеток.
В пищеварительном тракте белки расщепляются до глюкозы.
Продукты расщепления белков в клетках выделяются через почки, легкие и кожу.
Углеводы расщепляются до глюкозы.
Сахарный диабет возникает только при избыточном употреблении сладкого.
Животные и растительные жиры взаимно незаменимы.
Глицерин и жирные кислоты всасываются в кровь.
Минеральные соли человек употребляет в основном с растительной пищей.
Ожирение вызывается неумеренным употреблением не только жиров и углеводов.
Задание 2
Ниже перечислены процессы, протекающие в клетках организмов:
испарение воды;гликолиз;
расщепление жиров;
биосинтез белков;
фотосинтез;
биосинтез углеводов;
расщепление полисахаридов;
брожение;
дыхание;
биосинтез жиров.
Впишите номера, которыми они обозначены, в соответствии с принадлежностью их ассимиляции и диссимиляции.
Задание 3
Написать рассказ: «Солнце – главный источник энергии».
Тема 3.2. Обмен веществ и превращение энергии. Энергетический обмен.
1. Дайте определения понятий.
Метаболизм – набор химических реакций, которые возникают в живом организме для поддержания жизни.
Энергетический обмен – процесс метаболического распада, разложения на более простые вещества или окисления какого-либо вещества, обычно протекающий с высвобождением энергии в виде тепла и в виде АТФ.
Пластический обмен – совокупность всех процессов биосинтеза, протекающих в живых организмах.
2. Заполните таблицу.
3. Изобразите схематично молекулу АТФ. Обозначьте ее части. Укажите расположение макроэргических связей. Напишите полное название этой молекулы.
АТФ – аденозинтрифосфорная кислота
4. К какому классу органических веществ относится АТФ? Почему вы сделали такой вывод?
Нуклеотид, так как состоит из аденина, рибозы и трех остатков фосфорной кислоты.
5. Пользуясь материалом § 3.2, заполните таблицу.
6. Какова биологическая роль ступенчатого характера энергетического обмена?
Постепенное выделение энергии, идущее в ходе энергетического обмена, позволяет более рационально использовать и запасать энергию. При разовом выделении такого числа энергии большая ее часть просто не успела бы соединиться с АДФ и выделилась бы как тепло, что означает большие потери для организма.
7. Объясните, почему кислород необходим большинству современных организмов. В результате какого процесса в клетках образуется углекислый газ?
Кислород необходим для дыхания. При наличии кислорода органические вещества при дыхании полностью окисляются до углекислого газа и воды.
8. Как повлияло накопление в атмосфере Земли кислорода на степень интенсивности процессов жизнедеятельности обитателей нашей планеты?
Кислород оказывает глубокое влияние на организм в целом, повышая общую энергию жизнедеятельности обитателей нашей планеты. Возникли и эволюционировали новые организмы.
9. Вставьте пропущенные слова.
Реакции пластического обмена идут с поглощением энергии.
Реакции энергетического обмена идут с выделением энергии.
Подготовительный этап энергетического обмена осуществляется в ЖКТ и лизосомах
клетки.
Гликолиз протекает в цитоплазме.
Во время подготовительного этапа белки под действием пищеварительных ферментов превращаются в аминокислоты.
10. Выберите правильный ответ.
Тест 1.
Какая из аббревиатур обозначает носителя энергии в живой клетке?
3) АТФ;
Тест 2.
На подготовительном этапе энергетического обмена белки распадаются до:
2) аминокислот;
Тест 3.
В результате бескислородного окисления в клетках животных при недостатке кислорода образуется:
3) молочная кислота;
Тест 4.
Энергия, которая выделяется в реакциях подготовительного этапа энергетического обмена:
2) рассеивается в виде тепла;
Тест 5.
Гликолиз обеспечивают ферменты:
3) цитоплазмы;
Тест 6.
При полном окислении четырех молекул глюкозы образуется:
4) 152 молекулы АТФ.
Тест 7.
Для наиболее быстрого восстановления работоспособности при усталости в период подготовки к экзамену лучше всего съесть:
3) кусок сахара;
11. Составьте синквейн к термину «метаболизм».
Метаболизм
Пластический и энергетический.
Синтезирует, разрушает, превращает.
Набор химических реакций в живом организме для поддержания жизни.
Обмен веществ.
12. Скорость обмена веществ непостоянна. Укажите некоторые внешние и внутренние причины, которые, по вашему мнению, способны изменять скорость обмена веществ.
Внешние – температура окружающей среды, физические нагрузки, масса тела.
Внутренние – уровень гормонов в крови, состояние нервной системы (угнетение или возбуждение).
13. Вы знаете, что существуют аэробные и анаэробные организмы. А кто такие факультативные анаэробы?
Это организмы, энергетические циклы которых проходят по анаэробному пути, но способные существовать при доступе кислорода, в отличие от облигатных анаэробов, для которых кислород губителен.
14. Объясните происхождение и общее значение слова (термина), опираясь на значение корней, его составляющих.
15. Выберите термин и объясните, насколько его современное значение соответствует первоначальному значению его корней.
Выбранный термин – гликолиз.
Соответствие: термин соответствует, но дополнен. Современное определение гликолиза, это не просто «расщепление сладкого», а процесс окисления глюкозы, при котором из одной ее молекулы образуются две молекулы ПВК, осуществляемый последовательно за несколько ферментативных реакций и сопровождающийся запасанием энергии в форме АТФ и NADH.
16. Сформулируйте и запишите основные идеи § 3.2.
Для любого организма характерен обмен веществ – набор хим. реакций для поддержания жизни. Энергетический обмен – процесс разложения на более простые вещества, протекающий с высвобождением энергии в виде тепла и в виде АТФ. Пластический обмен – совокупность всех процессов биосинтеза, протекающих в живых организмах.
Молекула АТФ – универсальный поставщик энергии в клетках.
Энергетический обмен протекает в 3 стадии: подготовительный этап (образуется глюкоза и тепло), гликолиз (образуется ПВК, 2 молекулы АТФ и тепло) и кислородный, или клеточное дыхание, (образуется 36 молекул АТФ и углекислый газ).
Этапы энергетического обмена
☰
Энергетический обмен — это по-этапный распад сложных органических соединений, протекающий с выделением энергии, которая запасается в макроэргических связях молекул АТФ и используется потом в процессе жизнедеятельности клетки, в том числе на биосинтез, т.е. пластический обмен.
В аэробных организмах выделяют три последовательных этапа энергетического обмена:
- Подготовительный — расщепление биополимеров до мономеров.
- Бескислородный — гликолиз — расщепление глюкозы до пировиноградной кислоты.
- Кислородный — расщепление пировиноградной кислоты до углекислого газа и воды.
Подготовительный этап
На подготовительном этапе энергетического обмена происходит расщепление поступивших с пищей органических соединений на более простые, обычно мономеры. Так углеводы расщепляются до сахаров, в том числе глюкозы; белки — до аминокислот; жиры — до глицерина и жирных кислот.
Хотя при этом выделяется энергия, она не запасается в АТФ и, следовательно, не может быть использована впоследствии. Энергия рассеивается в виде тепла.
Расщепление полимеров у многоклеточных сложноорганизованных животных протекает в пищеварительном тракте под действием выделяющихся сюда железами ферментов. Затем образовавшиеся мономеры всасываются в кровь в основном через кишечник. Уже кровью питательные вещества разносятся по клеткам.
При этом не все вещества разлагаются до мономеров в пищеварительной системе. Расщепление многих происходит непосредственно в клетках, в их лизосомах. У одноклеточных организмов поглощенные вещества попадают в пищеварительные вакуоли, где и перевариваются.
Образовавшиеся мономеры могут использоваться как для энергетического, так и пластического обмена. В первом случае они расщепляются, во-втором – из них синтезируются компоненты самих клеток.
Бескислородный этап энергетического обмена
Бескислородный этап протекает в цитоплазме клеток и в случае аэробных организмов включает только гликолиз — ферментативное многоступенчатое окисление глюкозы и ее расщепление до пировиноградной кислоты, которую также называют пируватом.
Молекула глюкозы включает шесть атомов углерода. При гликолизе она расщепляется до двух молекул пирувата, который включает три атома углерода. При этом отщепляется часть атомов водорода, которые передаются на кофермент НАД, который, в свою очередь, потом будет участвовать в кислородном этапе.
Часть выделяющейся при гликолизе энергии запасается в молекулах АТФ. На одну молекулу глюкозы синтезируется всего две молекулы АТФ.
Энергия, оставшаяся в пирувате, запасенная в НАД, у аэробов далее будет извлечена на следующем этапе энергетического обмена.
В анаэробных условиях, когда кислородный этап клеточного дыхания отсутствует, пируват «обезвреживается» в молочную кислоту или подвергается брожению. При этом энергия не запасается. Таким образом, здесь полезный энергетический выход обеспечивается только малоэффектвным гликолизом.
Кислородный этап
Кислородный этап протекает в митохондриях. В нем выделяют два подэтапа: цикл Кребса и окислительное фосфорилирование. Поступающий в клетки кислород используется только на втором. В цикле Кребса происходит образование и выделение углекислого газа.
Цикл Кребса протекает в матриксе митохондрий, осуществляется множеством ферментов. В него поступает не сама молекула пировиноградной кислоты (или жирной кислоты, аминокислоты), а отделившаяся от нее с помощью кофермента-А ацетильная группа, включающая два атома углерода бывшего пирувата. За многоступенчатый цикл Кребса происходит расщепление ацетильной группы до двух молекул CO2 и атомов водорода. Водород соединяется с НАД и ФАД. Также происходит синтез молекулы ГДФ, приводящей к синтезу потом АТФ.
На одну молекулу глюкозы, из которой образуется два пирувата, приходится два цикла Кребса. Таким образом, образуется две молекулы АТФ. Если бы энергетический обмен заканчивался здесь, то суммарно расщепление молекулы глюкозы давало бы 4 молекулы АТФ (две от гликолиза).
Окислительное фосфорилирование протекает на кристах – выростах внутренней мембраны митохондрий. Его обеспечивает конвейер ферментов и коферментов, образующий так называемую дыхательную цепь, заканчивающуюся ферментом АТФ-синтетазой.
По дыхательной цепи происходит передача водорода и электронов, поступивших в нее от коферментов НАД и ФАД. Передача осуществляется таким образом, что протоны водорода накапливаются с внешней стороны внутренней мембраны митохондрий, а последние ферменты в цепи передают только электроны.
В конечном итоге электроны передаются молекулам кислорода, находящимся с внутренней стороны мембраны, в результате чего они заряжаются отрицательно. Возникает критический уровень градиента электрического потенциала, приводящий к перемещению протонов через каналы АТФ-синтетазы. Энергия движения протонов водорода используется для синтеза молекул АТФ, а сами протоны соединяются с анионами кислорода с образованием молекул воды.
Энергетический выход функционирования дыхательной цепи, выраженный в молекулах АТФ, велик и суммарно составляет от 32 до 34 молекул АТФ на одну исходную молекулу глюкозы.
Общий обзор основных метаболических путей
Метаболизм — это набор химических реакций, которые происходят в клетке, которые позволяют ей продолжать жить, расти и делиться. Метаболические процессы обычно классифицируются как:
глюконеогенез — синтез глюкозы из более мелких перкурсоров, который будет использоваться мозгом.Щелкните изображение, чтобы получить информацию о каждом пути
Метаболические пути взаимодействуют сложным образом, чтобы обеспечить адекватную регуляцию.Это взаимодействие включает ферментативный контроль каждого пути, метаболического профиля каждого органа и гормонального контроля.
Ферментативный контроль метаболических путей
Регулирование гликолиза
Метаболический поток при гликолизе можно регулировать в трех ключевых точках:
- гексокиназа: ингибируется глюкозой-6-P (ингибирование продукта)
- фосфофруктокиназа : ингибируется АТФ и цитратом (что сигнализирует об изобилии промежуточных продуктов цикла лимонной кислоты).Он также ингибируется H + , что становится важным при анаэробиозе (молочная ферментация производит молочную кислоту, что приводит к снижению pH). Вероятно, этот механизм не позволяет клетке использовать весь свой запас АТФ в реакции фосфофрутокиназы, что предотвратит активацию глюкозы гексокиназой. Он стимулируется его субстратом (фруктозо-6-фосфат), АМФ и АДФ (которые сигнализируют об отсутствии доступной энергии) и т. Д.
- пируваткиназа : ингибируется АТФ, аланином, свободными жирными кислотами и ацетил-КоА.Активируется фруктозо-1,6-бисфосфатом и AMP
Регуляция глюконеогенеза
Поток регулируется специфическими реакциями глюконеогенеза. Пируваткарбоксилаза активируется ацетил-КоА, что сигнализирует об изобилии промежуточных продуктов цикла лимонной кислоты, , то есть , о снижении потребности в глюкозе.
Регулирование цикла лимонной кислоты
Цикл лимонной кислоты регулируется в основном доступностью субстрата, ингибированием продукта и некоторыми промежуточными продуктами цикла.
- пируватдегидрогеназа: ингибируется ее продуктами, ацетил-КоА и НАДН
- цитратсинтаза : ингибируется ее продуктом, цитратом. Он также ингибируется НАДН и сукцинил-КоА (которые сигнализируют об изобилии промежуточных продуктов цикла лимонной кислоты).
- изоцитратдегидрогеназа и α-кетоглутарат дегидрогеназа : как и цитрат-синтаза, они ингибируются НАДН и сукцинил-КоА.Изоцитратдегидрогеназа также ингибируется АТФ и стимулируется АДФ. Все вышеупомянутые дегидрогеназы стимулируются Ca 2+ . Это имеет смысл в мышцах, поскольку высвобождение Ca 2+ из саркоплазматической сети вызывает сокращение мышц, что требует большого количества энергии. Таким образом, тот же «второй посланник» активирует энергозатратную задачу и — средства для производства этой энергии.
Регулирование цикла карбамида
Карбамоилфосфатсинтетаза стимулируется N-ацетилглутамином, который сигнализирует о наличии большого количества азота в организме.
Регуляция обмена гликогена
Печень содержит гексокиназу ( гексокиназа D или глюкокиназа ) с низким сродством к глюкозе, которая (в отличие от «обычной» гексокиназы) не подлежит ингибированию продуктом. Следовательно, глюкоза фосфрилируется в печени только тогда, когда она присутствует в очень высоких концентрациях (, то есть после еды). Таким образом, печень не будет конкурировать с другими тканями за глюкозу, когда этого сахара недостаточно, а будет накапливать высокие уровни глюкозы для синтеза гликогена сразу после еды.
Регуляция обмена жирных кислот
Движение ацил-КоА в митохондрии является решающим фактором регуляции. Малонил-КоА (который присутствует в цитоплазме в больших количествах, когда метаболическое топливо в изобилии) ингибирует карнитин-ацилтрансферазу, тем самым предотвращая проникновение ацил-КоА в митохондрии. Кроме того, 3-гидроксиацил-КоА-дегидрогеназа ингибируется НАДН, а тиолаза ингибируется ацетил-КоА, так что жирные кислоты не будут окисляться, когда в клетке имеется много энергоемких субстратов.
Регуляция пентозофосфатного пути
Метаболический поток через пентозофосфатный путь контролируется активностью глюкозо-6-фосфатдегидрогеназы, которая контролируется доступностью NADP + .
Мозг
Обычно нейроны используют только глюкозу в качестве источника энергии. Поскольку мозг хранит лишь очень небольшое количество гликогена, ему необходимо постоянное поступление глюкозы. Во время длительного голодания он становится способен окислять кетоновые тела.
Печень
Поддержание достаточно постоянной концентрации глюкозы в крови — одна из основных функций печени. Это достигается за счет глюконеогенеза, синтеза и распада гликогена. Когда ацетил-КоА в избытке, он синтезирует кетоновые тела. Это также место синтеза мочевины.
Он синтезирует жирные кислоты и хранит их в виде триацилглицеринов. Глюкагон активирует гормоночувствительную липазу, которая гидролизует триацилглицерины с образованием глицерина и жирных кислот.Затем они попадают в кровоток в виде липопротеинов.
Мышцы используют глюкозу, жирные кислоты, кетоновые тела и аминокислоты в качестве источника энергии. Он также содержит запас креатинфосфата, соединения с высоким потенциалом переноса фосфата, которое способно фосфорилировать АДФ до АТФ, тем самым производя энергию без использования глюкозы. Количество креатина в мышцах достаточно, чтобы выдержать 3-4 с нагрузки. По истечении этого периода мышца использует гликолиз, сначала анаэробно (так как он намного быстрее, чем цикл лимонной кислоты), а позже (когда повышенная кислотность замедляет фосфофрутокиназу настолько, чтобы цикл лимонной кислоты стал неограничивающим) в аэробных условиях. .
Почки
Он может осуществлять глюконеогенез и выделять глюкозу в кровоток. Он также отвечает за выведение мочевины, электролитов и т. Д. Метаболический ацидоз может быть усилен действием цикла мочевины, поскольку синтез мочевины (который происходит в печени) использует HCO 3 — , таким образом дальнейшее снижение pH крови. В этих условиях азот может быть устранен совместным действием почек и печени: избыток азота сначала включается в глутамин с помощью глутаминсинтетазы.Затем глутаминаза почек расщепляет глутамин с образованием глутамата e NH 3 , который немедленно выводится почками. Этот процесс позволяет вывести азот, не влияя на уровень бикарбоната в крови.
| Биохимия,
Дональд Воет и Джудит Воет Отличный текст. В нем представлена биохимия с частыми ссылками на органическую химию и биохимическую логику. Рекомендуется для студентов, изучающих биохимию, химию и фармацевтику. | Биохимия,
Stryer Широко используемый классический текст, часто обновляемый и переизданный. | ||
| Учебник
биохимии с клиническими корреляциями, Томас Девлин Настоятельно рекомендуется студентам сестринского дела, медицины, стоматологии и т. д. Множество примеров применения биохимических знаний в клинических случаях. | Принципы
of Biochemistry, Lehninger Широко используемый классический текст, часто обновляемый и переизданный. |
24,5 Метаболические состояния организма — анатомия и физиология
Цели обучения
К концу этого раздела вы сможете:
- Опишите, что определяет каждое из трех метаболических состояний
- Опишите процессы, происходящие во время абсорбционного состояния метаболизма
- Опишите процессы, происходящие во время постабсорбтивного метаболизма
- Объясните, как организм перерабатывает глюкозу, когда ему не хватает топлива
Вы едите периодически в течение дня; однако ваши органы, особенно мозг, нуждаются в постоянном поступлении глюкозы.Как организм удовлетворяет эту постоянную потребность в энергии? Ваше тело обрабатывает пищу, которую вы едите, для немедленного использования и, что немаловажно, для сохранения энергии для дальнейшего использования. Если бы не существовало метода хранения избыточной энергии, вам пришлось бы постоянно есть, чтобы удовлетворять потребности в энергии. Существуют особые механизмы, облегчающие накопление энергии и делающие накопленную энергию доступной во время голодания и голодания.
Состояние абсорбции
Состояние всасывания, или состояние сытости, возникает после еды, когда ваше тело переваривает пищу и поглощает питательные вещества (анаболизм превышает катаболизм).Пищеварение начинается в тот момент, когда вы кладете пищу в рот, так как пища распадается на составные части, которые всасываются через кишечник. Переваривание углеводов начинается во рту, тогда как переваривание белков и жиров начинается в желудке и тонком кишечнике. Составные части этих углеводов, жиров и белков транспортируются через стенку кишечника и попадают в кровоток (сахара и аминокислоты) или в лимфатическую систему (жиры). Из кишечника эти системы транспортируют их в печень, жировую ткань или мышечные клетки, которые будут обрабатывать, использовать или накапливать энергию.
В зависимости от количества и типов потребляемых питательных веществ состояние всасывания может сохраняться до 4 часов. Прием пищи и повышение концентрации глюкозы в кровотоке стимулируют бета-клетки поджелудочной железы выделять инсулин в кровоток, где он инициирует абсорбцию глюкозы в крови гепатоцитами печени, а также жировыми и мышечными клетками. Попав внутрь этих клеток, глюкоза немедленно превращается в глюкозо-6-фосфат. Таким образом устанавливается градиент концентрации там, где уровень глюкозы в крови выше, чем в клетках.Это позволяет глюкозе продолжать перемещаться из крови в клетки, где она необходима. Инсулин также стимулирует хранение глюкозы в виде гликогена в клетках печени и мышц, где ее можно использовать для будущих энергетических потребностей организма. Инсулин также способствует синтезу белка в мышцах. Как вы увидите, мышечный белок может катаболизироваться и использоваться в качестве топлива во время голодания.
Если энергия поступает вскоре после еды, пищевые жиры и сахара, которые были только что проглочены, будут переработаны и немедленно использованы для получения энергии.В противном случае избыток глюкозы откладывается в виде гликогена в клетках печени и мышц или в виде жира в жировой ткани; избыток пищевых жиров также сохраняется в виде триглицеридов в жировой ткани.
На рисунке 24.21 представлены метаболические процессы, происходящие в организме в состоянии абсорбции.
Рисунок 24.21 Состояние абсорбции В состоянии абсорбции организм переваривает пищу и поглощает питательные вещества.
Состояние после погружения
Состояние постабсорбции или состояние голодания возникает, когда пища переваривается, всасывается и хранится.Обычно вы голодаете всю ночь, но пропуск приема пищи в течение дня также ставит ваше тело в состояние после абсорбции. В этом состоянии организм изначально должен полагаться на запасенный гликоген. Уровень глюкозы в крови начинает падать, поскольку она всасывается и используется клетками. В ответ на снижение глюкозы падает и уровень инсулина. Запасы гликогена и триглицеридов замедляются. Однако из-за требований тканей и органов уровень глюкозы в крови должен поддерживаться в нормальном диапазоне 80–120 мг / дл.В ответ на падение концентрации глюкозы в крови альфа-клетки поджелудочной железы высвобождают гормон глюкагон. Глюкагон действует на клетки печени, где он подавляет синтез гликогена и стимулирует распад накопленного гликогена обратно на глюкозу. Эта глюкоза высвобождается из печени для использования периферическими тканями и мозгом. В результате уровень глюкозы в крови начинает повышаться. Глюконеогенез также начнется в печени, чтобы заменить глюкозу, которая была использована периферическими тканями.
После приема пищи жиры и белки перерабатываются, как описано ранее; однако обработка глюкозы немного меняется. Периферические ткани преимущественно поглощают глюкозу. Печень, которая обычно поглощает и перерабатывает глюкозу, не будет этого делать после длительного голодания. Глюконеогенез, который продолжается в печени, будет продолжаться после голодания, чтобы восполнить запасы гликогена, которые были истощены в печени. После того, как эти запасы пополнятся, избыток глюкозы, усваиваемой печенью, будет преобразован в триглицериды и жирные кислоты для длительного хранения.На рисунке 24.22 представлены метаболические процессы, происходящие в организме во время постабсорбтивного состояния.
Рис. 24.22 Постабсорбционное состояние В постабсорбционном состоянии тело должно полагаться на запасенный гликоген для получения энергии.
Голод
Когда тело лишено питания в течение длительного периода времени, оно переходит в «режим выживания». Первоочередной задачей выживания является обеспечение мозга достаточным количеством глюкозы или топлива. Второй приоритет — сохранение аминокислот для белков.Таким образом, организм использует кетоны для удовлетворения энергетических потребностей мозга и других глюкозозависимых органов, а также для поддержания белков в клетках (см. Рис. 24.2). Поскольку во время голодания уровень глюкозы очень низкий, гликолиз отключится в клетках, которые могут использовать альтернативные виды топлива. Например, мышцы переключатся с использования глюкозы на жирные кислоты в качестве топлива. Как объяснялось ранее, жирные кислоты могут быть преобразованы в ацетил-КоА и переработаны в цикле Кребса с образованием АТФ. Пируват, лактат и аланин из мышечных клеток не превращаются в ацетил-КоА и не используются в цикле Кребса, а экспортируются в печень для использования в синтезе глюкозы.Поскольку голодание продолжается и требуется больше глюкозы, глицерин из жирных кислот может высвобождаться и использоваться в качестве источника глюконеогенеза.
После нескольких дней голодания кетоновые тела становятся основным источником топлива для сердца и других органов. По мере того как голод продолжается, запасы жирных кислот и триглицеридов используются для создания кетонов для организма. Это предотвращает продолжающийся распад белков, которые служат источниками углерода для глюконеогенеза. Когда эти запасы полностью истощаются, белки из мышц высвобождаются и расщепляются для синтеза глюкозы.Общая выживаемость зависит от количества жира и белка, хранящегося в организме.
Идентификация основных метаболических процессов в масштабе генома для нацеливания на стадию плазмодия в печени
Основные моменты
- •
1342 штрих-кода Нокаут-мутанты P. berghei (KO) проанализированы на предмет специфичных для стадии фенотипов
4- •
- • Метаболические модели, специфичные для каждой стадии жизни, показывают перепрограммирование клеточной функции
- •
- • Метаболические модели, специфичные для каждой стадии жизни, показывают перепрограммирование клеточной функции
Высокое соответствие между моделями метаболизма на стадии кровь / печень и данными генетического скрининга
- •
Выявлены основные метаболические пути развития паразитов и их механическое происхождение
Резюме
Функции гена Plasmodium на стадиях комара и печени остаются плохо изученными из-за ограничений в производительности фенотипирования на этих стадиях.Чтобы восполнить этот пробел, мы проследили более 1300 мутантов P. berghei со штрих-кодом на протяжении всего жизненного цикла. Мы обнаружили 461 ген, необходимый для эффективной передачи паразитов комарам через печень и обратно в кровоток мышей. Мы анализируем экран в контексте геномных, транскриптомных и метаболомных данных, создавая термодинамическую модель метаболизма P. berghei на стадии печени, которая показывает значительное перепрограммирование метаболизма паразитов для достижения быстрого роста в печени.Мы выделяем семь метаболических подсистем, которые становятся важными на стадиях печени по сравнению с стадиями бесполой крови: синтез и удлинение жирных кислот типа II (FAE), трикарбоновая кислота, аминосахар, гем, липоат и метаболизм шикимата. Выбранные прогнозы модели индивидуально проверяются на единичных мутантах, чтобы обеспечить будущие цели для разработки лекарств.
Ключевые слова
малярия
Plasmodium berghei
метаболическая сеть
биосинтез жирных кислот
удлинение жирных кислот
аминосахарный биосинтез
000 скрининг генома
000 стадия метаболического генома
модель генома
метаболическая модель
Рекомендуемые статьи Цитирующие статьи (0)
Просмотр аннотации© 2019 Авторы.Опубликовано Elsevier Inc.
Рекомендуемые статьи
Цитирующие статьи
Метаболические особенности и регуляция цикла заживления — новая модель патогенеза и лечения хронических заболеваний
Основные моменты для митохондрий
- •
Четыре этапа заживления цикл определяется с точки зрения биоэнергетики и метаболизма.
- •
Продолжение цикла заживления контролируется метабокинами и митохондриями.
- •
Описаны три состояния дифференцировки поляризованных митохондрий; противовоспалительный M2, провоспалительный M1 и незафиксированный M0.
- •
Патофизиология хронического заболевания изменилась в результате нарушений в передаче сигналов метабокина и митохондрий.
- •
Когда нормальные стадии реакции клетки на опасность (CDR) сохраняются ненормально, цикл заживления блокируется и возникает хроническое заболевание.
Abstract
Без исцеления многоклеточная жизнь на Земле не существовала бы. Без исцеления одна травма предрасполагает к другой, приводя к инвалидности, хроническим заболеваниям, ускоренному старению и смерти. Более 60% взрослых и 30% детей и подростков в Соединенных Штатах сейчас живут с хроническими заболеваниями. Достижения в области масс-спектрометрии и метаболомики дали ученым новые возможности для изучения здоровья и болезней. Это исследование определяет цикл исцеления в терминах метаболизма и переосмысливает патофизиологию хронического заболевания как результат нарушений метаболической сигнализации, которые блокируют заживление и вызывают аномальное сохранение нормальных стадий реакции клетки на опасность (CDR).После травмы активное прохождение стадий заживления обусловлено последовательными изменениями в клеточной биоэнергетике и расположением кислородного и углеродного скелетов, используемых для топлива, передачи сигналов, защиты, ремонта и восстановления. > 100 хронических заболеваний можно разделить на три устойчивых стадии CDR. Представлены сто два нацеленных хемосенсорных связанных с G-белком и ионотропных рецептора, которые регулируют CDR и заживление. Метабокины — это сигнальные молекулы, полученные в результате метаболизма, которые регулируют эти рецепторы.Переосмысление патогенеза хронического заболевания таким образом, как системной проблемы, которая поддерживает заболеваний, вместо того, чтобы сосредоточиться на удаленных триггерах, которые причинили первоначальное повреждение, позволяет новым исследованиям сосредоточиться на новых сигнальных методах лечения, чтобы разблокировать цикл исцеления и восстановить здоровье, когда другие подходы потерпели неудачу.
Ключевые слова
Реакция клетки на опасность
Цикл исцеления
Митохондриальный нексус
Метаболическая зависимость
Метаболическая память
Пуринергическая передача сигналов
Метабокины
00020002000 Митохондриальная терапия
000 Митохондрия000 Митохондриальная терапия000Аллостаз
Аллостатическая нагрузка
Комплексная реакция на стресс
Аббревиатуры
TOGLEsтранспортеры Опсины G белковые рецепторы, лиганды и эффекторы
ASDрасстройство аутистического спектра
CFS000 синдром хронической усталости
000 DAMPs синдром
000 молекулярных повреждений
000 DAMPs реактивные метаболиты, связанные с повреждением
PTSDпосттравматическое стрессовое расстройство
M2противовоспалительная митохондриальная поляризация
Рекомендуемые статьиЦитирующие статьи (0)
Просмотреть аннотацию© 2018 Автор.Опубликовано Elsevier B.V.
Рекомендуемые статьи
Цитирование статей
Уровни белка I, связывающего инсулиноподобный фактор роста, тесно связаны с чувствительностью к инсулину и ожирением у детей раннего полового созревания1 | Журнал клинической эндокринологии и метаболизма
Было показано, что в условиях, связанных с инсулинорезистентностью, уровни белка-I, связывающего инсулино-подобный фактор роста (IGFBP-I), обратно коррелируют с уровнями инсулина. Половое созревание связано с инсулинорезистентностью и, таким образом, представляет собой модель для сравнения взаимосвязи IGFBP-I как с уровнями инсулина, так и с показателями чувствительности к инсулину.В исследуемую популяцию вошли 104 здоровых ребенка пубертатного возраста в возрасте 9,8–14,6 лет. У каждого испытуемого оценивалась его / ее чувствительность к инсулину (Si) с помощью модифицированной минимальной модели Бергмана, которая использует часто отбираемый внутривенный тест толерантности к глюкозе. Результаты показали, что уровни IGFBP-I были значительно выше у мальчиков, чем у девочек пубертатного возраста ( P <0,01). Наблюдалась сильная положительная корреляция между уровнями IGFBP-I и Si (r = 0,65, P <0,0001) и более слабая отрицательная корреляция с уровнями инсулина натощак (r = -0.38, P <0,0001). Также была обнаружена обратная зависимость между уровнями IGFBP-I и индексом массы тела (r = -0,46, P <0,0001) и уровнями IGF-I (только для девочек, r = -0,41, P <0,003). Следовательно, чувствительность к инсулину, ожирение и IGF-I являются важными предикторами уровней IGFBP-I у детей полового созревания. Возможно, что инсулино-опосредованное подавление IGFBP-I у детей с ожирением может повысить уровни свободного IGF-I и, таким образом, способствовать соматическому росту. Тот же механизм может действовать у детей полового созревания, у которых инсулинорезистентность и ускорение роста возникают одновременно.
Метаболические и митогенные эффекты инсулиноподобных факторов роста (IGF-I и IGF-II) модулируются семейством из шести IGF-связывающих белков (IGFBP) (1). Эти связывающие белки, хотя структурно схожи, обладают уникальными биологическими свойствами и регулируются независимо. В то время как IGFBP-3, основная циркулирующая форма, зависит от GH (2), IGFBP-I не зависит от GH и в первую очередь зависит от инсулина (3, 4). Производство IGFBP-I в печени ингибируется инсулином (5). Было показано, что уровни циркулирующего IGFBP-I обратно коррелируют с уровнями инсулина в плазме; таким образом, повышенные уровни IGFBP-I наблюдаются при состояниях с низким уровнем инсулина, таких как голодание, физические упражнения и инсулинозависимый сахарный диабет (6–8).Аналогичным образом, при состояниях с высоким содержанием инсулина, таких как гиперинсулинемические зажимы, инсулиномы и постпрандиальные состояния, уровни IGFBP-I снижаются (9). Считается, что IGFBP-I ингибирует действие IGF-I, предотвращая связывание IGF-I с рецепторами на клеточных мембранах (10). Следовательно, в состоянии сытости, когда секреция инсулина высока, подавленные уровни IGFBP-I могут усиливать инсулиноподобные действия свободного IGF, таким образом связывая доступность и действие IGF с резкими изменениями статуса питания.
Было продемонстрировано, что состояния, сопровождающиеся инсулинорезистентностью, включая ожирение, синдром поликистозных яичников и инсулиннезависимый сахарный диабет, связаны со снижением уровня IGFBP-I (11, 12).Было обнаружено, что у детей уровни IGFBP-I в сыворотке обратно коррелируют со стадией полового созревания (13), что ранее объяснялось повышением уровня инсулина, сопровождающим половое созревание (14). Уровни инсулина высоки в период полового созревания в ответ на физиологическое снижение чувствительности к инсулину, которое происходит в это время (15, 16). Следовательно, половое созревание представляет собой модель для сравнения взаимосвязи IGFBP-I как с уровнями инсулина, так и с показателями чувствительности к инсулину. В этом исследовании мы изучили эти отношения на большой группе мальчиков и девочек пубертатного возраста.Кроме того, мы проанализировали влияние других переменных, таких как пол, ожирение и уровни IGF-I, на концентрации IGFBP-I.
Объекты и методы
Субъекты
Исследуемая популяция состояла из 104 здоровых детей без диабета в возрасте от 9,8 до 14,6 лет. Эти субъекты описаны в предыдущем исследовании чувствительности к инсулину в период полового созревания (16). Пубертатное развитие оценивали по критериям Маршалла и Таннера по развитию волос на лобке, груди или гениталий (17).Характеристики испытуемых представлены в таблице 1. Сорок девять мальчиков были европеоидной расы, двое афроамериканцев и двое латиноамериканцев. Сорок девять девочек были европеоидной расы, одна афроамериканка и одна латиноамериканка. Протокол исследования был одобрен Комиссией по множественному анализу учреждений штата Колорадо, и информированное согласие было получено от участвующих субъектов и их родителей.
Таблица 1.Характеристика 104 субъектов
| . | Мальчики . | Девочки . | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Таннер 2 (n = 32) . | Таннер 3 (n = 21) . | Таннер 2 (n = 25) . | Таннер 3 (n = 26) . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Возраст (лет) | 12,6 ± 0,9 | 13,1 ± 0,7 | 11,3 ± 0,9 | 12,3 ± 0,9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рост (см) | 154.7 ± 5,9 | 162,9 ± 6,1 | 147,3 ± 7,7 | 156,4 ± 7,2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Масса, кг | 53,4 ± 14,9 | 52,5 ± 8,9 | 41,7 ± 9,2 | 23
Характеристики 104 субъектов
Часто отбираемый внутривенный тест толерантности к глюкозеИндекс чувствительности к инсулину (Si) был рассчитан на основе часто отбираемого внутривенного теста на толерантность к глюкозе с использованием модифицированной минимальной модели Бергмана (18, 19). Все пациенты были госпитализированы в Педиатрический центр клинических исследований в Детской больнице в Денвере после 10-часового ночного голодания. Катетер для в / в вводили в каждую руку.Через 30 минут были взяты исходные образцы крови, включая измерения уровней IGFBP-I и инсулина. В нулевое время вливали 25% декстрозу (0,3 г / кг) в течение 60 секунд. Через двадцать минут после инфузии декстрозы болюс толбутамида (300 мг / 1,73 м 2 ) был введен в течение 60 секунд. Дополнительные образцы крови были взяты из противоположной руки через 2, 4, 8, 19, 22, 25, 30, 35, 40, 50, 70, 90 и 180 минут. Каждый образец помещали в охлажденную гепаринизированную пробирку для измерения глюкозы и инсулина. Антропометрические измеренияРост и вес измерялись у испытуемых босиком и в больничном халате. Рост измерялся ростомером Harpendon. Был рассчитан индекс массы тела (ИМТ) (вес в килограммах, деленный на квадрат роста в метрах) (20). Подводное взвешиваниеКаждый субъект прошел гидростатическое определение плотности тела, которое позволяет рассчитать процентное содержание жира в организме.Эта процедура была описана ранее (16). Процент жира в организме оценивался по плотности тела с использованием модифицированного уравнения Siri, как описано Ломаном (21). Это модифицированное уравнение учитывает гендерные и возрастные различия в плотности безжировой массы. АнализыСразу после сбора были проведены измерения глюкозы в плазме с помощью метода глюкозооксидазы (анализатор глюкозы STAT, модель 2300, Yellow Springs Instrument Co., Yellow Springs, OH). Инсулин определяли методом двойного РИА антител (22).Коэффициенты вариации инсулина внутри и между исследованиями составляли 5,8–6,4% и 5,4–5,8% соответственно. Уровни IGFBP-I оценивали с помощью иммунорадиометрической пробирки с покрытием, предоставленной лабораторией диагностических систем (Вебстер, Техас). Сыворотка была соответствующим образом разбавлена для измерения в пределах линейного диапазона анализа, который составляет 0,15–20 нг / мл. Тринадцать из 104 субъектов имели значения IGFBP-I ниже, чем чувствительность анализа 0,15. Для статистического анализа эти значения были приняты за 0.075. Вариация внутри и между исследованиями составляла ≤ 5%. Уровни IGF-I в сыворотке также измеряли методом двойного анализа антител ( 125 I RIA Kit, INCSTAR Corp., Stillwater, MN) с коэффициентами вариации внутри и между анализами 9,6% и 7,7% соответственно. Концентрации эстрадиола и тестостерона в сыворотке также определяли с использованием наборов RIA (Coat-A-Count Estradiol и Coat-A-Count Total Testosterone, Diagnostic Products Corp., Лос-Анджелес, Калифорния). Чувствительность анализа для эстрадиола составила 29 пмоль / л, а для тестостерона — 0.21 нмоль / л. РасчетыВсе определения Si были рассчитаны на основе данных глюкозы и инсулина из часто отбираемого внутривенного теста на толерантность к глюкозе с помощью модифицированной программы минимальных моделей Бергмана (18). В этом методе математические модели кинетики глюкозы и инсулина реализованы на компьютере и используются для анализа динамики глюкозы и инсулина в плазме после внутривенной инъекции глюкозы и толбутамида. Статистический анализВсе статистические анализы были выполнены с использованием системы программного обеспечения статистического анализа (SAS) (Cary, NC).Все указанные корреляции являются коэффициентами линейной корреляции Пирсона. Для оценки надежности использовались парные t тестов. Односторонний дисперсионный анализ ANOVA использовался для сравнения средних уровней различных измерений жировых отложений и уровней IGFBP-I. При оценке комбинированного воздействия пола и стадии Таннера на уровни IGFBP-I и чувствительность к инсулину использовали двухфакторный дисперсионный анализ ANOVA. Пошаговый множественный регрессионный анализ был использован для исследования независимых предикторов IGFBP-I. РезультатыИзмерения IGFBP-IУ всех субъектов уровни IGFBP-I варьировались от <0.От 15 до 52,5 нг / мл со средним значением 9,9 ± 1,0. Средний уровень IGFBP-I у мальчиков (12,6 ± 1,6) был достоверно выше, чем у девочек (7,0 ± 1,2; P <0,01). Когда принималась во внимание стадия Таннера, уровни IGFBP-I были значительно выше у детей стадии Таннера 2 (11,7 ± 1,6), чем у детей стадии Таннера 3 (7,6 ± 1,1; P <0,08). Уровни IGFBP-I у девочек 3-й стадии Таннера (4,6 ± 1,3) были значительно ниже, чем у мальчиков 2-й стадии Таннера (13,5 ± 2.5; P <0,002) и мальчиков 3-й стадии Таннера (11,3 ± 1,7; P <0,03), но незначительно отличаются от девочек 2-й стадии Таннера (9,5 ± 1,9) (Таблица 2). Таблица 2. УровниIGFBP-1, Si, инсулина натощак и IGF-1 по полу и стадии Таннера
Уровни IGFBP-1, Si, инсулина натощак и IGF-1 по полу и стадии Таннера
Чувствительность к инсулину натощак и инсулину натощак измеренияСредний уровень инсулина натощак у мальчиков (65.1 пмоль / л ± 7,1) незначительно отличался от среднего уровня инсулина натощак у девочек (68,9 ± 4,3). Кроме того, не было различий в уровнях инсулина натощак между стадиями Таннера (Таблица 2). Однако были значительные различия в чувствительности к инсулину. Среднее значение Si у мальчиков (1,28 ± 0,09 × 10 −4 мин −1 / пмоль / л) было выше, чем у девочек (1,00 ± 0,07, P <0,01). Когда принималась во внимание стадия Таннера, Si был значительно ниже у девочек со стадией Таннера (0.83 ± 0,09) по сравнению с таковыми у девочек 2 стадии Таннера (1,16 ± 0,09, P <0,05), мальчиков 2 стадии Таннера (1,26 ± 0,13, P <0,005) и мальчиков 3 стадии Таннера (1,32 ± 0,12, P <0,005) (Таблица 2). Си в последних трех группах существенно не отличались друг от друга. Измерения IGF-IСредний уровень IGF-I у девочек (33,8 ± 1,2 нмоль / л) был значительно выше, чем у мальчиков (29 ± 1,1 нмоль / л, P <0.005). Уровни IGF-I также были выше у детей Tanner 3 (36,8 ± 1,1), чем у детей Tanner 2 (26,8 ± 0,85, P <0,0001). У девочек 3-й стадии Таннера уровень IGF-I был выше (39,3 ± 1,4 нмоль / л), чем у девочек 2-й стадии Таннера (28,1 ± 1,1 нмоль / л, P <0,0001), мальчиков 2-й стадии Таннера (25,8 ± 1,2 нмоль / л, P <0,0001), и мальчики на стадии Таннера 3 (33,7 ± 1,5 нмоль / л, P <0,006). Кроме того, мальчики на стадии Таннера 3 имели более высокие уровни IGF-I, чем мальчики и девочки на стадии Таннера ( P <0.01) (таблица 2). Измерение ожиренияТаблица 3 показывает средний ИМТ, процент жира в организме и общую массу жира для субъектов, разделенных по полу и стадии Таннера. При рассмотрении совокупности стадий Таннера не было гендерных различий между этими переменными. Однако у девочек на стадии Таннера 2 ИМТ и жировая масса были значительно ниже, чем у мальчиков Таннера 2 и девочек Таннера ( P <0,05). Мальчики на стадии Таннера 3 имели более низкий ИМТ, процент жира и массу жира, чем мальчики на стадии Таннера 2 ( P <0.05). Мальчики со стадией Таннера 3 также имели более низкий процент жира в организме, чем девочки Таннер 3 ( P <0,05) (Таблица 3). Таблица 3.ИМТ, процент жира в организме и жировая масса по полу и стадии Таннера
. | Мальчики
. | Девочки
. | Таннер 2 (n = 32)
. | Таннер 3 (n = 21)
. | Таннер 2 (n = 25)
. | Таннер 3 (n = 26)
. | ИМТ (кг 2 ) | 22,1 ± 0,9 | 19,5 ± 0,6 1 | 19,2 ± 0,7 2 | 21,6 ± 0,9 | 7 ± 1,7 | 24,1 ± 1,1 3 4 | 27 ± 1,6 | 28,9 ± 1,9 | Масса жира (кг) | 17,6 ± 1,6 3 | 12,8 ± 0,9 5 | 11,8 ± 1,2 6 | 16,3 ± 1,8 | Предикторы IGFBP-IНаблюдалась сильная положительная корреляция между уровнями IGFBP-I и Si (r = 0,65, P <0,0001) (рис.1), тогда как корреляция между IGFBP-I и уровнями инсулина натощак была ниже (r = -0,38, P <0,0001). Также была обнаружена обратная зависимость между уровнями IGFBP-I и всеми показателями ожирения (ИМТ, r = - 0,46, P <0,0001; жировая масса, r = -0,44, P <0,0001; процент жира в организме, r = −0,41, P <0,0002) (рис.2). У девочек уровни IGFBP-I также обратно коррелировали с уровнями IGF-I (r = -0,41, P <0,003) (рис. 3).Уровни IGFBP-I не были связаны ни с уровнями тестостерона, ни с уровнями эстрогена. Построен пошаговый множественный регрессионный анализ с учетом переменных пола, стадии Таннера, чувствительности к инсулину, ожирения, уровней IGF-I, инсулина натощак и половых стероидов. Также были проанализированы двусторонние взаимодействия этих переменных. Когда были рассмотрены все субъекты, уровни IGFBP-I лучше всего прогнозировались по чувствительности к инсулину ( P <0,0001) и уровням IGF-I ( P <0,015) (для общей модели r 2 = 0.45, P <0,0001). Рисунок 1. Уровни IGFBP-I натощак по сравнению с чувствительностью к инсулину , измеренной с помощью модифицированной минимальной модели Бергмана, у 104 мальчиков и девочек в раннем пубертатном периоде, r = 0,65, P <0,0001. Рисунок 1. Уровни IGFBP-I натощак по сравнению с чувствительностью к инсулину , измеренной с помощью модифицированной минимальной модели Бергмана, у 104 мальчиков и девочек раннего полового созревания, r = 0,65, P <0.0001. Рисунок 2. Уровни IGFBP-I натощак против ИМТ у мальчиков и девочек раннего полового созревания. Для мальчиков (обозначено пунктирной линией ) r = -0,53, P <0,0001. Для девочек (обозначено сплошной линией ) r = — 0,47, P <0,0004. Рис. 2. Уровни IGFBP-I натощак по сравнению с ИМТ у мальчиков и девочек раннего полового созревания. Для мальчиков (обозначено пунктирной линией ) r = −0.53, P <0,0001. Для девочек (обозначено сплошной линией ) r = — 0,47, P <0,0004. Рисунок 3. Уровни IGFBP-I натощак против . уровни IGF-I натощак у девочек раннего полового созревания, r = -0,41, P <0,003. Рисунок 3. Уровни IGFBP-I натощак против . уровни IGF-I натощак у девочек раннего полового созревания, r = -0,41, P <0,003. ОбсуждениеУровниIGFBP-I были измерены у 104 девочек и мальчиков раннего полового созревания, и в соответствии с другими сообщениями, в нашей исследуемой популяции наблюдался широкий диапазон уровней IGFBP-I.Уровни IGFBP-I сильно и положительно коррелировали с чувствительностью к инсулину, но лишь слабо коррелировали с уровнями инсулина натощак. Несколько исследований продемонстрировали обратную зависимость между IGFBP-I и уровнями инсулина (9). Исследования in vitro показали, что физиологические концентрации инсулина ингибируют накопление белка IGFBP-I и уровни информационной РНК IGFBP-I в линиях клеток печени. Считается, что этот ингибирующий эффект инсулина опосредуется на уровне транскрипции (23, 24). Хотя инсулин напрямую подавляет продукцию IGFBP-I, уровни IGFBP-I подавляются у инсулинорезистентных субъектов. Это говорит о том, что резистентность к инсулино-опосредованному удалению глюкозы сопровождается сохранением чувствительности печени к инсулину в отношении продукции IGFBP-I. Учитывая, что сам инсулин непосредственно ингибирует IGFBP-I, интересно, что уровни IGFBP-I в большей степени связаны с показателями чувствительности к инсулину, чем с уровнями самого инсулина. Это может быть вторичным по отношению к быстрой колебательной природе секреции инсулина, а уровни С-пептида могут иметь более сильную корреляцию с уровнями IGFBP-I (25).Кроме того, возможно, что концентрация портального инсулина является основным регулятором продукции IGFBP-I (25). Периферический инсулин отражает, но не обязательно предсказывает концентрацию портального инсулина. Следовательно, сильная взаимосвязь, обнаруженная между IGFBP-I и чувствительностью к инсулину, вероятно, отражает инсулиновую зависимость обеих переменных. Считается, что IGFBP-I снижает действие IGF-I, ингибируя его связывание с клеточными мембранами (10). Хотя большинство исследований предполагают, что основная роль IGFBP-I заключается в регулировании метаболических действий свободного IGF-I, есть доказательства того, что он также может регулировать митогенные эффекты IGF-I.Cox et al. (26) продемонстрировали, что совместное введение рекомбинантного человеческого IGFBP-I (rhIGFBP-I) с rhIGF-I гипофизэктомированным крысам приводит к ингибированию стимулирующих рост эффектов rhIGF-I. Кроме того, постулируется, что IGFBP-I играет роль в замедлении линейного роста, наблюдаемом у детей с хронической почечной недостаточностью. Было показано, что у этих детей уровни IGFBP-I и сывороточная IGF-связывающая активность были повышены по сравнению с контрольной группой (27). Следовательно, интересно предположить, как и другие, что существует взаимосвязь между уровнями IGFBP-I и ростом у детей с ожирением.Хорошо известно, что дети с ожирением имеют более высокие темпы роста и высокие концентрации IGF-I в сыворотке, несмотря на снижение секреции GH; однако механизмы, лежащие в основе этих измененных отношений, остаются неясными (28). Возможно, что инсулино-опосредованное подавление IGFBP-I у детей с ожирением может повысить уровень свободного IGF-I и, таким образом, способствовать наблюдаемому усиленному росту. Тот же механизм может действовать у детей полового созревания, у которых инсулинорезистентность и рост происходят одновременно. Были продемонстрированы гендерные различия в уровнях IGFBP-I, причем у мальчиков уровни были значительно выше, чем у девочек.Другие исследования детей, насколько нам известно, не выявили этих гендерных различий. Холли и др. (14) измерил уровни IGFBP-I во время голодания у детей препубертатного и пубертатного возраста и обнаружил тенденцию только у мальчиков препубертатного возраста иметь более высокие пиковые уровни IGFBP-I, чем у девочек препубертатного возраста. В более крупном исследовании Juul et al. (29) измерили уровни IGFBP-I у 907 детей и не обнаружили гендерных различий. Исследования взрослых показали, что у женщин уровень IGFBP-I выше, чем у мужчин (30).Механизм, лежащий в основе этих гендерных различий, обнаруженных у взрослых, не выяснен; однако было высказано предположение, что эстроген может повышать концентрацию IGFBP-I (31, 32). В нашем исследовании у мальчиков был более высокий уровень IGFBP-I, и это можно объяснить наблюдением, что у мальчиков была более высокая чувствительность к инсулину, чем у девочек. Гендерные различия в уровнях IGF-I также могут вносить вклад в наблюдаемые различия в IGFBP-I. У мальчиков уровни IGF-I были ниже, чем у девочек, и было обнаружено, что уровни IGFBP-I у девочек обратно коррелированы с IGF-I.Поскольку мы изучали детей в раннем периоде полового созревания, возможные эффекты эстрогена не обязательно проявлялись, потому что уровни у девочек не достигли значений для взрослых. В настоящем исследовании было обнаружено, что уровни IGFBP-I имеют сильную одномерную обратную корреляцию с ожирением тела. Скорее всего, это объясняется влиянием ожирения на чувствительность к инсулину. В предыдущем исследовании мы показали, что чувствительность к инсулину у детей раннего полового созревания в наибольшей степени связана с ожирением тела (16).Кроме того, однофакторная взаимосвязь между IGFBP-I и ожирением в настоящем исследовании не сохраняется при использовании множественной модели, включающей чувствительность к инсулину. Это говорит о том, что ожирение не связано независимо с IGFBP-I. В заключение, уровни IGFBP-I у детей полового созревания демонстрируют гендерные различия, противоположные тем, которые наблюдаются у взрослых. У мальчиков уровень IGFBP-I был значительно выше, чем у девочек, и это, по-видимому, вторично по отношению к гендерным различиям в чувствительности к инсулину.Кроме того, инсулин, IGF-I и жирность тела обратно пропорциональны уровню IGFBP-I. Однако самая сильная связь была между чувствительностью к инсулину и IGFBP-I. Это говорит о том, что резистентность к инсулину, возникающая в период полового созревания, особенно у детей с ожирением, не распространяется на резистентность к подавлению IGFBP-I. Интересно предположить, что опосредованное инсулином подавление уровней IGFBP-I может увеличить свободный IGF-I и, таким образом, усилить его митогенное действие. Это, следовательно, могло способствовать ускоренному росту, наблюдаемому как у детей с ожирением, так и у детей полового созревания. Мы благодарим Терезу Шарп, Трейси Хортон и Дебби Якобсон за выполнение подводных измерений веса. Мы также благодарим сотрудников Общего клинического исследовательского центра Детской больницы за их огромные усилия, которые помогли завершить этот проект. 1Бакстер RC , Мартин JL.1989 Связывающие белки для инсулиноподобных факторов роста. Prog Growth Factor Res .1 :49 —68 .2Blum WF ,Albertsson-Wikland K ,Rosberg S , Ranke MB.1993 Уровни в сыворотке инсулиноподобного фактора роста I (IGF-1) и IGF-связывающего белка 3 отражают спонтанную секрецию гормона роста. Дж Клин Эндокринол Метаб .76 :1610 —1616 .3Suikkari AM ,Koivisto VA ,Rutanen EM ,Yki-9000 Kar5000 9000 9000 9000 Härvin2en 000 , Сеппяля М. 1988 Инсулин регулирует сывороточные уровни белков, связывающих низкомолекулярный инсулиноподобный фактор роста. Дж Клин Эндокринол Метаб .66 :266 —272 .4Conover CA ,Butler PC ,Wang M ,Rizza PDK RA , Lee.1990 Отсутствие эффекта гормона роста на инсулино-ассоциированное подавление белка 1, связывающего инсулиноподобный фактор роста, у людей. Диабет .39 :1251 —1256 .5Lewitt MS , Baxter RC.1989 Регулирование гормона роста-независимого белка, связывающего инсулиноподобный фактор роста (ВР-28) в культивируемых эксплантатах печени плода человека. Дж Клин Эндокринол Метаб .69 :246 —252 ,6Cotterill AM ,Cowell CT ,Baxter RC ,McNeil Dik Dik 1988 Регулирование белка, связывающего фактор роста, не зависящего от гормона роста, у детей. Дж Клин Эндокринол Метаб .67 :882 —887 .7Suikkari AM ,Sane T ,Seppälä M ,Yki-Järvin2000 9000 9000 Härvin2000 9000 9000 Karvin 9000 , Койвисто В.А. 1989 Продолжительные упражнения увеличивают сывороточные концентрации белка, связывающего инсулиноподобный фактор роста. Дж Клин Эндокринол Метаб .68 :141 —144 .8Партия JA ,Baxter RC , Werther G.1991 Аномальная регуляция инсулино-подобного фактора роста белков инсулина подростка -зависимый диабет. Дж Клин Эндокринол Метаб .73 :964 —968 ,9Lee PDK ,Jensen MD ,Divertie GD ,Heiling VJ2 CA. 1993 Ответ белка-1, связывающего инсулиноподобный фактор роста, на инсулин во время подавления секреции эндогенного инсулина. Метаболизм .42 :409 —414 .10Ritvos O ,Ranta T ,Jalkanen J и др.1988 Белок, связывающий инсулиноподобный фактор роста (IGF) из децидуальной оболочки человека, ингибирует связывание и биологическое действие IGF-1 в культивируемых клетках хориокарциномы. Эндокринология .122 :2150 —2157 .11Buyalos RP ,Pekonen F ,Halme JK ,Judd HJutan 1995 Взаимосвязь между циркулирующими андрогенами, ожирением и гиперинсулинемией на сывороточный белок-1, связывающий инсулиноподобный фактор роста, при синдроме поликистозных яичников. Am J Obstet Gynecol .172 :932 —939 .12Mogul HR ,Marshall M ,Frey M и др.1996 Инсулиноподобный фактор роста-связывающий белок-1 как маркер гиперинсулинемии у полных женщин в менопаузе. Дж Клин Эндокринол Метаб .81 :4492 —4495 ,13Ибанжес Л ,Потау N ,Замполли M ,000 Sampolli M ,000 Сагер 000Рике Рике 9000 А.1997 Гиперинсулинемия и пониженное содержание белка-1, связывающего инсулиноподобный фактор роста, являются общими признаками у девочек препубертатного и пубертатного возраста с анамнезом преждевременного лобка. Дж Клин Эндокринол Метаб .82 :2283 —2288 .14Холли JMP ,Smith CP ,Dunger DB и др.1989 Уровни небольшого белка, связывающего инсулиноподобный фактор роста, сильно связаны с уровнями инсулина у детей препубертатного и пубертатного возраста, но лишь слабо после полового созревания. Дж Эндокринол .121 :383 —387 .15Caprio S ,Plewe G ,Diamond MP и др.1989 Повышенная секреция инсулина в период полового созревания: компенсаторный ответ на снижение чувствительности к инсулину. J Педиатр .114 :963 —967 .16Travers SH ,Jeffers BW ,Bloch CA ,Hill JckOel .1995 Гендерные и кожные различия в составе тела и чувствительности к инсулину у детей раннего полового созревания. Дж Клин Эндокринол Метаб .80 :172 —178 ,17Таннер JM .1962 Рост и отрочество.2-е изд. Oxford :Blackwell Scientific Publications. 18Bergman RN ,Beard JC ,Chen M .1986 Метод минимального моделирования. Оценка чувствительности к инсулину и функции бета-клеток in vivo . В: Кларк В.Л., Ларнер Дж., Поль С.Л., ред. Методы исследования диабета, т. II: клинические методы.Нью-Йорк :John Wiley & Sons; 16–34. 19Катфилд WS ,Бергман RN ,Menon RK , Sperling MA.1990 Модифицированная минимальная модель: приложение для измерения чувствительности к инсулину у детей. Дж Клин Эндокринол Метаб .70 :1644 —1650 ,20Roche AF ,Siervogel RM ,Chumlea WC , Webb P.Ограниченная жирность тела .Ам Дж. Клин Нутр .34 :2831 —2838 ,21Ломан Т.Г. 1986 Применимость методов и констант композиции тела для детей и юношества. Exerc Sport Sci Rev .14 :325 —357 .22Desbuquois B , Aurbach GD.1971 Использование полиэтиленгликоля для разделения свободных и связанных с антителами пептидных гормонов в радиоиммуноанализах. Дж Клин Эндокринол Метаб .33 :732 —738 .23Пауэлл DR ,Suwanichkul A ,Cubbage ML ,DePaolis DePaolis LAPDK. 1991 Инсулин ингибирует транскрипцию человеческого гена белка-1, связывающего инсулиноподобный фактор роста. Дж. Биол Хим .266 :18868 —18876 .24Suwanichkul A ,Allender SV ,Morris SL , Powell DR.1994 Глюкокортикоиды и инсулин регулируют экспрессию человеческого гена белка-1, связывающего инсулиноподобный фактор роста, через проксимальные элементы промотора. Дж. Биол Хим .269 :30835 —30841 ,25Yki-Järvinen H ,Mäkimattila S ,Utriainen EMTen .1995 Концентрации портального инсулина, а не чувствительность к инсулину, регулируют сывороточный глобулин, связывающий половые гормоны, и белок, связывающий инсулиноподобный фактор роста 1 in vivo . Дж Клин Эндокринол Метаб .80 :3227 —3232 .26Cox GN ,McDermott MJ ,Merkel E и др.1994 Рекомбинантный белок-1, связывающий человеческий инсулиноподобный фактор роста (IGF), подавляет соматический рост, стимулируемый IGF-1 и гормоном роста, у гипофизэктомированных крыс. Эндокринология .135 :1913 —1920 .27Lee PDK ,Hintz RL ,Sperry BC ,Baxter RC .1989 Белки, связывающие инсулиноподобный фактор роста в сыворотке крови у детей с задержкой роста с хронической почечной недостаточностью. Педиатр Res .36 :308 —315 ,28Бине E ,Schlumberger A , Chaussain JL.1976 Активность соматомедина в сыворотке у детей с ожирением. Педиатр Adolesc Endocrinol .1 :153 —156 .29Juul A ,Dalgaard P ,Werner FB и др.1995 Сывороточные уровни белка-3, связывающего инсулиноподобный фактор роста (IGF) (IGFBP-3) у здоровых младенцев, детей и подростков: связь с IGF-1, IGF-II, IGFBP-1, IGFBP-2, возраст, пол, индекс массы тела и половое созревание. Дж Клин Эндокринол Метаб .80 :2534 —2542 .30Yeoh S-I , Baxter RC.1988 Метаболическая регуляция независимого от гормона роста белка, связывающего инсулиноподобный фактор роста, в плазме крови человека. Acta Endocrinol (Копен) .119 :465 —473 .31Suikkari AM ,Tiitinen A ,Stenman UH ,9000 Launcher 000000 Men Оральные контрацептивы повышают концентрацию инсулиноподобного фактора роста-связывающего белка-1 у женщин с поликистозом яичников.Fertil Steril .55 :895 —899 .32Мартикайнен H ,Koistinen R , Seppälä M.1992 Влияние эстрогена на инсулино-индуцированные изменения в сыворотке крови. концентрация белка-1, связывающего фактор роста. Fertil Steril .58 :543 —546 .Авторские права © 1998 Общество эндокринологов Ритмичность менструального цикла: особенности обмена веществ у здоровых женщинQuabbe, H.J. Хронобиология секреции гормона роста. Chronobiologia 4 , 217–246 (1977). CAS PubMed Google Scholar Бейкер Ф. и Драйвер Х. С. Циркадные ритмы, сон и менструальный цикл. Sleep Med 8 , 613–622, https://doi.org/10.1016/j.sleep.2006.09.011 (2007). Артикул PubMed Google Scholar Van Reen, E. & Kiesner, J. Индивидуальные различия в самооценке трудностей со сном в течение менструального цикла. Arch Womens Ment Health 19 , 599–608, https://doi.org/10.1007/s00737-016-0621-9 (2016). Артикул PubMed Google Scholar Гласс, Л. Синхронизация и ритмические процессы в физиологии. Nature 410 , 277–284, https://doi.org/10.1038/35065745 (2001). ADS CAS Статья PubMed Google Scholar Shechter, A., Lesperance, P., Ng Ying Kin, N. M. & Boivin, D. B. Пилотное исследование циркадного ритма мелатонина в плазме в течение менструального цикла в небольшой группе женщин с предменструальным дисфорическим расстройством. PLoS One 7 , e51929, https://doi.org/10.1371/journal.pone.0051929 (2012). ADS CAS Статья PubMed PubMed Central Google Scholar Li, R., Cheng, S. и Wang, Z. Ген циркадных часов играет ключевую роль в овариальном цикле и самопроизвольном аборте. Cell Physiol Biochem 37 , 911–920, https://doi.org/10.1159/000430218 (2015). CAS Статья PubMed Google Scholar Аллен, А. М. и др. . Определение менструальной фазы в биоповеденческих исследованиях человека: обзор с рекомендациями. Exp Clin Psychopharmacol 24 , 1–11, https: // doi.org / 10.1037 / pha0000057 (2016). Артикул PubMed PubMed Central Google Scholar Штраус, Дж. Ф. Б. и Роберт Л. Репродуктивная эндокринология Йен и Яффе: физиология , Патофизиология , и клиническое управление , Седьмое издание . (Сондерс, 2014). Воет, Д. Э. А. Биохимия . Второе издание, 1272 г. (John Wiley & Sons, 1995). Гугаприя, Т. С., Картик, С. и Нагарджуна, Б. Проспективное исследование изменчивости гликемического контроля во время различных фаз менструального цикла у женщин с диабетом 2 типа, использующих высокочувствительный С — реактивный белок. Журнал клинических и диагностических исследований: JCDR 8 , CC01–04, https://doi.org/10.7860/JCDR/2014/8118.4240 (2014). CAS Статья PubMed Google Scholar Варламов, О., Бетеа, К. Л. и Робертс, К. Т. мл. Половые различия в метаболизме липидов и глюкозы. Frontiers in endocrinology 5 , 241, https://doi.org/10.3389/fendo.2014.00241 (2014). Артикул PubMed Google Scholar Йен, Дж. Й. и др. . Тяга женщин с предменструальным дисфорическим расстройством к пище с высоким содержанием сладких жиров: эмоциональная реакция, скрытое отношение и поощрение чувствительности. Психонейроэндокринология 35 , 1203–1212, https://doi.org/10.1016/j.psyneuen.2010.02.006 (2010). Артикул PubMed Google Scholar Макнил, Дж., Кэмерон, Дж. Д., Финлейсон, Г., Бланделл, Дж. Э. и Дусет, Э. Более высокие общие обонятельные характеристики, явное желание употреблять продукты с высоким содержанием жиров и липидов в середине лютеиновой фазы менструальный цикл. Физиология и поведение 112-113 , 84–89, https: // doi.org / 10.1016 / j.physbeh.2013.02.008 (2013). CAS Статья Google Scholar Шехтер А., Варин Ф. и Бойвин Д. Б. Циркадные вариации сна во время фолликулярной и лютеиновой фаз менструального цикла. Сон 33 , 647–656 (2010). Артикул Google Scholar Шехтер А. и Бойвин Д. Б. Сон, гормоны и циркадные ритмы на протяжении менструального цикла у здоровых женщин и женщин с предменструальным дисфорическим расстройством. Международный эндокринологический журнал 2010 , 259345, https://doi.org/10.1155/2010/259345 (2010). CAS Статья PubMed PubMed Central Google Scholar Киснер, Дж. У одной женщины низкий уровень — другой женский: парадоксальные эффекты менструального цикла. Психонейроэндокринология 36 , 68–76, https://doi.org/10.1016/j.psyneuen.2010.06.007 (2011). Артикул PubMed Google Scholar Биггс, В. С. и Демут, Р. Х. Предменструальный синдром и предменструальное дисфорическое расстройство. Am Fam Physician 84 , 918–924 (2011). PubMed Google Scholar Рю А. и Ким Т. Х. Предменструальный синдром: мини-обзор. Maturitas 82 , 436–440, https://doi.org/10.1016/j.maturitas.2015.08.010 (2015). Артикул PubMed Google Scholar Уоллес, М. и др. . Влияние фазы менструального цикла на метаболомный профиль у женщин в пременопаузе. Hum Reprod 25 , 949–956, https://doi.org/10.1093/humrep/deq.011 (2010). CAS Статья PubMed Google Scholar Фонг А. К. и Кретч М. Дж. Изменения в потреблении пищи, азота в моче и объеме мочи в течение менструального цикла. Am J Clin Nutr 57 , 43–46 (1993). CAS Статья Google Scholar Рид С. К., Левин Ф. Р. и Эванс С. М. Изменения настроения, когнитивных функций и аппетита в поздней лютеиновой и фолликулярной фазах менструального цикла у женщин с ПМДР и без нее (предменструальное дисфорическое расстройство). Horm Behav 54 , 185–193, https://doi.org/10.1016/j.yhbeh.2008.02.018 (2008). CAS Статья PubMed PubMed Central Google Scholar Frackiewicz, E. J. & Shiovitz, T. M. Оценка и лечение предменструального синдрома и предменструального дисфорического расстройства. J Am Pharm Assoc (Вашингтон) 41 , 437–447 (2001). CAS Статья Google Scholar Дай, Л. и Бланделл, Дж. Э. Менструальный цикл и контроль аппетита: значение для регулирования веса. Hum Reprod 12 , 1142–1151 (1997). CAS Статья Google Scholar Каллоуэй, Д. Х. и Курцер, М. С. Менструальный цикл и потребности женщин в белке. Журнал питания 112 , 356–366 (1982). CAS Статья Google Scholar Горчица, А. М. и др. . Изменения в потреблении макроэлементов, микроэлементов и пищевых групп на протяжении менструального цикла у здоровых женщин в пременопаузе. Eur J Nutr 55 , 1181–1188, https: // doi.org / 10.1007 / s00394-015-0931-0 (2016). CAS Статья PubMed Google Scholar Webb, P. 24-часовой расход энергии и менструальный цикл. Am J Clin Nutr 44 , 614–619 (1986). CAS Статья Google Scholar Монтане, Дж. Л. и Перес-Баллестер, Б. Циклические изменения содержания и состава фосфолипидов в эндометрии человека во время менструального цикла. J Reprod Fertil 73 , 317–321 (1985). CAS Статья Google Scholar Бонни Р. С. Измерение активности фосфолипазы А2 в эндометрии человека во время менструального цикла. J Endocrinol 107 , 183–189 (1985). CAS Статья Google Scholar Haoula, Z. et al. . Липидомный анализ образцов плазмы от женщин с синдромом поликистозных яичников. Metabolomics 11 , 657–666, https://doi.org/10.1007/s11306-014-0726-y (2015). CAS Статья PubMed Google Scholar Zhao, Y. et al. . Метаболические профили, характеризующие различные фенотипы синдрома поликистозных яичников: анализ метаболомики плазмы. BMC Med 10 , 153, https://doi.org/10.1186/1741-7015-10-153 (2012). CAS Статья PubMed PubMed Central Google Scholar Баттиста, Н. и др. . Роль эндоканнабиноидов в функции гонад и фертильности вдоль оси эволюции. Mol Cell Endocrinol 355 , 1–14, https://doi.org/10.1016/j.mce.2012.01.014 (2012). CAS Статья PubMed Google Scholar Горзалка Б. Б. и Данг С. С. Мини-обзор: Эндоканнабиноиды и гонадные гормоны: двунаправленные взаимодействия в физиологии и поведении. Эндокринология 153 , 1016–1024, https://doi.org/10.1210/en.2011-1643 (2012). CAS Статья PubMed Google Scholar Карриер, Э. Дж., Патель, С. и Хиллард, К. Дж. Эндоканнабиноиды в нейроиммунологии и стрессе. Препарат Curr действует на нервные расстройства в ЦНС 4 , 657–665 (2005). CAS Статья Google Scholar Ан, К., Маккинни, М. К. и Краватт, Б. Ф. Ферментативные пути, регулирующие передачу сигналов эндоканнабиноидов в нервной системе. Chem Rev 108 , 1687–1707, https://doi.org/10.1021/cr0782067 (2008). CAS Статья PubMed PubMed Central Google Scholar Mai, M. et al. . Уровни ацилкарнитинов в сыворотке крови изменяются в преддиабетических состояниях. PLoS One 8 , e82459, https: // doi.org / 10.1371 / journal.pone.0082459 (2013). ADS CAS Статья PubMed PubMed Central Google Scholar Рутковски, Дж. М. и др. . Ацилкарнитины активируют провоспалительные сигнальные пути. Американский физиологический журнал. Эндокринология и метаболизм 306 , E1378–1387, https://doi.org/10.1152/ajpendo.00656.2013 (2014). CAS Статья PubMed PubMed Central Google Scholar Ке, К. и др. . Профили метаболизма плазмы у женщин зависят от менопаузы. PLoS One 10 , e0141743, https://doi.org/10.1371/journal.pone.0141743 (2015). CAS Статья PubMed PubMed Central Google Scholar Barnett, J. B. et al. . Уровни липидов и липопротеинов в плазме во время фолликулярной и лютеиновой фаз менструального цикла. Журнал клинической эндокринологии и метаболизма 89 , 776–782, https: // doi.org / 10.1210 / jc.2003-030506 (2004). CAS Статья PubMed Google Scholar Schisterman, E. F., Mumford, S. L. & Sjaarda, L. A. Отсутствие учета фазы менструального цикла может привести к неверной интерпретации клинических и исследовательских данных кардиометаболических биомаркеров у женщин в пременопаузе. Epidemiol Rev 36 , 71–82, https://doi.org/10.1093/epirev/mxt007 (2014). Артикул PubMed Google Scholar Ахумада Хемер, Х. и др. . Изменения липидов и липопротеинов в сыворотке крови на протяжении менструального цикла. Fertil Steril 44 , 80–84 (1985). CAS Статья Google Scholar Смит, Г. И., Ридс, Д. Н., Окунаде, А. Л., Паттерсон, Б. В. и Миттендорфер, Б. Системная доставка эстрадиола, но не тестостерона или прогестерона, изменяет кинетику липопротеинов и триглицеридов очень низкой плотности у женщин в постменопаузе. Журнал клинической эндокринологии и метаболизма 99 , E1306–1310, https://doi.org/10.1210/jc.2013-4470 (2014). CAS Статья PubMed PubMed Central Google Scholar Dinicola, S., Chiu, T. T., Unfer, V., Carlomagno, G. & Bizzarri, M. Обоснование комбинированного лечения мио-инозитола и D-хиро-инозита при синдроме поликистозных яичников. J Clin Pharmacol 54 , 1079–1092, https: // doi.org / 10.1002 / jcph.362 (2014). CAS Статья PubMed Google Scholar Rago, R. et al. . Влияние мио-инозита и альфа-липоевой кислоты на качество ооцитов у женщин с синдромом поликистозных яичников без ожирения, перенесших оплодотворение in vitro : пилотное исследование. J Biol Regul Homeost Agents 29 , 913–923 (2015). CAS PubMed Google Scholar Карломаньо Г., Нордио М., Чиу Т. и Унфер В. Вклад мио-инозита и мелатонина в репродуктивную функцию человека. евро J Obstet Gynecol Reprod Biol 159 , 267–272, https://doi.org/10.1016/j.ejogrb.2011.07.038 (2011). CAS Статья PubMed Google Scholar Пейн, Дж. Л., Палмер, Дж. Т. и Иоффе, Х. Репродуктивный подтип депрессии: концептуализация моделей и движение к этиологии. Harv Rev Psychiatry 17 , 72–86, https://doi.org/10.1080/10673220 9706 (2009).Артикул PubMed PubMed Central Google Scholar Payne, J. L. et al. . Симптомы настроения, связанные с репродуктивным циклом, у женщин с большой депрессией и биполярным расстройством. J Affect Disord 99 , 221–229, https://doi.org/10.1016/j.jad.2006.08.013 (2007). Артикул PubMed Google Scholar Перич, Т.А. и др. . Клиническая характеристика женщин с симптомами биполярного расстройства, связанного с репродуктивным циклом. Aust N Z J Psychiatry 51 , 161–167, https://doi.org/10.1177/0004867416670015 (2017). Артикул PubMed Google Scholar Вигод, С. Н., Страсбург, К., Даскалакис, З. Дж. И Блумберже, Д. М. Систематический обзор дефицита ингибиторов гамма-аминомасляной кислоты на протяжении репродуктивного жизненного цикла. Arch Womens Ment Health 17 , 87–95, https://doi.org/10.1007/s00737-013-0403-6 (2014). Артикул PubMed Google Scholar Amin, Z. et al. . Взаимодействие нейроактивных стероидов и ГАМК в развитии нервно-психических расстройств у женщин. Pharmacol Biochem Behav 84 , 635–643, https://doi.org/10.1016/j.pbb.2006.06.007 (2006). CAS Статья PubMed Google Scholar Clayton, A.H., Keller, A.E., Leslie, C. & Evans, W. Исследовательское исследование предменструальных симптомов и изменчивости серотонина. Arch Womens Ment Health 9 , 51–57, https://doi.org/10.1007/s00737-005-0118-4 (2006). CAS Статья PubMed Google Scholar Талли Д. Б., Олгуд В. Э. и Сидловски Дж. А. Модуляция экспрессии гена, опосредованной стероидными рецепторами, с помощью витамина B6. FASEB J 8 , 343–349 (1994). CAS Статья Google Scholar Кашанян М., Мазинани Р. и Джалалманеш С. Пиридоксин (витамин B6) для лечения предменструального синдрома. Int J Gynaecol Obstet 96 , 43–44, https://doi.org/10.1016/j.ijgo.2006.09.014 (2007). CAS Статья PubMed Google Scholar Долл, Х., Браун, С., Терстон, А.И Весси, М. Пиридоксин (витамин B6) и предменструальный синдром: рандомизированное перекрестное исследование. J R Coll Gen Pract 39 , 364–368 (1989). CAS PubMed PubMed Central Google Scholar Damoiseaux, V. A., Proost, J. H., Jiawan, V. C. & Melgert, B. N. Половые различия в фармакокинетике антидепрессантов: влияние женских половых гормонов и оральных контрацептивов. Clin Pharmacokinet 53 , 509–519, https: // doi.org / 10.1007 / s40262-014-0145-2 (2014). CAS Статья PubMed Google Scholar Байерле, И., Мейбом, Б. и Дерендорф, Х. Гендерные различия в фармакокинетике и фармакодинамике. Int J Clin Pharmacol Ther 37 , 529–547 (1999). CAS PubMed Google Scholar Предигер, М. Э., Гамаро, Г. Д., Крема, Л.М., Фонтелла, Ф. У. и Далмаз, С. Эстрадиол защищает от окислительного стресса, вызванного хроническим разнообразным стрессом. Neurochem Res 29 , 1923–1930 (2004). CAS Статья Google Scholar Serviddio, G. et al. . Модуляция окислительно-восстановительного баланса эндометрия во время менструального цикла: связь с половыми гормонами. Журнал клинической эндокринологии и метаболизма 87 , 2843–2848, https: // doi.org / 10.1210 / jcem.87.6.8543 (2002). CAS Статья PubMed Google Scholar Massafra, C. et al. . Влияние эстрогенов и андрогенов на активность супероксиддисмутазы, антиоксиданта эритроцитов, каталазы и глутатионпероксидазы во время менструального цикла. J Эндокринол 167 , 447–452 (2000). CAS Статья Google Scholar Ха, Э. Дж. И Смит, А. М. Селен в плазме, а также активность глутатионпероксидазы в плазме и эритроцитах повышаются с эстрогеном во время менструального цикла. J Am Coll Nutr 22 , 43–51 (2003). CAS Статья Google Scholar Sheng-Huang, C. et al. . Влияние эстрогена на уровни глутатиона и каталазы в эритроцитах человека во время менструального цикла. Biomed Rep 3 , 266–268, https: // doi.org / 10.3892 / br.2014.412 (2015). Артикул PubMed Google Scholar Алмейда, М. и др. . Эстрогены ослабляют окислительный стресс, а также дифференциацию и апоптоз остеобластов за счет независимого от связывания ДНК действия ERalpha. J Bone Miner Res 25 , 769–781, https://doi.org/10.1359/jbmr.0 (2010). CAS Статья PubMed Google Scholar Аббас, А. М. и Эльсамануди, А. З. Влияние 17-бета-эстрадиола и введения антиоксидантов на окислительный стресс и инсулинорезистентность у крыс с удаленными яичниками. Can J Physiol Pharmacol 89 , 497–504, https://doi.org/10.1139/Y11-053 (2011). CAS Статья PubMed Google Scholar Duvan, C. I., Cumaoglu, A., Turhan, N. O., Karasu, C. & Kafali, H. Окислительный / антиоксидантный статус при предменструальном синдроме. Arch Gynecol Obstet 283 , 299–304, https://doi.org/10.1007/s00404-009-1347-y (2011). CAS Статья PubMed Google Scholar Pal, L. et al. . Терапевтическое значение витамина D и кальция у женщин с избыточным весом и синдромом поликистозных яичников. Гинекол Эндокринол 28 , 965–968, https://doi.org/10.3109/0 | (2012). CAS Статья PubMed PubMed Central Google Scholar Бертоне-Джонсон, Э. Р., Чокано-Бедоя, П. О., Загаринс, С. Э., Мика, А. Э. и Ронненберг, А. Г. Потребление витамина D с пищей, уровни 25-гидроксивитамина D3 и предменструальный синдром у населения студенческого возраста. J Steroid Biochem Mol Biol 121 , 434–437, https://doi.org/10.1016/j.jsbmb.2010.03.076 (2010). CAS Статья PubMed Google Scholar Патрик, Р. П. и Эймс, Б. Н.Гормон витамина D регулирует синтез серотонина. Часть 1: актуальность для аутизма. FASEB J 28 , 2398–2413, https://doi.org/10.1096/fj.13-246546 (2014). CAS Статья PubMed Google Scholar Ким, К. Х. Функциональное реле от прогестерона до витамина D в иммунной системе. DNA Cell Biol 34 , 379–382, https://doi.org/10.1089/dna.2015.2857 (2015). CAS Статья PubMed PubMed Central Google Scholar Mendoza, C., Ortega, E., Ruiz, E., Carreras, A. и Osorio, C. Метаболизм кальция у женщин в постменопаузе. Rev Esp Fisiol 41 , 447–450 (1985). CAS PubMed Google Scholar Ирани, М. и Мери, З. Роль витамина D в физиологии яичников и его влияние на репродуктивную функцию: систематический обзор. Fertil Steril 102 , 460–468 e463, https://doi.org/10.1016 / j.fertnstert.2014.04.046 (2014). CAS Статья PubMed Google Scholar Knight, J. A., Wong, J., Blackmore, K. M., Raboud, J. M. & Vieth, R. Связь витамина D с эстрадиолом и прогестероном у молодых женщин. Контроль причин рака 21 , 479–483, https://doi.org/10.1007/s10552-009-9466-0 (2010). Артикул PubMed Google Scholar Браш, М. Г., Уотсон, С. Дж., Хорробин, Д. Ф. и Манку, М. С. Аномальные уровни незаменимых жирных кислот в плазме у женщин с предменструальным синдромом. Am J Obstet Gynecol 150 , 363–366 (1984). CAS Статья Google Scholar Montserrat-de la Paz, S., Garcia-Gimenez, MD, Angel-Martin, M., Perez-Camino, MC & Fernandez Arche, A. Длинноцепочечные жирные спирты из масла примулы вечерней ингибируют воспалительный ответ в перитонеальных макрофагах мышей. J Ethnopharmacol 151 , 131–136, https://doi.org/10.1016/j.jep.2013.10.012 (2014). CAS Статья PubMed Google Scholar Голд, Э. Б., Уэллс, К. и Расор, М. О. Связь воспаления с предменструальными симптомами. J Womens Health (Larchmt) 25 , 865–874, https://doi.org/10.1089/jwh.2015.5529 (2016). Артикул Google Scholar Хубер, М. и др. . Как мы должны определять здоровье? BMJ 343 , d4163, https://doi.org/10.1136/bmj.d4163 (2011). Артикул PubMed Google Scholar Стров, Дж. Х. М., ван Витмаршен, Х., Кремер, Б. Х. А., ван Оммен, Б. и Воперейс, С. Фенотипическая гибкость как мера здоровья: тест оптимальной пищевой стресс-реакции. Genes Nutr 10 , 13, https: // doi.org / 10.1007 / s12263-015-0459-1 (2015). CAS Статья PubMed PubMed Central Google Scholar ван Оммен, Б., ван дер Греф, Дж., Ордовас, Дж. М. и Даниэль, Х. Фенотипическая гибкость как ключевой фактор во взаимоотношениях между питанием и здоровьем человека. Genes Nutr 9 , 423, https://doi.org/10.1007/s12263-014-0423-5 (2014). Артикул PubMed PubMed Central Google Scholar Сохраби Н., Кашанян М., Гафури С. и Малакути С. К. Оценка эффекта омега-3 жирных кислот при лечении предменструального синдрома: «пилотное испытание». Complement Ther Med 21 , 141–146, https://doi.org/10.1016/j.ctim.2012.12.008 (2013). Артикул PubMed Google Scholar Вятт, К. М., Диммок, П. В., Джонс, П. В. и Шон О’Брайен, П. М. Эффективность витамина B-6 в лечении предменструального синдрома: систематический обзор. BMJ 318 , 1375–1381 (1999). CAS Статья Google Scholar Бьянкини, Ф. и Вайнио, Х. Изотиоцианаты в профилактике рака. Drug Metab Rev 36 , 655–667, https://doi.org/10.1081/DMR-200033468 (2004). CAS Статья PubMed Google Scholar Ленц, Э. М. и др. .Метабономика, влияние питания и культурные различия: основанное на 1H ЯМР исследование образцов мочи, полученных от здоровых британских и шведских субъектов. J Pharm Biomed Anal 36 , 841–849, https://doi.org/10.1016/j.jpba.2004.08.002 (2004). CAS Статья PubMed Google Scholar Wallace, M. et al. . Связь между липидомом, маркерами воспаления и инсулинорезистентностью. Molecular bioSystems 10 , 1586–1595, https://doi.org/10.1039/c3mb70529c (2014). CAS Статья PubMed Google Scholar Noga, M. J. et al. . Метаболомика спинномозговой жидкости выявляет изменения в метаболизме центральной нервной системы на модели рассеянного склероза у крыс. Метаболомика 8 , 253–263, https://doi.org/10.1007/s11306-011-0306-3 (2012). CAS Статья PubMed Google Scholar van der Kloet, F. M., Bobeldijk, I., Verheij, E. R. & Jellema, R. H. Снижение аналитических ошибок с использованием калибровки по одной точке для точного и точного метаболомного фенотипирования. J Proteome Res 8 , 5132–5141, https://doi.org/10.1021/pr9r (2009). CAS Статья PubMed Google Scholar Hu, C. и др. . RPLC-ion-trap-FTMS метод определения липидного профиля плазмы: валидация метода и применение к модели мутантных мышей p53. J Proteome Res 7 , 4982–4991, https://doi.org/10.1021/pr800373m (2008). CAS Статья PubMed Google Scholar Kantae, V. et al. . Эндоканнабиноидный тонус у здоровых худощавых южноазиатских мужчин выше, чем у белых кавказских мужчин. Sci Rep 7 , 7558, https: // doi.org / 10.1038 / s41598-017-07980-5 (2017). ADS CAS Статья PubMed PubMed Central Google Scholar Петерс Ф. Т., Драммер О. Х. и Муссхофф Ф. Валидация новых методов. Forensic Int. 165 , 216–224, https://doi.org/10.1016/j.forsciint.2006.05.021 (2007). CAS Статья PubMed Google Scholar Abbott Laboratories, D. D. ARCHITECT Руководство по эксплуатации системы 201837-113-2016-04-29 (Abbott Park, IL 60064 USA2016). Маккалло, К. Э., Сирл, С. Р. и Нойхаус, Дж. М. Обобщенные , линейные , и смешанные модели , 2-е издание . 157–187 (John Wiley & Sons, 2008). Benjamini, Y. & Hochberg., Y. Контроль уровня ложных открытий: практичный и эффективный подход к множественному тестированию. Журнал Королевского статистического общества . Серия B (методологическая) 57 , 289–300 (1995). Артикул Google Scholar Hothorn, T., Bretz, F. и Westfall, P. Одновременный вывод в общих параметрических моделях. Biom J 50 , 346–363, https://doi.org/10.1002/bimj.200810425 (2008). MathSciNet Статья PubMed МАТЕМАТИКА Google Scholar Бейтс, Д. М. М. Б. Б. С. С. Подбор линейных моделей смешанных эффектов с использованием Ime4. Журнал статистического программного обеспечения 67 , 1–48 (2015). ADS Статья Google Scholar Т. З. А. Х. Диагностическая проверка в регрессионных отношениях. R News 2 , 7–10 (2002). Thiele, I. et al. . Глобальная реконструкция метаболизма человека по инициативе сообщества. Nat Biotechnol 31 , 419–425, https://doi.org/10.1038/nbt.2488 (2013). CAS Статья PubMed Google Scholar Свейнстон, Н., Мендес, П. и Келл, Д. Б. Анализ «управляемой сообществом» реконструкции метаболической сети человека. Метаболомика 9 , 757–764, https://doi.org/10.1007/s11306-013-0564-3 (2013). CAS Статья PubMed PubMed Central Google Scholar Swainston, N. и др. . Рекон 2.2: от реконструкции к модели метаболизма человека. Метаболомика 12 , 109, https://doi.org/10.1007/s11306-016-1051-4 (2016). CAS Статья PubMed PubMed Central Google Scholar Канехиса, М., Фурумичи, М., Танабе, М., Сато, Ю. и Моришима, К. КЕГГ: новые взгляды на геномы, пути, болезни и лекарства. Исследование нуклеиновых кислот 45 , D353 – D361, https: // doi.org / 10.1093 / nar / gkw1092 (2017). CAS Статья PubMed Google Scholar Halbreich, U., Borenstein, J., Pearlstein, T. & Kahn, L.S. Распространенность, нарушение, влияние и бремя предменструального дисфорического расстройства (ПМС / ПМДР). Психонейроэндокринология 28 (Приложение 3), 1-23 (2003). CAS PubMed Google Scholar Шмидт, П. Дж., Ниман, Л. К., Данасо, М. А., Адамс, Л. Ф. и Рубинов, Д. Р. Дифференциальные поведенческие эффекты гонадных стероидов у женщин с предменструальным синдромом и без него. Медицинский журнал Новой Англии 338 , 209–216, https://doi.org/10.1056/NEJM19 23380401 (1998). CAS Статья PubMed Google Scholar Fafouti, M. et al. . Расстройство настроения со смешанными признаками из-за дефицита витамина B (12) и фолиевой кислоты. Gen Hosp Psychiatry 24 , 106–109 (2002). Артикул Google Scholar Уровни циркулирующей ретиноевой кислоты и развитие метаболического синдрома | Журнал клинической эндокринологии и метаболизмаАбстрактныеКонтекст и цель: В этом проспективном исследовании мы оценили связь ретиноевой кислоты (РА) с метаболическим синдромом (МетС) у населения Китая. Дизайн и участники: В течение 4 лет проспективно наблюдались 1042 взрослых недиабетических взрослых из популяционной группы «Питание и здоровье стареющего населения». Определяли сывороточные концентрации RA и исследовали его взаимосвязь с MetS и его компонентом. Результаты: Исходно более высокие уровни РА были обратно связаны с наличием МетС (отношение шансов 0,61; 95% доверительный интервал [ДИ] 0,44–0,74, P <.001) после корректировки на возраст, пол, индекс массы тела, индекс оценки модели гомеостаза для инсулинорезистентности (HOMA-IR) и другие мешающие факторы. Пациенты с более низким уровнем РА имели прогрессивно худший профиль кардиометаболического риска на исходном уровне. Уровни RA в сыворотке были обратно связаны с 8-изопростагландином F2α ( P <0,001), высокочувствительным С-реактивным белком ( P = 0,015) и IL-6 ( P = 0,020). и положительно коррелировал с холестерином липопротеинов высокой плотности ( P =.038). Среди 825 субъектов без МетС на исходном уровне у 146 он развился через 4 года. RA в сыворотке по квартилям обратно коррелировал с встречающимся MetS (скорректированное отношение рисков 0,67; 95% ДИ 0,48–0,81, P = 0,006). Помимо HOMA-IR ( P <0,001), исходный уровень РА был единственным независимым предиктором развития метаболического синдрома в течение 4-летнего периода наблюдения (отношение шансов 0,53; 95% ДИ 0,40–0,69; P <0,001) после поправки на возраст, пол, индекс массы тела и HOMA-IR. Выводы: Уровень RA в сыворотке обратно пропорционален развитию MetS независимо от ожирения и инсулинорезистентности. Метаболический синдром (Метаболический синдром), совокупность множественных метаболических нарушений, включая центральное ожирение, дислипидемию, гипергликемию, инсулинорезистентность и гипертензию, стал серьезной проблемой общественного здравоохранения во всем мире. МетС играет важную роль в возникновении кардиометаболических заболеваний, включая сердечно-сосудистые заболевания и сахарный диабет 2 типа (1–3).Распространенность МетС резко возросла в последние десятилетия, что сопровождалось быстрым экономическим ростом, принятием малоподвижного образа жизни и резкими изменениями в привычках питания; в настоящее время он достигает масштабов эпидемии в Китае (4–6). Согласно последнему общенациональному опросу, проведенному в 2014 году, распространенность МетС у взрослых китайцев составляла примерно 20–25% (7). Хотя было доказано, что режимы питания играют важную роль в развитии этой эпидемии (8–11), крайне важно определить конкретные пищевые питательные вещества и их метаболиты для профилактики МетС. Полностью транс-ретиноевая кислота (РА) — это активный метаболит витамина А (ретинол), который обеспечивает физиологические функции, необходимые для роста и развития (11, 12). RA синтезируется внутриклеточно и в основном из ретинальдегида, который сам может быть продуцирован из ретинола или из каротиноидов провитамина А, таких как β-каротин (13). Он оказывает широкий спектр биологических эффектов в значительной степени за счет контроля экспрессии генов. RA связывается и активирует членов семейства ядерных рецепторов, включая рецептор ретиноевой кислоты и ретиноидный рецептор X (RXR), факторы транскрипции, которые связывают метаболизм витамина A с регуляцией транскрипции специфических генных кассет (14–16).RXR также контролирует ключевые метаболические пути, выступая в качестве облигатного гетеродимерного партнера для нескольких членов семейства ядерных рецепторов стероидных гормонов, включая рецепторы, активируемые пролифератором пероксисом (17). Адипогенез — это процесс дифференцировки, регулируемый сложным взаимодействием некоторых гетеродимерных партнеров RXR (18). В анализах дифференцировки адипоцитов 3T3-L1 эффекты ретиноевой кислоты варьируются в зависимости от стадии адипогенеза и относительного рецептора ретиноевой кислоты, рецептора-γ, активируемого пролифератором пероксисом, и экспрессии RXR (19).Ингибирование эндогенной продукции RA путем инактивации ретинальдегиддегидрогеназы (первичного фермента, метаболизирующего ретинальдегид) увеличивает рассеяние энергии и снижает накопление жира в брюшной полости, таким образом предотвращая и уменьшая ожирение, вызванное диетой (20). Хотя роль RA в адипогенезе в целом доказана in vitro, китайской популяции доступно мало информации о взаимосвязи между уровнем RA в сыворотке и MetS (а также его компонентами). Для дальнейшей оценки связи между RA в сыворотке и заболеваемостью MetS, мы проспективно исследовали 4-летнее развитие MetS по отношению к исходным уровням RA в сыворотке в популяционной когорте, состоящей из 1042 китайских субъектов, набранных из Guangzhou Nutrition и Популяция, изучающая здоровье старения. Материалы и методыУчастники исследованияУчастники исследования были отобраны из популяционного исследования «Питание и здоровье пожилого населения в Южном Китае», в котором изучались ассоциации диетических и генетических факторов, а также их взаимодействие с метаболическими заболеваниями, связанными со старением. С марта 2008 г. по март 2009 г. в перекрестном исследовании приняли участие 2280 человек в возрасте 50–70 лет. Среди этих субъектов 1042 субъекта без диабета (согласно диагностическим критериям Американской диабетической ассоциации 2007 г.) (21) были впоследствии приглашены для участия в проспективном когортном исследовании для оценки прогрессирования метаболического синдрома и его компонента.Субъекты, получавшие регулярные гиполипидемические препараты без доступного липидного профиля перед лечением или принимавшие поливитаминные добавки, были исключены из дальнейшего анализа. Протокол исследования был одобрен институциональным наблюдательным советом Университета Сунь Ятсена, проводился в соответствии с принципами, изложенными в Хельсинкской декларации, и от всех участников было получено письменное информированное согласие. Сбор данныхИсходные данные были собраны обученными интервьюерами с помощью полуструктурированных вопросников во время личных интервью.Анкета была разработана на основе нескольких пилотных опросов, проведенных среди этой группы населения. В анкету была включена информация о социально-демографических факторах, состоянии здоровья и образе жизни. Рост стоя, масса тела и окружность талии измерялись у участников в легкой домашней одежде и без обуви. Индекс массы тела (ИМТ) рассчитывался как вес в килограммах, разделенный на рост в метрах в квадрате. Два исследователя независимо вводили исходные данные из анкет, и данные были дополнительно проверены третьим исследователем, когда были обнаружены различия.Все испытуемые были обследованы утром после ночного голодания. Лабораторные измеренияОбразцы крови натощак в течение ночи собирали в пробирки, содержащие жидкую ЭДТА, центрифугировали при 4 ° C и хранили при -80 ° C до анализа. Общий холестерин в крови, холестерин липопротеинов высокой плотности (ЛПВП), триглицериды и глюкоза измеряли ферментативно на автоматическом биохимическом анализаторе Hitachi 7180 (Hitachi) с использованием коммерческого набора для анализа (Wako Pure Chemical Industries).Холестерин липопротеинов низкой плотности (ЛПНП) впоследствии был рассчитан по формуле Фридевальда (22). Концентрацию инсулина в плазме измеряли с помощью RIA (Roche), который имеет перекрестную реактивность с проинсулином менее 0,2%. Оценка модели гомеостаза инсулинорезистентности (HOMA-IR) рассчитывалась по следующей формуле: инсулин натощак (в единицах на литр) × глюкоза натощак (в миллимолях на литр) / 22,5. Концентрацию адипонектина измеряли в хранящейся замороженной плазме с использованием коммерчески доступного конкурентного набора для ELISA (R&D Systems; каталожный номер DRP300), как описано ранее (23).Уровни 8-изопростагландина F2α в плазме (8-изо PGF2α) количественно определяли с использованием набора для ELISA (Enzo Life Sciences International). Чувствительность анализа составила 16,3 пг / мл. Коэффициент вариации внутри анализа составлял 4,4–11%, а коэффициент вариации между анализами составлял 5,0–11%. С-реактивный белок (CRP) плазмы измеряли с помощью иммунотурбидиметрического анализа с усилением частиц (набор Ultrasensitive CRP; CRM Diagnostic Systems) с использованием микрочастиц, покрытых антителами против человеческого CRP. Точность метода в пороговом значении решения (1.8–2 мкг / мл) составляет менее 5,5%. Уровни IL-6 в сыворотке измеряли с использованием набора для ELISA IL-6 (Abcam). Определение концентраций РАКонцентрации RA в сыворотке измеряли с помощью имеющегося в продаже набора для ELISA в соответствии с инструкциями производителя (номер по каталогу MBS705877; MyBioSource). Этот анализ имеет высокую чувствительность и отличную специфичность для обнаружения ретиноевой кислоты человека. Не наблюдалось значительной перекрестной реактивности или интерференции между ретиноевой кислотой человека и аналогами.Диапазон обнаружения составляет 0,625–10 нг / мл. Уровни RA в сыворотке измеряли дважды в аликвотах сыворотки, подвергшихся одному или двум циклам замораживания-оттаивания. Образцы ELISA были проанализированы в двух экземплярах. Коэффициент вариации для межисследовательских повторных образцов был менее 8%. Определение MetSMetS был определен на основе обновленных критериев Национальной образовательной программы по холестерину / третьей группы лечения взрослых для американцев азиатского происхождения как имеющий по крайней мере три из следующих компонентов: 1) окружность талии 90 см или больше для мужчин или 80 см или больше для женщин; 2) триглицериды 1.7 ммоль / л или больше; 3) холестерин ЛПВП менее 1,03 ммоль / л для мужчин или менее 1,30 ммоль / л для женщин; 4) артериальное давление (АД) 130/85 мм рт.ст. или выше или текущий прием гипотензивных препаратов; или 5) уровень глюкозы натощак 5,6 ммоль / л или более, ранее диагностированный диабет 2 типа или лечение пероральными противодиабетическими средствами или инсулином (24). Статистический анализНормально распределенные данные были выражены как среднее ± стандартное отклонение, тогда как переменные с асимметричным распределением были представлены как медиана (межквартильный размах) и логарифмически преобразованы для приблизительной нормальности перед анализом.Категориальные переменные выражались как частота и процент. Ковариационный анализ для непрерывных переменных и многомерный логистический регрессионный анализ для категориальных переменных применялись для сравнения в соответствии с квартилями RA. Коэффициенты корреляции между РА и метаболическими особенностями рассчитывались с помощью частичного корреляционного анализа по рангам (корреляция Спирмена). Уровни RA в сыворотке отображали в соответствии с количеством компонентов MetS с использованием модели линейной регрессии. Модели многомерной логистической регрессии использовались для оценки отношения шансов (OR) для MetS и его компонентов.Возможные искажающие переменные, включая возраст, ИМТ, холестерин ЛПНП, холестерин ЛПВП, адипонектин, 8-iso PGF2α, высокочувствительный CRP (hsCRP), IL-6 и RA в квартилях, зависящих от пола. Обработка данных и статистический анализ выполнялись с помощью SPSS версии 19.0 (SPSS, Inc). P <0,05 считалось статистически значимым. РезультатыИсходные клинические характеристики когорты суммированы в таблице 1. Среди 1042 субъектов, которые были набраны для 4-летнего последующего наблюдения, 825 субъектов не имели МетС на исходном уровне.Больше мужчин имели MetS по сравнению с женщинами ( P <0,05). Как и ожидалось, у субъектов с MetS на исходном уровне было больше неблагоприятных факторов риска, чем у пациентов без MetS, включая более высокий ИМТ, возраст, холестерин ЛПНП и индекс инсулинорезистентности (по определению HOMA-IR), а также параметры, определяющие MetS, такие как окружность талии, уровень глюкозы натощак, триглицериды, гипертония и низкий уровень холестерина ЛПВП. Субъекты с метаболическим синдромом также имели более высокий уровень вчСРБ и более низкие уровни адипонектина в сыворотке (оба P <.001). Кроме того, концентрация RA была значительно ниже у субъектов с MetS по сравнению с субъектами без MetS ( P <0,001, с поправкой на пол). Уровень RA постепенно снижался с увеличением количества компонентов MetS (Рисунок 1). Уровни RA постепенно снижались от субъектов без MetS (2,33 нг / мл) до пациентов со всеми пятью компонентами MetS (0,81 нг / мл). Рисунок 1. Концентрация RA в сыворотке в зависимости от количества компонентов MetS на исходном уровне. Значения P были рассчитаны на основе модели общей линейной регрессии с множеством переменных. Ковариаты были скорректированы по возрасту, полу, ИМТ и HOMA-IR. Рисунок 1. Концентрация RA в сыворотке в зависимости от количества компонентов MetS на исходном уровне. Значения P были рассчитаны на основе модели общей линейной регрессии, скорректированной с несколькими переменными. Ковариаты были скорректированы по возрасту, полу, ИМТ и HOMA-IR. Таблица 1.Базовые характеристики субъектов с MetS или без него на исходном уровне
Базовые характеристики субъектов с или без него на исходном уровне
Множественный пошаговый логистический регрессионный анализ факторов MetS на исходном уровне
На исходном уровне было обнаружено, что РА с поправкой на возраст и пол имеет значительную обратную корреляцию с множеством неблагоприятных метаболических параметров (таблица 3). RA в сыворотке отрицательно коррелировал с уровнем глюкозы в плазме натощак ( r = -0,185, P <0,001), инсулином ( r = -0,126, P = 0,014) и HOMA-IR ( r ). = -0,208, P <0,001). Кроме того, уровень RA в сыворотке обратно пропорционален общему холестерину ( r = -0.102, P = 0,023), триглицериды ( r = -0,194, P <0,001) и холестерин ЛПНП ( r = -0,152, P = 0,009). Участники с более высоким RA в сыворотке имели более высокий уровень холестерина ЛПВП ( r = 0,177, P <0,001). Наблюдалась обратная корреляция между RA и систолическим АД ( r = -0,131, P = 0,010), но не было обнаружено значимой связи между RA и диастолическим АД ( r = -0,054, P =.087). РА был положительно связан с уровнем адипонектина ( r = 0,155, P = 0,008). Кроме того, более высокий уровень RA сильно коррелировал с более низкими окислительными маркерами, такими как 8-iso PGF2α ( r = -0,191, P <0,001) и сниженными провоспалительными молекулами, включая hsCRP ( r = -0,167, P = 0,005). Таблица 3.скорректированных по нескольким параметрам коэффициентов корреляции Спирмена RA и метаболических факторов риска на исходном уровне a
испытуемых, у которых не было встреченных пациентов Исходно у 143 субъектов развился МетС после 4-летнего наблюдения. Исходная концентрация РА была значительно ниже у субъектов, у которых через 4 года развился метаболический синдром: 1,18 нг / мл (межквартильный диапазон 1,02–1,45 нг / мл) против 1,65 нг / мл (межквартильный диапазон 1.36–1,97 нг / мл) у субъектов без метаболического синдрома (с поправкой на пол P <0,001). Как показано в таблице 4, частота встречаемости MetS и каждого компонента была значительно снижена в соответствии с квартилями уровня RA в сыворотке. OR (95% ДИ) MetS составлял 3,52 (2,73, 4,44) в самом высоком квартиле RBP4 по сравнению с нижним квартилем после учета возраста, пола, ИМТ, курения, употребления алкоголя, семейного анамнеза сердечно-сосудистых заболеваний и диабета. Уровень RA также был обратно связан с компонентами MetS, включая центральное ожирение, гипертриглицеридемию, снижение холестерина ЛПВП и гипергликемию.Ни одна из этих ассоциаций не была значительно ослаблена после дальнейшей корректировки на адипокины и маркеры окислительного стресса и воспаления. Таблица 4.Частота встречаемости MetS и ее компонентов по квартилям сывороточного RA после 4-летнего наблюдения
Частота встречаемости MetS и его компонентов по квартилям сывороточного RA после 4-летнего наблюдения
В анализе множественной пошаговой логистической регрессии исходный RA ( P <.001) и HOMA-IR ( P = 0,001) были единственными независимыми предикторами развития MetS на 4 год (таблица 5). HOMA-IR положительно коррелировал с инцидентным MetS, тогда как RA был обратно коррелирован с инцидентным MetS. Субъекты с наивысшим гендерно-специфическим квартилем исходного RA имели на 46% меньший риск развития метаболического синдрома на 4 году по сравнению с пациентами с RA в самом низком квартиле (OR 0,54, 95% ДИ 0,42–0,65, P <0,001). ) после корректировки на BMI и HOMA-IR.Поправка на статус употребления алкоголя и курения не повлияла ни на один из вышеперечисленных результатов. Таблица 5. Анализ множественной логистической регрессиифакторов, прогнозирующих развитие метаболического синдрома при 4-летнем наблюдении
Множественный логистический регрессионный анализ факторов, прогнозирующих развитие MetS через 4 года наблюдения
ОбсуждениеРанее сообщалось, чтоRA, наиболее изученный метаболит в пути витамина А, играет особую метаболическую роль в дифференцировке адипоцитов in vitro и в индуцированной диетой инсулинорезистентности и ожирении in vivo (25).Однако доказательства, подтверждающие потенциальную роль РА в развитии метаболического синдрома у людей, ограничены. В настоящем исследовании мы представляем первые клинические доказательства, демонстрирующие, что RA в сыворотке крови является важным защитным фактором для развития MetS, независимо от ожирения и инсулинорезистентности. Как наши поперечные, так и проспективные исследования продемонстрировали независимую связь уровня циркулирующего РА со всеми метаболическими факторами риска, включая абдоминальное ожирение, инсулинорезистентность, атерогенную дислипидемию, гипергликемию и гипертензию.Исходный уровень РА предсказал развитие метаболического синдрома в течение 4-летнего периода наблюдения, даже с поправкой на возраст, пол, ИМТ и другие мешающие факторы. Примечательно, что наш анализ множественной логистической регрессии продемонстрировал, что только уровень RA и HOMA-IR были независимыми предикторами MetS в этой когорте, предполагая, что более низкий уровень RA может быть важным защитником этого заболевания у людей. Более того, повышенный риск развития метаболического синдрома, связанный с более низким исходным РА, не зависел от исходного статуса компонентов метаболического синдрома. MetS представляет собой комплекс клинических признаков и наиболее важную особенность, которая представляет собой увеличенное депо висцерального жира в брюшной полости (26). Хотя было показано, что RA ингибирует адипогенез в преадипоцитах (27) и на животной модели с ожирением (28), возможная роль RA на массу тела и жировую массу в популяциях людей все еще неизвестна. Здесь мы продемонстрировали, что более высокий уровень RA в сыворотке достоверно связан с более низким ИМТ в этой популяции. Кроме того, РА был обратно связан с состоянием талии и соотношением талии к бедрам, двумя антропометрическими и простыми измерениями центрального ожирения, которые могут прогнозировать риск сердечно-сосудистых заболеваний и диабета (29).Лица, страдающие ожирением и / или страдающие метаболическим синдромом, демонстрируют характерный дисбаланс своего адипокинового профиля (30, 31). Этот измененный профиль адипокина приводит к глубоким изменениям чувствительности к инсулину и другим биохимическим изменениям метаболитов, делая человека более предрасположенным к метаболическим нарушениям (32, 33). В текущем исследовании мы обнаружили, что высокий уровень РА положительно связан с уровнем адипонектина, ключевого отрицательного модулятора инсулинорезистентности. Таким образом, наши данные предполагают, что RA может улучшить аберрантную продукцию адипокинов и, таким образом, имеет терапевтический потенциал в управлении MetS.Однако влияние RA на клеточный состав жировой ткани, измененную продукцию адипокинов и лежащие в основе молекулярные механизмы необходимо выяснить в будущих исследованиях. Кроме того, наши результаты показали, что высокие уровни RA в сыворотке были связаны с более низким уровнем глюкозы натощак и индексом HOMA. Кроме того, в этой популяции наблюдалась положительная связь между сывороточным RA и концентрацией холестерина ЛПВП, но обратная корреляция с общим холестерином, холестерином ЛПНП и триглицеридами в этой популяции.Мы предполагаем, что влияние РА на концентрацию липидов в крови (особенно холестерина и триглицеридов) может быть опосредовано его ролью в метаболизме жирных кислот печени, который регулирует экспрессию генов, участвующих в метаболизме липидов (34, 35). Системное воспаление, проявляющееся повышенными уровнями в плазме hsCRP и IL-6, является важным предиктором метаболического синдрома (36–38). Настоящее исследование выявило обратную корреляцию между уровнем RA и повышенными воспалительными маркерами, включая hsCRP и IL-6, даже после поправки на ожирение, которые, как было документально подтверждено, играют важную роль в инициации и развитии воспалительных эффектов в жировой ткани. .Таким образом, наши результаты определили провоспалительные маркеры как критическую связь между RA и заболеваемостью MetS. Повышенный окислительный стресс играет важную роль в нарушениях, связанных с метаболическим синдромом (39, 40). В этом исследовании более высокий уровень RA в сыворотке был значительно связан с более низкими концентрациями в сыворотке 8-iso PGF2-α, основных продуктов перекисного окисления ненасыщенных жирных кислот и надежного маркера оксидантного стресса (41). Эти результаты показывают, что более высокий статус RA может предотвратить системное окислительное повреждение.Следовательно, окислительный стресс может представлять собой еще один механизм, с помощью которого высокий статус RA защищается от метаболических нарушений. Тем не менее, следует обратить внимание на некоторые ограничения этого исследования. Во-первых, количество субъектов, у которых развился MetS, было относительно небольшим в течение 4-летнего периода наблюдения. Обратную корреляцию РА с риском метаболического синдрома необходимо подтвердить на более крупных исследуемых популяциях. Кроме того, наши выводы также должны быть подтверждены в других этнических популяциях с другим генетическим и экологическим происхождением.Еще одним ограничением настоящего исследования является то, что статистический анализ не основывался на гипотезах, а был исследовательским по своей природе, чтобы найти значимые факторы в результате применения пошаговых методов. Наконец, сывороточная концентрация RA измерялась только один раз на исходном уровне исследуемой когорты. Таким образом, мы не смогли скорректировать возможные умеренные колебания RA в сыворотке крови во время последующего наблюдения, например, из-за повышенного потребления пищи, богатой витамином A. В заключение, наши результаты позволяют предположить, что снижение уровней РА связано с повышенным риском наличия метаболического синдрома и неблагоприятных значений для компонентов, связанных с метаболическим синдромом.Более того, высокие уровни RA в сыворотке отрицательно связаны с воспалительными маркерами и окислительным стрессом. Наши результаты предполагают потенциальную связь между RA и заболеваемостью MetS. Поскольку есть доказательства этнических различий в эффекте РА и ограниченные данные об ассоциации РА с MetS у азиатов, наши данные дают новое понимание природы этой связи среди азиатов. Тем не менее, преимущества витамина А в отношении метаболического синдрома и связанных с ним заболеваний, таких как диабет 2 типа, необходимо подтвердить в будущих проспективных исследованиях и клинических испытаниях. БлагодарностиАвторы сделали следующие работы: Ю.Л. и H.C. провел исследование. Y.L., H.C., D.M., J.F., J.S., Y.Z. и D.L. просмотрел / отредактировал рукопись. Y.L., H.C., D.M., J.F., J.S., Y.Z. и D.L. проанализировали данные. M.X. участвовал в разработке эксперимента и рукописи, руководил всем проектом и написал рукопись. Работа поддержана Комитетом по науке и технологиям Гуанчжоу (грант 201510010220). Раскрытие информации: авторам нечего раскрывать. Сокращения
Каталожные номера1.Ford ES ,Giles WH ,Dietz WH .Распространенность метаболического синдрома среди взрослых в США: результаты третьего Национального исследования здоровья и питания .JAMA .2002 ;287 :356 —359 . 2.Eckel RH ,Grundy SM ,Zimmet PZ .Метаболический синдром .Ланцет .2005 ;365 :1415 —1428 . 3.Группа экспертов по обнаружению, оценке и лечению повышенного холестерина в крови у взрослых .Краткое изложение третьего отчета Группы экспертов Национальной образовательной программы по холестерину (NCEP) по обнаружению, оценке и лечению высокого уровня холестерина в крови у взрослых (Группа лечения взрослых III) .JAMA .2001 ;285 :2486 —2497 .4.Wang L ,Kong L ,Wu F ,Bai Y ,Burton R .Профилактика хронических заболеваний в Китае .Ланцет .2005 ;366 :1821 —1824 . 5.Ян G ,Ван Y ,Zeng Y и др. .Быстрый переход к здоровью в Китае, 1990–2010 гг .: результаты исследования глобального бремени болезней, 2010 г. .Ланцет .2013 ;381 :1987 —2015 .6.He J ,Gu D ,Wu X и др. .Основные причины смерти мужчин и женщин Китай .N Engl J Med .2005 ;353 :1124 —1134 .7.Xu Y ,Wang L ,He J и др..2010 Китайская группа по надзору за неинфекционными заболеваниями. Распространенность диабета и борьба с ним у взрослых китайцев .JAMA .2013 ;310 :948 —959 .8.Салас-Сальвадо J ,Гуаш-Ферре M ,Bulló M ,Sabaté J .Орехи в профилактике и лечении метаболического синдрома .Ам Дж. Клин Нутр .2014 ;100 :399S —407S .9.Rumawas ME ,Meigs JB ,Dwyer JT ,McKeown NM ,Jacques PF .Средиземноморский режим питания, снижение риска метаболического синдрома и заболеваемость в когорте потомков Фрамингема .Ам Дж. Клин Нутр .2009 ;90 :1608 —1614 .10.Carpentier YA ,Portois L ,Malaisse WJ .n-3 Жирные кислоты и метаболический синдром .Ам Дж. Клин Нутр .2006 ;83 :1499S —1504S .11.Рис BH ,Cifelli CJ ,Pikosky MA ,Miller GD .Молочные компоненты и факторы риска кардиометаболического синдрома: последние данные и возможности для будущих исследований .Adv Nutr .2011 ;2 :396 —407 .12.Росс SA ,McCaffery PJ ,Drager UC ,De Luca LM .Ретиноиды в эмбриональном развитии .Physiol Ред. .2000 ;80 :1021 —1054 . 13.Петкович ПМ .Метаболизм ретиноевой кислоты .J Am Acad Dermatol .2001 ;45 :S136 —S142 . 14.Blomhoff R ,Blomhoff HK .Обзор метаболизма и функции ретиноидов .Дж Нейробиол .2006 ;66 :606 —630 . 15.Шульман AI ,Мангельсдорф DJ .Гетеродимеры рецепторов ретиноида X в метаболическом синдроме .N Engl J Med .2005 ;353 :604 —615 . 16.Heyman RA ,Mangelsdorf DJ ,Dyck JA ,Stein RB ,Eichele G .Ретиноевая кислота является лигандом с высоким сродством к рецептору ретиноида X .Ячейка .1992 ;68 :397 —406 . 17.Зиузенкова O ,Plutzky J .Метаболизм ретиноидов и ответы ядерных рецепторов: новый взгляд на скоординированную регуляцию комплекса PPAR-RXR .FEBS Lett .2008 ;582 :32 —38 . 18.Plutzky J .Транскрипционный комплекс PPAR-RXR в сосудистой сети: энергия на балансе .Circ Res .2011 ;108 :1002 —1016 .19.Fu M ,Sun T ,Bookout AL ,Downes M ,Yu RT .Атлас ядерных рецепторов: 3T3-L1 adipogenesis .Мол Эндокринол .2005 ;19 :2437 —2450 .20.Modak T ,Mukhopadhaya A .Влияние цитраля, встречающейся в природе антиадипогенной молекулы, на модель ожирения с энергоемкой диетой .Индийский J Pharmacol .2011 ;43 :300 —305 .21.Американская диабетическая ассоциация .Диагностика и классификация сахарного диабета. Американская диабетическая ассоциация .Уход за диабетом .2007 ;30 (доп. 1 ):S42 —S47 . 22.Friedewald WT ,Levy RI ,Fredrickson DS .Оценка концентрации холестерина липопротеидов низкой плотности в плазме без использования препаративной ультрацентрифуги .Clin Chem .1972 ;18 :499 —502 . 23.Лю Y ,Li D ,Zhang Y ,Sun R ,Xia M .Антоцианин увеличивает секрецию адипонектина и защищает от эндотелиальной дисфункции, связанной с диабетом .Am J Physiol Endocrinol Metab .2014 ;306 :E975 —E988 .24.Grundy SM ,Cleeman JI ,Daniels SR ,Donato KA ,Eckel RH .Диагностика и лечение метаболического синдрома: научное заявление Американской кардиологической ассоциации / Национального института сердца, легких и крови .Тираж .2005 ;112 :2735 —2752 . 25.Berry DC ,DeSantis D ,Soltanian H ,Croniger CM ,Noy N .Ретиноевая кислота активирует гены преадипоцитов, блокируя адипогенез и подавляя ожирение, вызванное диетой .Диабет .2012 ;61 :1112 —1121 . 26.Kim S ,Cho B ,Lee H и др. .Распространение висцеральной и подкожной жировой ткани брюшной полости и метаболический синдром среди корейского населения .Уход за диабетом .2011 ;34 :504 —506 . 27.Фелипе F ,Bonet ML ,Ribot J ,Palou A .Модуляция экспрессии резистина ретиноевой кислотой и статусом витамина А .Диабет .2004 ;53 :882 —829 . 28.Берри ДЦ ,Ной N .Полностью транс-ретиноевая кислота подавляет ожирение и инсулинорезистентность путем активации рецептора β / δ, активируемого пролиферацией пероксисом, и рецептора ретиноевой кислоты .Mol Cell Biol .2009 ;29 :3286 —3296 . 29.Goh LG ,Dhaliwal SS ,Welborn TA ,Lee AH ,Della PR .Антропометрические измерения общего и центрального ожирения и прогнозирование риска сердечно-сосудистых заболеваний у женщин: перекрестное исследование .BMJ Открыть .2014 ;4 :e004138 .30.Choi KM ,Yannakoulia M ,Park MS и др. .Концентрация связывающего жирные кислоты белка адипоцитов, ретинол-связывающего белка 4 и адипонектина в отношении развития метаболического синдрома у корейских мальчиков: 3-летнее проспективное когортное исследование .Ам Дж. Клин Нутр .2011 ;93 :19 —26 .31.Kim JY ,Ahn SV ,Yoon JH и др. .Проспективное исследование сывороточного адипонектина и инцидентного метаболического синдрома: исследование ARIRANG .Уход за диабетом .2013 ;36 :1547 —1553 . 32.Winer JC ,Zern TL ,Taksali SE ,Dziura J ,Cali AM .Адипонектин при ожирении у детей и подростков и его связь с воспалительными маркерами и компонентами метаболического синдрома .Дж. Клин Эндокринол Метаб .2006 ;91 :4415 —4423 . 33.Xu A ,Tso AW ,Cheung BM ,Wang Y ,Wat NM .Уровни циркулирующих белков жирных кислот и адипоцитов предсказывают развитие метаболического синдрома: 5-летнее проспективное исследование .Тираж .2007 ;115 :1537 —1543 . 34.Manolescu DC ,Sima A ,Bhat PV .Полностью транс-ретиноевая кислота снижает концентрацию ретинол-связывающего белка 4 в сыворотке и увеличивает чувствительность к инсулину у мышей с диабетом .J Nutr .2010 ;140 :311 —316 .35.Bonet ML ,Ribot J ,Palou A .Обмен липидов в тканях млекопитающих и его контроль с помощью ретиноевой кислоты .Biochim Biophys Acta .2012 ;1821 :177 —189 . 36.Romeo GR ,Lee J ,Shoelson SE .Метаболический синдром, инсулинорезистентность и роль механизмов воспаления и терапевтические цели .Артериосклер Тромб Vasc Biol .2012 ;32 :1771 —1776 .37.Ridker PM ,Buring JE ,Cook NR ,Rifai N .С-реактивный белок, метаболический синдром и риск сердечно-сосудистых событий: 8-летнее наблюдение за 14719 первоначально здоровыми американскими женщинами .Тираж .2003 ;107 :391 —397 0,38.Wild SH ,Byrne CD ,Tzoulaki I ,Lee AJ ,Rumley A .Метаболический синдром, гемостатические и воспалительные маркеры, цереброваскулярные заболевания и заболевание периферических артерий: Эдинбургское исследование артерий .Атеросклероз .2009 ;203 :604 —609 . 39.Furukawa S ,Fujita T ,Shimabukuro M ,Iwaki M ,Yamada Y .Повышенный окислительный стресс при ожирении и его влияние на метаболический синдром .Дж. Клин Инвест .2004 ;114 :1752 —1761 .40.Джеймс AM ,Коллинз Y ,Логан A ,Мерфи MP .Митохондриальный оксидативный стресс и метаболический синдром .Trends Endocrinol Metab .2012 ;23 :429 —434 .41.Pratico D .F (2) -изопростаны: чувствительные и специфические неинвазивные показатели перекисного окисления липидов in vivo .Атеросклероз .1999 ;147 :1 —10 .Авторские права © 2016 Эндокринологическое общество .
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

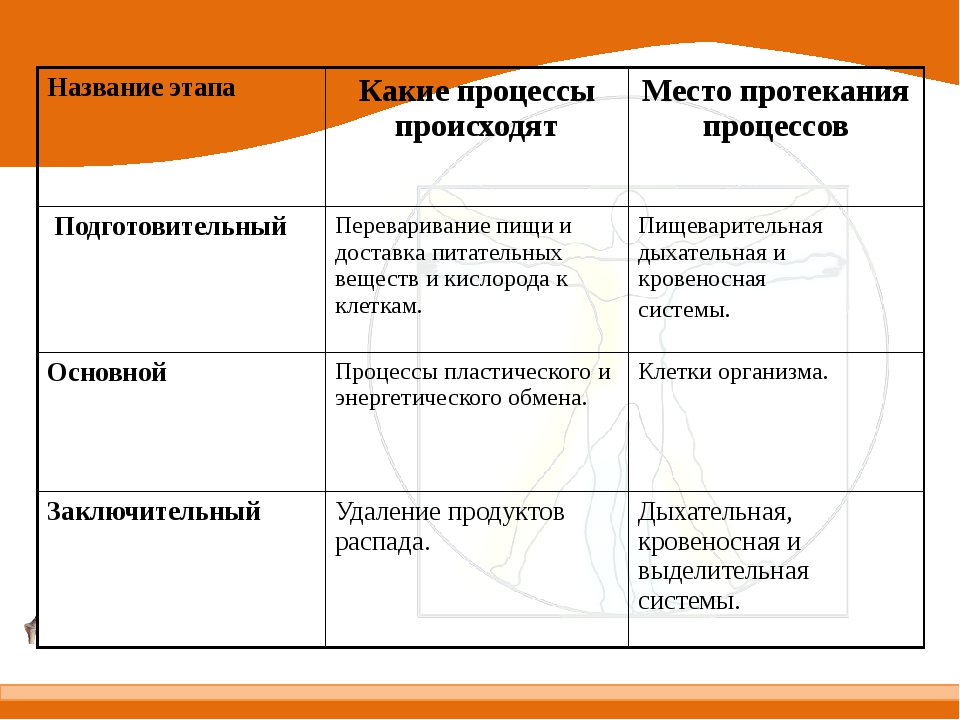

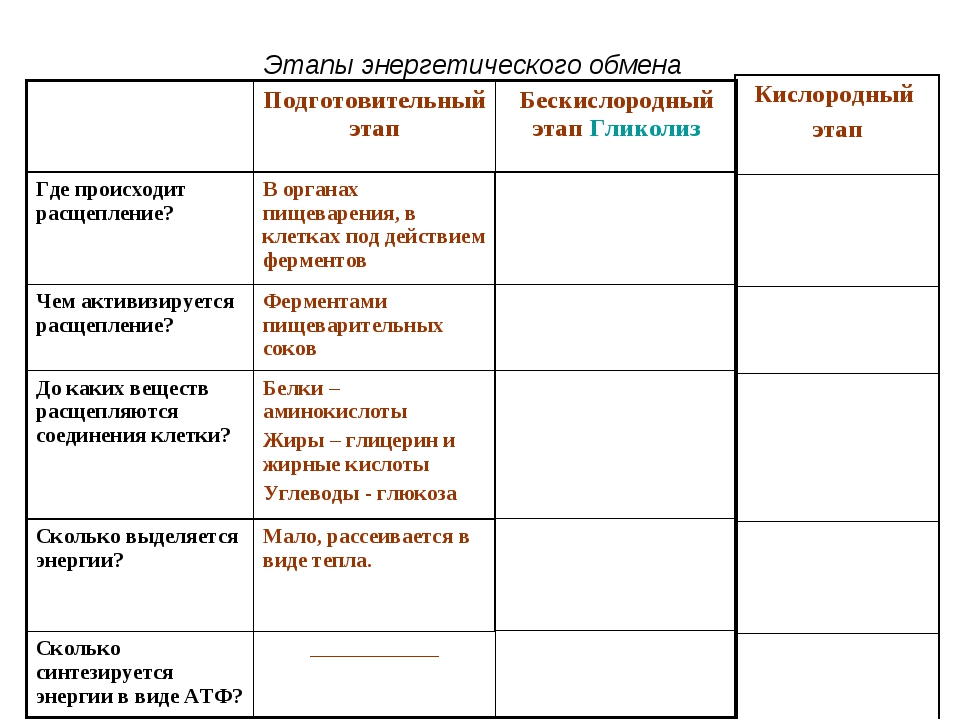 Предложите различные ассоциации.
Предложите различные ассоциации.