Меланин вырабатывается: Не хватает меланина. Почему седеют волосы
Не дайте украсть свой сон
Мелатонин называют гормоном сна и долгой жизни. Удивительно: вещество, открытое почти 60 лет назад, до сих пор остается предметом научных дискуссий, его свойства и влияние на организм до конца не изучены, а потому обрастают множеством мифов.Мелатонин вырабатывается в эпифезе — шишковидной железе. Эта часть головного мозга в среднем за сутки вырабатывает до 30 микрограммов гормона сна, выполняющего множество функций: он защищает нас от стрессов, преждевременного старения, депрессий и даже от раковых заболеваний. Свое второе название мелатонин получил не случайно: он действительно является нашими внутренними часами, благодаря которым ночью хочется спать, а утром — просыпаться. Именно в темное время суток вырабатывается практически весь суточный запас этого гормона. На пик процесс выходит к полуночи и продолжается приблизительно до 4 утра. Замечали, как постепенно с вечера и все ближе к ночи нас одолевает дремота и начинает клонить в сон? Это в организме начинается синтез мелатонина, который обеспечивает засыпание, регулирует продолжительность сна и его качество. Потому мы так остро ощущаем на себе смену часовых поясов: сбиваются наши внутренние часы, организм пытается подстроиться к новому времени дня и ночи. Оттого и нарушаются ритмы выработки мелатонина, а мы ощущаем проблемы со сном, настроением и аппетитом.
— Мелатонин по праву можно называть гормоном современности, — считает профессор кафедры эндокринологии БГМУ, доктор медицинских наук Алла Шепелькевич.
— Ведь раньше человек жил в большей взаимосвязи с природой, подчиняясь ее ритмам: ложился спать, когда стемнеет, вставал с первым солнцем. Сегодня эти механизмы стали нарушаться, в том числе из–за перелетов, стрессов, работы в ночное время суток. А ведь уже давно доказано, что такой образ жизни очень сказывается на здоровье человека, способствуя развитию сердечных патологий, онкозаболеваний, сахарного диабета…
Ведь неспроста же говорят, что сон — лучшее лекарство. Выспавшийся и отдохнувший человек всегда чувствует себя здоровее. Пока мы спим, мелатонин, подобно ремонтной бригаде, по кирпичику укрепляет наш организм, лечит все поломки и восстанавливает силы. В этот момент активируются антиоксидантные и иммуномоделирующие свойства гормона сна. Он препятствует выработке активных радикалов, а значит, защищает нас от старения, рака и сердечных заболеваний. К слову, уровень мелатонина оказывает влияние и на снижение гормонов стресса.
Выспавшийся и отдохнувший человек всегда чувствует себя здоровее. Пока мы спим, мелатонин, подобно ремонтной бригаде, по кирпичику укрепляет наш организм, лечит все поломки и восстанавливает силы. В этот момент активируются антиоксидантные и иммуномоделирующие свойства гормона сна. Он препятствует выработке активных радикалов, а значит, защищает нас от старения, рака и сердечных заболеваний. К слову, уровень мелатонина оказывает влияние и на снижение гормонов стресса.
Многие свойства мелатонина пока еще пристально изучаются наукой. К примеру, не до конца понятны его противоопухолевые механизмы. Но уже точно известно, что такими свойствами гормон сна безусловно обладает. Ученые заметили: у женщин, работающих в ночные смены, риск онкопатологий возрастает на 40 — 60%. Весьма показательны эксперименты на животных. Скажем, когда мышам искусственно увеличили длину светлого времени суток, их продолжительность жизни сократилась в среднем на 20%… Также замечено, что мелатонин сказывается не только на суточных ритмах, но и на реакции организма на смену времен года. Стоит увеличиться солнечному свету и долготе дня, как снижается и уровень мелатонина. Тогда многие млекопитающие, ведущие дневной образ жизни, приступают к поиску партнеров. Подобную закономерность ученые выявили и у людей: половое влечение в короткие дни года значительно ниже, чем в длинные. Необходим мелатонин и для нормального протекания беременности. Именно благодаря его помощи регулируется обновление клеток плаценты.
Примерно к 20 годам синтез мелатонина в организме нормализуется, а уже около 40 — начинает снижаться. С возрастом ослабевает иммунная функция, нарушается сон. И нехватка мелатонина — одна из причин. Однако заниматься самолечением и бросаться на поиски гормона сна не стоит. Даже ученые не могут посоветовать ничего лучшего, чем просто соблюдать нормы физиологии, заложенные природой. Проще говоря, прислушиваться к своим биологическим часам, не путая день с ночью. И обязательно следовать универсальной схеме распорядка дня, где 8 часов должно отводиться на работу, 8 — на отдых и столько же — на сон.

Секреты хорошего сна
Организму будет привычнее засыпать и просыпаться в одно и то же время — соблюдайте режим дня.
То, как прошел ваш день, обязательно скажется на сне. Хорошо влияют на него прогулки на свежем воздухе, расслабляющие ванны, чай с ромашкой.
Спать надо при выключенном свете, с задернутыми шторами. Не засыпайте под телевизор и не злоупотребляйте кофе — так вы не сможете быстро успокоиться и уснуть.
Старайтесь лечь спать не позже полуночи. Ведь именно на это время приходится пик выработки мелатонина. Если вы все же засиделись допоздна, то комнату лучше освещать не очень яркой настольной лампой.
Кстати
Во многих продуктах также содержится мелатонин. Есть он в незначительных дозах в бананах, какао, мясе индейки, бобовых и соевых. Однако если даже усиленно налегать на них, восполнить серьезную нехватку мелатонина вряд ли удастся: основные его запасы производятся самим организмом ночью во время сна.
Ольга Савицкая
Советская Белоруссия, 19 января 2017
«Волшебный гормон». Для чего организму нужен мелатонин? | Советы | ЗДОРОВЬЕ
Руководитель отдела канцерогенеза и онкогерантологии НИИ онкологии им. Петрова, профессор Владимир Анисимов рассказал SPB.AIF.RU, как и зачем нужно дружить с этим «волшебным» гормоном.
С полуночи до четырёх
SPB.AIF.RU: – Владимир Николаевич, в первую очередь объясните: что такое мелатонин? Откуда он берётся?
Владимир Анисимов: – Он вырабатывается в эпифизе – шишковидной железе, придатке головного мозга. Этот гормон, как дирижёр в большом оркестре, участвует в синхронизации биоритмов и всех процессов в организме. Не будет мелатонина – всё пойдёт вразнобой. Также он комплексно влияет на гормональную и иммунную систему. Устраняет депрессию, тревожность, нормализует сон. И значительно замедляет старение.
– Да, с полуночи до трёх-четырёх часов. Причём не обязательно во сне, главное – в темноте. Если в вашей спальне в это время горит свет, вы сидите у компьютера или телевизора, работаете, гуляете – организм столь необходимого ему мелатонина не получает. Это со временем провоцирует преждевременное старение, психические заболевания, нарушение обмена веществ, ожирение и даже онкологию.
Причём не обязательно во сне, главное – в темноте. Если в вашей спальне в это время горит свет, вы сидите у компьютера или телевизора, работаете, гуляете – организм столь необходимого ему мелатонина не получает. Это со временем провоцирует преждевременное старение, психические заболевания, нарушение обмена веществ, ожирение и даже онкологию.
Вот показательный пример: на Аляске провели исследование и выяснили, что за последние 30 лет число больных раком в этом регионе выросло в три раза. Ломали голову: почему? Выяснилось – из-за постоянного доступа к свету. Раньше эскимосы в своих жилищах использовали лучину, керосиновую лампу. Сейчас – электрическое освещение.
Вообще, чем дальше от экватора, тем больше потребление электроэнергии и выше заболеваемость раком. Израильтяне, например, несколько лет назад составили карту освещённости своей страны и увидели, что она как под копирку совпадает с картой заболеваемости женщин раком молочной железы! После этого они провели аналогичную проверку в 164 странах, и результаты снова совпали.
– Но как недостаток гормона может провоцировать рак?
– Происходит снижение иммунитета и нарушение налаженного ритма организма. Не восстанавливаются молекулы ДНК, которые повреждаются вследствие воздействия канцерогенов. Ну, а провоцирующих факторов может быть множество – генетическая предрасположенность, ультрафиолет, вредная пища, выхлопные газы, плохая экология и так далее.
Бананы, орехи, сыр
– Ещё как. Все околополярные субарктические регионы, в том числе Петербург, подвержены избыточному освещению. В мае-июне это белые ночи. В остальное время – ночной световой режим, когда улицы города освещены фонарями, рекламами, витринами магазинов. Всё это негативно сказывается на здоровье.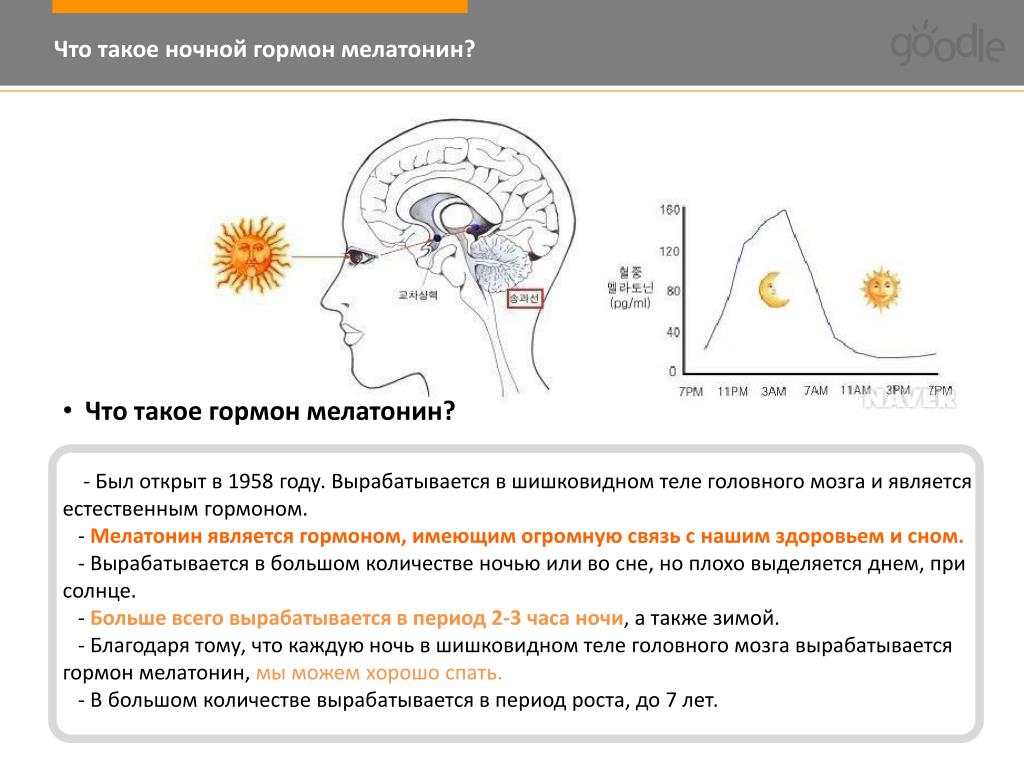 Особенно страдают ночные и сменные работники – медсёстры, полицейские, таксисты, продавцы магазинов, лётчики. Риск рака, сахарного диабета, язвы желудка, ожирения у них значительно выше, чем у тех, кто трудится днём.
Особенно страдают ночные и сменные работники – медсёстры, полицейские, таксисты, продавцы магазинов, лётчики. Риск рака, сахарного диабета, язвы желудка, ожирения у них значительно выше, чем у тех, кто трудится днём.
– Но не работать ночью тоже нельзя!
– Во-первых, нужно всё равно стараться находить время для отдыха ночью — здоровье дороже. Во-вторых, употреблять продукты, которые содержат мелатонин – бананы, грецкие и миндальные орехи, тыквенные семечки, сыр, кукурузу, мясо индейки, курицы, рис. Также я бы очень рекомендовал принимать препараты, содержащие мелатонин, они продаются в любой аптеке. Кстати, исследования нашего института показали, что после операций по удалению опухолей желудка и толстой кишки безрецидивный период у пациентов, которые принимали мелатонин, увеличивается на 30%.
– Какой свет – самый вредный?
– Бело-голубой, который излучают люминесцентные и галогенные лампы – он в 4-5 раз сильнее подавляет выработку мелатонина, чем свет от обычных электрических лампочек. Наиболее безвредное излучение – красное: длина его волны такова, что он практически не вредит нашему здоровью. Поэтому в квартире желательно использовать красные ночники.
– Ночью для поддержания мелатонина необходимо находиться в темноте. А как же днём?
– Днём как раз нужно больше света. Чем больше контраст, тем сильнее выработка гормона ночью. А многие ведь у нас любят в светлое время суток занавесить окна шторами, тюлем. Мой совет: следуйте природе. Вставайте с солнышком, побольше находитесь на свежем воздухе и ложитесь не позже полуночи. Вы сами почувствуете, как улучшится ваше здоровье.
Сага о мелатонине. Почему нужно ложится спать до 23:00 ночи и вставать до 7:00?
Не секрет, что все живые организмы на планете Земля живут по циркадным ритмам циклические (колебаниям интенсивности различных биологических процессов, связанных со сменой дня и ночи). Этот термин сравнительно недавно вошел в лексикон научного мира. Но еще во времена Александра Македонского было описано изменение положения листьев в течение дня у тамаринда (растение семейства бобовых). Человеческое тело также целиком подчиняется природным биоритмам.
Этот термин сравнительно недавно вошел в лексикон научного мира. Но еще во времена Александра Македонского было описано изменение положения листьев в течение дня у тамаринда (растение семейства бобовых). Человеческое тело также целиком подчиняется природным биоритмам.
В зависимости от времени суток в организме повышается уровень одних гормонов и снижается уровень других. Гормоны отвечают за наше настроение, аппетит, активность или вялость. Именно от соответствия природным ритмам правильного чередования сна и бодрствования зависят хорошее самочувствие, правильное функционирование организма и нормальный уровень гормонов в организме человека.
Сейчас всё чаще и чаще звучат голоса ученных, которые утверждают, что наши предки не зря вставали с восходом солнца и ложились с его закатом.
В современном мире очень распространено деление людей на «сов» и «жаворонков». Жаворонки встают рано, к вечеру достаточно устают и засыпают до 22-23 часов. А совы, напротив, любят лечь спать, как минимум, после 24 часов, а встать уже после обеда. Таким образом, «совы» спят, когда угодно, только не в отведенное природой для этого время — ночью. А ведь, совершенно ясно, что, если человек хронически не спит по ночам, он просто не может быть здоровым.
Для каждой возрастной группы людей есть свои нормы сна:
— новорожденные (1- 2 месяца): от 11 часов до 18 часов;
— младенцы (3-11 месяцев): от 10 часов до 14 часов;
— дети от года до пяти: от 12 до 14 часов;
— дети от 5 до 12 лет: от 10 до 11 часов;
— подростки от 12 до 18 лет: от 8,5 до 9,5 часов;
— взрослые люди от 18 лет: от 7,5 до 8,5 часов.
Доказанный факт: для организма взрослого человека (среднего возраста) одинаково вредно спать, как меньше 7,5 часов, так и больше 8,5 часов. Чем больше человек пренебрегает сном, тем сильнее возрастает риск возникновения серьезных заболеваний. Например, люди, которые спят меньше 7 часов в сутки, гораздо чаще страдают простудными заболеваниями, лишним весом, ожирением и депрессией. А все это, как мы знаем, благоприятная почва для развития таких опасных заболеваний, как диабет 2-го типа, сердечно-сосудистых патологий и даже рака!
А все это, как мы знаем, благоприятная почва для развития таких опасных заболеваний, как диабет 2-го типа, сердечно-сосудистых патологий и даже рака!
Если Вы постоянно ложитесь спать позже 23 часов ночи и/или встаете позже 7 часов утра, рано или поздно у вас появятся необратимые проблемы со здоровьем. Поэтому, крайне важно, отрегулировать свой распорядок дня, таким образом, чтобы он соответствовал природным ритмам.
Давайте раз и навсегда разберемся, как работают человеческие био-часы, и почему так важно им подчинятся. Дело в том, что нашим организмом, а именно эпифизом (шишковидной железой) вырабатывается очень важный гормон – мелатонин. Это удивительное вещество вырабатывается только когда мы спим в полной темноте. Именно он управляет циркадными ритмами человека. За ночь выделяется около 70 процентов суточной нормы мелатонина. Интересной особенностью является то, что выработка мелатонина в организме происходит в промежутке между 23 часов и 3:00 ночи. Эпифиз начинает вырабатывать мелатонин только в полной темноте, даже небольшая лампочка, горящая в комнате ночью, существенно снижает уровень мелатонина. Недостаток мелатонина способен привести наш организм к плачевным последствиям. Ведь данный гормон, играет ключевую роль в нашем теле, выполняя целый набор незаменимых функций:
1) замедляет процессы старения в организме;
2) влияет на уровень гормона роста;
3) помогает бороться со стрессом;
4) уменьшает жировую прослойку в теле;
5) увеличивает размер мышц;
6) обладает противораковыми свойствами;
7) поддерживает иммунитет, либидо;
8) контролирует аппетит.
Когда свет перестает попадать на сетчатку глаза, мозг дает сигнал на выработку мелатонина. Гормон выбрасывается в кровь, проникает в каждую клетку организма, температура тела падает, и организм начинает засыпать. В этот момент в гипофизе начинают вырабатываться гормоны эндорфины и экефалины. Это опиоидные гормоны, обладающие наркотическим действием, поэтому процесс засыпания сопровождается приятными ощущениями. После двух часов ночи уровень мелатонина в крови начинает снижется, а уже в три-четыре часа ночи надпочечники начинают вырабатывать гормон кортизол, который возбуждает нервную систему (приводит к повышению давления, учащению сердечных сокращений и повышению тонуса сосудов). Пика своей концентрации в крови кортизол достигает к шести – семи утра. Таким образом природой задумано, чтобы приблизительно в это время человек просыпался. Если этого не происходит, то кортизол из гормона бодрости и пробуждения превращается в гормон стресса.
Это опиоидные гормоны, обладающие наркотическим действием, поэтому процесс засыпания сопровождается приятными ощущениями. После двух часов ночи уровень мелатонина в крови начинает снижется, а уже в три-четыре часа ночи надпочечники начинают вырабатывать гормон кортизол, который возбуждает нервную систему (приводит к повышению давления, учащению сердечных сокращений и повышению тонуса сосудов). Пика своей концентрации в крови кортизол достигает к шести – семи утра. Таким образом природой задумано, чтобы приблизительно в это время человек просыпался. Если этого не происходит, то кортизол из гормона бодрости и пробуждения превращается в гормон стресса.
Неслучайно, один из действенным способом борьбы со стрессом является ранний подъем и зарядка.
Как бы далеко не заходил технический прогресс и как бы не облегчал нам жизнь, человеческое тело продолжает оставаться частью природы и для того, чтобы сохранить здоровье и продлить молодость должно подчинятся её законам. Мы мало чем отличаемся от наших предков генетически, но гораздо больше расходимся с природными био-ритмами. Может быть, именно из-за этого сейчас так много людей больных физически и даже психически. А ведь поддерживать гармонию своего тела не так уж и сложно. И на вопрос, как повысить мелатонин в организме, мы уже знаем ответ – для начала надо начать вовремя засыпать до 23 часов и просыпаться раньше 7 утра. И Вы заметите, как многие проблемы со здоровьем уйдут сами собой. Начните менять свою жизнь к лучшему уже сегодня вечером, не откладывайте здоровье на потом!
Может ли мелатонин влиять на тяжесть течения заболевания COVID-19?
Может ли мелатонин влиять на тяжесть течения заболевания COVID-19?
Огромное количество информации о лечении и профилактике, лекарствах и биологически активных добавках для защиты от COVID-19, болезни, вызываемой новым коронавирусом, циркулирует в интернете, СМИ, социальных сетях по всему миру.
Мы знаем об этом вирусе всего несколько месяцев, но ученые активно работают над тем, чтобы лучше понять, как этот вирус действует на наш организм, а также найти способы лечения.
Одним из препаратов, применяемых для лечения, который в настоящее время исследуется и демонстрирует некоторые положительные эффекты, является мелатонин.
Хотя в настоящее время отсутствует достаточное количество научных доказательств, подтверждающих, что мелатонин может защитить от серьезных последствий COVID-19, однако есть признаки того, что мелатонин может влиять на тяжесть заболевания, чрезмерный иммунный ответ и последующее серьезное повреждение легких, которое присутствует у большинства пациентов с тяжелым течением новой коронавирусной инфекции.
Мелатонин — это гормон, наиболее известный как помощник сна. Мелатонин регулирует сон, воздействуя на биологические часы организма (циклы сна и бодрствования).
Мелатонин вырабатывается в нашем организме преимущественно шишковидной железой в головном мозге естественным путем. Он также доступен в форме биологически активных добавок. Научные исследования показывают, что такие добавки мелатонина могут благотворно влиять на циклы сна и бодрствования.
Природный мелатонин вырабатывается под влиянием света. Наш мозг получает световые сигналы через сетчатку глаза, которые затем передаются по зрительному нерву в главные биологические часы мозга, супрахиазматическое ядро, которое посылает соответствующий сигнал шишковидной железе, отвечающей за выработку гормона.
Как и большинство гормонов, мелатонин вырабатывается в соответствии с ежедневным циркадным ритмом. Производство мелатонина увеличивается в темное время суток и подавляется под воздействием света. Уровень мелатонина начинает значительно расти около 9 часов вечера и, достигая своего пика в течение ночи, падает до самого низкого уровня утром.
Связь мелатонина с циклами света и темноты — это основная причина, по которой ночное освещение может быть вредным для нашего сна и здоровья.
Также мы знаем, что с возрастом способность организма вырабатывать мелатонин ночью, снижается. Некоторые ученые предполагают, что возможная причина низкого распространения COVID-19 у детей связана с естественным высоким уровнем у них мелатонина.
Мелатонин наиболее известен как регулятор сна, но он также играет важную роль в регулировании деятельности нашей иммунной системы. Также мелатонин является сильным антиоксидантом и обладает противовоспалительными свойствами.
Мелатонин сдерживает иммунную активность, влияя на выработку цитокинов – белков, которые действуют как сигналы иммунной системы клеткам организма. Цитокины могут вызывать (провоспалительные цитокины) или ограничивать (противовоспалительные цитокины) воспаление.
Известно, что мелатонин снижает выработку цитокинов, вызывающих воспаление. Также известно, что мелатонин является антиоксидантом, нейтрализующим клетки свободных радикалов и ограничивающим окислительный стресс и повреждения, которые способствуют воспалению.
Провоспалительные цитокины участвуют в развитии воспалительной реакции организма, которая борется с вирусом, бактериями и другими патогенными агентами. Таким образом наш организм защищает себя. Но чтобы этот цитокиновый ответ был полезен, он должен быть пропорционален угрозе. Чрезмерный ответ провоспалительных цитокинов создает опасность для организма и может способствовать распространению вирусной инфекции, а не ослаблять ее. Именно эта чрезмерная воспалительная реакция и связанное с ней распространение вируса, по-видимому, имеют место в наиболее серьезных случаях COVID-19.
COVID-19 является острым респираторным заболеванием, которое в некоторых случаях приводит к исключительно сильному поражению легких. В то время как большинство случаев новой коронавирусной инфекции имеют легкие симптомы, похожие на простуду и грипп, и наносит сравнительно небольшой ущерб молодым и здоровым людям, у пожилых людей и людей с хроническими заболеваниями COVID-19 может привести к тяжелой пневмонии. В наиболее тяжелых случаях коронавирусная инфекция приводит к острому повреждению легких и острому респираторному дистресс-синдрому, из-за которого легкие и дыхательная система не могут поглощать достаточное количество кислорода и распределять его через кровоток. Такие пациенты нуждаются в искусственной вентиляции легких (ИВЛ).
Такие пациенты нуждаются в искусственной вентиляции легких (ИВЛ).
В основе пневмонии и повреждения легких, которыми проявляются тяжелые случаи коронавирусной инфекции, лежит чрезмерная воспалительная реакция собственной иммунной системы организма.
В частности, новый коронавирус, активирует инфламассомы – «датчики» нашей иммунной системы, которые обнаруживают потенциальные угрозы для нашего организма и реагируют на них, вызывая воспаление.
Новый коронавирус активирует специфические инфламассомы, включая NLRP3. Было показано, что именно инфламассомы NLRP3 имеют тесную связь с острым повреждением легких и острым респираторным дистресс-синдромом и являются ключевым триггером избыточного ответа иммунной системы, который может привести к инвалидизирующим и угрожающим жизни поражениям легких.
В ряде научных исследований мелатонин был отмечен как подавляющий действие NLRP3 агент. Было обнаружено, что способность мелатонина подавлять активацию NLRP3, влияет на тяжесть воспалительных реакций, снижает выработку провоспалительных цитокинов, а также уменьшает проникновение иммунных клеток в легкие и, соответственно, уменьшает повреждение тканей легких.
Исследования на мышах, в которых рассматривалось именно влияние мелатонина на острое повреждение легких, продемонстрировали, что мелатонин обеспечивает защиту от наиболее тяжелого повреждения легких благодаря его способности подавлять воспаление с помощью NLRP3.
Именно эта способность мелатонина воздействовать на воспаление наряду с высокой степенью безопасности и пользы для сна, привлекает внимание ученых к мелатонину как к средству, которое может повлиять на иммунный ответ организма при воздействии коронавируса, потенциально снижая тяжесть течения новой коронавирусной инфекции.
Итак, значит ли это, что мы все должны срочно начать принимать мелатонин? Конечно же нет. В настоящее время возможность использования мелатонина при новой коронавирусной инфекции носят характер хоть и весьма многообещающей, но гипотезы.
Если вы хотите использовать добавки мелатонина, обязательно проконсультируйтесь с врачом, особенно если вы относитесь к одной из перечисленных групп: беременные и кормящие женщины, люди с нарушениями свертываемости крови, люди, перенесшие трансплантацию, люди, страдающие депрессией, диабетом, с повышенным артериальным давлением.
Следует помнить, что мелатонин является мощным гормоном, оказывающим влияние на циркадные ритмы и другие физиологические функции организма. При приеме слишком большого количества мелатонина могут наблюдаться такие побочные эффекты, как нарушение циркадных ритмов и циклов сна и бодрствования, сонливость, снижение кровяного давления, головокружение, головная боль, тошнота, боль в желудке, боль в суставах, депрессия, беспокойство, раздражительность.
Лучшее время для приема добавки мелатонина — от 30 минут до 1 часа перед сном – зависит также от хронотипа. Жаворонки должны принимать мелатонин раньше по вечерам, а совы позже.
Чтобы повысить выработку мелатонина в организме без добавок необходимо следовать следующим правилам:
1. Придерживайтесь графика сна с регулярным временем сна и бодрствования, так вы усилите свои циркадные ритмы.
2. Избегайте воздействия искусственного света ночью. Низкая освещенность позволяет организму вырабатывать больше мелатонина. Очки, блокирующие синий свет, помогут вам избежать подавления выработки мелатонина, вызванного воздействием ночного света — без необходимости сидеть в темноте или отказаться от небольшого количества Netflix в конце долгого дня.
3. Создайте комфортную среду для вашего сна, в вашей спальне должно быть прохладно, темно и максимально тихо.
4. Не тренируйтесь и не принимайте пищу непосредственно перед сном, избегайте ситуаций и разговоров, которые могут вывести вас из равновесия.
5. Выделите время для себя: примите ванну, медитируйте, слушайте расслабляющую музыку, используйте успокаивающие и расслабляющие дыхательные техники.
Нехватка мелатонина — Статьи — Золотой Кубок
Мелатонин известен и как «гормон сна»,
и как «гормон красоты». Говорят, что его достаточная выработка способна
продлить жизнь на 15, а то и больше лет. Многие специалисты, врачи, психологи,
тренеры говорят о полезности и важности хорошего здорового сна. Без него
организм становится более подвержен стрессам, появляется усталость, которая не
дает нормально работать, тренироваться, радоваться жизни. А также снижается
иммунитет и ускоряются процессы старения.
Говорят, что его достаточная выработка способна
продлить жизнь на 15, а то и больше лет. Многие специалисты, врачи, психологи,
тренеры говорят о полезности и важности хорошего здорового сна. Без него
организм становится более подвержен стрессам, появляется усталость, которая не
дает нормально работать, тренироваться, радоваться жизни. А также снижается
иммунитет и ускоряются процессы старения.
Мелатонин: для чего он нужен?
Он выполняет множество полезных функций в организме. Многие гормоны связаны друг с другом, и недостаток одного сказывается на общем гормональном фоне, поэтому нужно внимательно следить за своим состоянием.
В задачи мелатонина входит:
- Упрощать засыпание;
- Устранять сонливость и усталость в дневное время;
- Поддерживать работу сердца;
- Укреплять иммунитет;
- Нормализовать работу эндокринной системы;
- Улучшать работу головного мозга;
- Нормализовать обмен веществ;
- Укреплять костную ткань;
- Улучшать состояние при психических заболеваниях;
- Поддерживать на нормальном уровне артериальное давление.
Также мелатонин влияет на массу тела. Существует мнение, что благодаря нему вырабатывается полезный бежевый жир, который служит источником энергии. Поэтому спортсмены особенно должны следить за уровнем мелатонина. Также он помогает предотвращать развитие онкологических заболеваний, снижать болевой синдром.
Где и когда вырабатывается?
За выработку отвечает самый
таинственный участок мозга, эпифиз (шишковидное тело), который называют
«третьим глазом». Одни специалисты говорят, что мелатонин вырабатывается, когда
человек спит, другие утверждают, что засыпать вовсе не обязательно, достаточно
находиться в покое и в темноте. Поэтому рекомендуют не спать при свете,
ночниках, включенном компьютере или телевизоре. Самый вредный для мелатонина
свет – бело-голубой, который исходит от люминесцентных ламп. Если все же
невозможно не использовать ночники, то лучше выбирать красные, они имеют
безопасную длину волны и не повлияют на сон.
Поэтому рекомендуют не спать при свете,
ночниках, включенном компьютере или телевизоре. Самый вредный для мелатонина
свет – бело-голубой, который исходит от люминесцентных ламп. Если все же
невозможно не использовать ночники, то лучше выбирать красные, они имеют
безопасную длину волны и не повлияют на сон.
Важную роль в синтезе играет серотонин, который производится под лучами солнца, поэтому людям, страдающим бессонницей, днем рекомендуют погулять на свежем воздухе.
Люди, которые спят не меньше 8 часов в сутки, обычно не нуждаются в приеме седативных препаратов, так как их нервная система в порядке, а стрессоустойчивость повышена.
В определенное время выработка мелатонина достигает максимума. Так, в 9 часов вечера уровень гормона повышается, а к 2 часам ночи достигает своего пика. К 9 утра он постепенно снижается. Именно отсюда пошло мнение, что сон красоты – с 9 до 11 вечера. У людей, которые работают по ночам, нарушаются все биоритмы, появляется хроническая усталость. Поэтому врачи советуют даже на работе находить пару часов для отдыха.
Симптомы и последствия дефицита мелатонина
Дневная норма мелатонина составляет 30-35 мкг. Стоит помнить, что выработанный мелатонин расходуется в течение суток. Поэтому хороший сон позволит быть бодрым только 1 день, а не всю неделю.
Признаками дефицита являются:
- Бессонница, невозможность долгое время уснуть, некрепкий сон, усталость по утрам;
- Подверженность инфекциям из-за снижения иммунитета;
- Гипертония;
- Нервные срывы;
- Тревожность, чувство отчаяния.
Нередко у людей с нехваткой мелатонина развивается депрессия. Чтобы нормализовать уровень гормона, необходимо пересмотреть свое питание. В тяжелых случаях лучше обратиться к специалисту.
Дефицит мелатонина может привести к очень неприятным последствиям для организма:
- Преждевременное старение. У человека начинают рано
появляться морщины, кожа становится дряблой, цвет лица сереет.

- Увеличение массы тела. Давно уже было отмечено, что быстрый набор массы связан и с режимом сна, и с гормональным фоном.
- Ранняя менопауза. Гормональные сбои нередко приводят к тому, что климакс наступает несколько раньше.
- Повышается риск развития рака груди. Проводились исследования, которые показали, что есть связь между онкологическими заболеваниями молочных желез и недостатком мелатонина. При приеме препаратов с мелатонином снижается вероятность развития рецидива.
Также люди с дефицитом этого гормона нередко страдают от отечности. При появлении тревожных признаков лучше обратиться к врачу.
Способы нормализации мелатонина
Уровень гормона во многом зависит от питания. Чтобы его повысить, нужно есть больше вишни, бананов, клубники, гранатов. Бананы к тому же оказывают расслабляющее действие. Также немало мелатонина в морковке, кукурузе, редисе, томатах. Полезным будет рис, овсянка.
Не стоит забывать, что есть продукты, которые способствуют уменьшению уровня мелатонина. К ним относят алкогольные напитки, крепкий кофе и чай, никотин. Если человек плохо спит, не стоит употреблять алкоголь и пить на ночь кофе и чай.
Некоторая доза мелатонина есть в молоке. Поэтому на ночь стакан теплого молока будет очень полезен. Сон станет крепче и приятнее.
Поскольку мелатонин и серотонин связаны, на хороший сон влияет практически все, что приносит человеку удовольствие. Это могут быть красивые пейзажи, приятные запахи, любимые занятия. Уровень серотонина и мелатонина от этого начинает повышаться. Поэтому при бессоннице рекомендуют как можно чаще баловать себя. Конечно, в этот же список включается и секс, который приводит к выбросу гормона удовольствия в кровь. Не зря ходят шутки о быстром засыпании после полового акта.
Если дефицит сильно выражен и
сказывается на самочувствии, врач может прописать препараты с мелатонином. К
ним, например, относят Мелаксен, Меларитм. Они используются как при хронической
бессоннице, так и при смене часовых поясов, чтобы быстрее адаптироваться.
Они используются как при хронической
бессоннице, так и при смене часовых поясов, чтобы быстрее адаптироваться.
Назначать дозировку и длительность приема препаратов должен врач. Они не вызывают привыкания, однако возможно возникновение побочных эффектов в виде тошноты и рвоты. Несмотря на низкую токсичность препарата, у некоторых людей на фоне его приема появляются проблемы с работой кишечника, усиливается отечность. Также не рекомендуется принимать мелатонин в таблетках с другими гормональными препаратами, так как они могут усиливать действие друг друга. Алкоголь снижает действие препарата.
Есть и определенные противопоказания. Не стоит принимать препараты с данным гормоном во время беременности, при сахарном диабете, эпилепсии, аутоиммунных заболеваниях, онкологических заболеваниях. В некоторых случаях рекомендуют внутривенное введение серотонина для борьбы с бессонницей.
Также важно помнить о влиянии света на выработку мелатонина. Ночью желательно находиться в полной темноте, а днем при максимальном освещении. Полезно гулять по несколько часов в день в солнечную погоду. Физические нагрузки вместе с солнечным светом поспособствуют нормальному сну и выработке гормона.
Мелатонин для похудения
Как уже говорилось выше, этот гормон влияет на массу тела. Тем, кто следит за фигурой, нужно помнить о поддержании нормального уровня мелатонина. В первую очередь гормон влияет на обмен веществ, ускоряя его. Таким образом жировые отложения появляются гораздо медленнее, а большая часть запасов уходит на выработку энергии для организма.
Несмотря на несомненную пользу, нельзя принимать большие дозы гормона. Это даст обратный эффект, приведет к сильной усталости, чувству разбитости.
Изучение мелатонина и его воздействие
на вес ведется до сих пор. Однако исследования уже показали, что, чем меньше
этого гормона, тем сложнее организму сгонять лишний вес. Уже говорилось про
бежевый жир, который является полезным для организма. Он не только дает
человеку энергию, но и имеет потрясающую способность сжигать калории.
Однако исследования уже показали, что, чем меньше
этого гормона, тем сложнее организму сгонять лишний вес. Уже говорилось про
бежевый жир, который является полезным для организма. Он не только дает
человеку энергию, но и имеет потрясающую способность сжигать калории.
Некоторые спортсмены принимают мелатонин, потому что повышается термогенный эффект во время тренировок. Также хороший сон ускоряет восстановление мышечной ткани, поврежденной по время физических нагрузок.
Мифы о мелатонине
Существуют определенные заблуждения, связанные с этим гормоном. Чтобы избежать ошибок, нужно знать о том, что представляет собой мелатонин и какие функции выполняет. Самыми распространенными являются следующие мифы:
- «Принимать таблетки с мелатонином нужно только в тяжелых случаях». Не всегда гормоны вредны для организма. В некоторых странах мелатонин считается биологической добавкой. Например, американцы пьют мелатонин на ночь, чтобы продлить молодость.
- «Если долго принимать, возникнет привыкание». Зависимости мелатонин не вызывает и синдрома отмены соответственно тоже. Врачи говорят, что любые снотворные препараты не стоит принимать дольше 3 недель. В случае с мелатонином никто не ставит жестких рамок, но нужно следить за реакцией организма: нет ли аллергии, побочных эффектов. Осторожность стоит проявлять женщинам, принимающим оральные контрацептивы. Они усиливают действие мелатонина, а соответственно и повышается риск возникновения побочных эффектов.
- «От приема этого снотворного утром тяжелее просыпаться». Мелатонин не является сильным снотворным препаратом, это гормон, который присутствует в каждом организме. Он лишь нормализует собственные биоритмы, а не вызывает резкую сонливость. Он справляется только с той бессонницей, которая связана с недостатком мелатонина, неправильным режимом дня и т.д.
Даже несмотря на все познания
относительно мелатонина, принимать постоянно в больших дозах препараты с ним
без консультации врача нельзя. Безопасным считается только смена питания и
нормализация времени и качества сна.
Безопасным считается только смена питания и
нормализация времени и качества сна.
Меланоцитстимулирующий гормон (МСГ) и его производные
С поправками от 16.07.2019
Меланоцитостимулирующий гормон (МСГ) — это пептидный гормон, который вырабатывается в организме человека и регулирует функцию пигментных клеток кожи (меланоцитов) [1]. МСГ также влияет на другие типы клеток [2, 3]. Из него производят различные синтетические препараты [4], которые аналогичны натуральному МСГ. Синтетические формы, которые имитируют меланоцитостимулирующий гормон в организме, включают Меланотан I и Меланотан II, также называемый «лекарством Барби». Эти инъекционные или назальные спреи часто используются для загара. Меланотан I — немного более дорогой продукт, который дает более естественный загар. Меланотан II дешевле, дает темный загар и снижает аппетит [5].
Термин «Меланотан I» и статус вещества могут вызвать некоторую путаницу. На рынке есть пептид, ранее известный как Меланотан I. Однако сегодня это вещество называется афамеланотидом. Афамеланотид был разрешен в конце 2014 года и используется в медицинских целях. Термины «Меланотан I и II» используются сегодня для обозначения препарата для загара, который распространяется незаконно. Афамеланотид изучен более широко и признан относительно безопасным. То же самое нельзя сказать о меланотанах I и II, поскольку их производство и продажа не регулируются и не контролируются [6].
МСГ особенно влияет на функцию кожи. Кожа — это самый большой орган чувств, который ощущает давление, контакт, температуру и боль [7]. Структура кожи включает несколько слоев [7]. Внешний слой кожи, называемый роговым слоем, состоит из мертвых и ороговевших клеток. Под роговым слоем находится эпидермис. Внутренний слой эпидермиса состоит из специальных пигментных клеток, меланоцитов, в которых образуется меланин. Под эпидермисом находится дерма, которая представляет собой водный и жировой подкожный слой без четких границ. Кроме того, показано, что МСГ может влиять и на поступление питательных веществ [8, 9]. Если в теле абсорбируется больше питательных веществ, чем необходимо клеткам на текущий момент, то дополнительное количество питательных веществ откладывается в виде гликогена или жировой ткани [7].
Если в теле абсорбируется больше питательных веществ, чем необходимо клеткам на текущий момент, то дополнительное количество питательных веществ откладывается в виде гликогена или жировой ткани [7].
Между приемами пищи из данных резервов в организме выделяется энергия. В организме человека происходит гормональная регуляция высвобождения и хранения питательных веществ. При этом α-меланоцитостимулирующий гормон снижает количество потребляемых питательных веществ [8, 9], что может привести к снижению массы тела.
Применение в медицине
МСГ действует на множество точек приложения и рецепторов в организме человека, благодаря чему он может использоваться в различных медицинских целях [3]. Аналог α-МСГ (афамеланотид) ранее изучался, в частности, для лечения эритропоэтической протопорфирии (ЭП) [8]. ЭП — это заболевание, симптомы которого включают нарушение чувствительности кожи к эффектам солнечного излучения. Аналоги α-МСГ также изучались в качестве препаратов для лечения эректильных нарушений.
Свойства и механизм действия
Меланоцитостимулирующий гормон влияет на организм человека через меланокортиновые рецепторы [3]. Данные рецепторы находятся в разных частях тела, что объясняет множественные эффекты МСГ на организм человека. С точки зрения пациента, эффекты могут быть желаемыми или вредными. Показано, что помимо пигментации кожи, МСГ оказывает влияние на половую функцию и регуляцию поступления питательных веществ.
Эпителиальный меланин играет важную роль в защите клеток кожи от вредных ультрафиолетовых лучей (УФ-лучей) [2, 7]. Когда кожа подвергается воздействию ультрафиолетовых лучей, меланин связывается с самими лучами, что вызывает активацию меланоцитов и начало выработки большего количества меланина [7]. По мере увеличения количества меланина кожа становится более темной или загорелой. Таким образом, меланиновый пигмент кожи защищает кожу от повреждений ультрафиолетовыми лучами [2].
Исследования показали, что синтетический α-МСГ усиливает пигментацию кожи [11, 4]. Было обнаружено, что α-МСГ значительно увеличивает количество меланина в коже и в то же время уменьшает количество повреждений, вызванных УФ-излучением [4].
Было обнаружено, что α-МСГ значительно увеличивает количество меланина в коже и в то же время уменьшает количество повреждений, вызванных УФ-излучением [4].
Гормон, стимулирующий α-меланоциты, уменьшает количество потребляемой пищи [8, 9], что может привести к потере веса. Тошнота и снижение аппетита были отмечены как побочные эффекты меланотана II [11], что может [9], что также может объяснить возможную потерю веса, связанную с меланоцитостимулирующим гормоном.
Синтетический α-МСГ используется для получения эффекта загара. Желание похудеть и ускорение процесса похудения, а также повышение либидо ¬также являются причинами принимать аналоги α-МСГ. Вот почему Меланотан II также называют «лекарством Барби».
Побочные эффекты
В исследованиях аналогов α-МСГ было описано несколько побочных эффектов, в том числе тошнота, покраснение лица [4, 10, 11], усталость [11, 4], рвота [4], аритмия, потоотделение, повышенная агрессия, а также спонтанная эрекция и продолжительная эрекция, т. е. приапизм. Приапизм является болезненной продолжительной эрекцией и может потребовать хирургического вмешательства [13]. У тех, кто принимает препарат, отмечается также быстрое развитие меланомы, но причинно-следственная связь пока не ясна [14].
МСГ и его аналоги оказывают множество эффектов в организме человека. При применении аналогов МСГ нет уверенности в том, что будут проявляться только желаемые эффекты гормона. Могут проявляться и побочные эффекты. Меланотан II, в частности, имеет больше потенциальных побочных эффектов [6].
Это обусловлено тем, что рецепторы-мишени МСГ находятся во многих частях тела. Инъекционное применение МСГ или его синтетического аналога может воздействовать на все эти рецепторы и приводить к развитию нежелательных эффектов. Кроме того, состав аналогов, продаваемых в интернет-магазинах, например препарата Меланотан II, неизвестен. Таким образом, безопасность применения подобных препаратов оценить достаточно трудно.
Salla Ruuska (Салла Рууска)
Магистр наук, фармацевт
Правки внесены: Dopinglinkki
Что такое Меланин — Umetex Aesthetics
Меланин – живая природная краска, пигмент черного, коричневого, красного или желтого цвета, который содержится в радужке глаза, волосах, коже человека и отвечает за их цвет. Много меланина находится в некоторых отделах мозга и внутреннем ухе человека.
Много меланина находится в некоторых отделах мозга и внутреннем ухе человека.
Вырабатывается меланин специальными клетками – меланоцитами. Главная его функция – защита организма от ультрафиолетового излучения, химических и физических факторов, имеющих канцерогенные и мутагенные свойства.
Меланин экранирует и поглощает солнечные лучи, трансформируя одну часть энергии в тепло, а другую использует для фотохимических реакций организма (образование загара). Пигмент скапливается возле ядра клетки, что позволяет:
- защищать хранящуюся в ядре генетическую информацию;
- предотвращать злокачественное перерождение клетки под действием ультрафиолета.
У людей с разными фототипами кожи содержание меланина сильно отличается. Меньше всего его содержание у людей с 1-ым фототипом, больше всего – с 6-ым. Если организм совсем не вырабатывает меланин, тогда мы получаем людей-альбиносов. В животном мире альбиносы встречаются гораздо чаще, особенно среди грызунов.
Количество меланина в организме может снижаться под воздействием:
- нарушения гормонального баланса;
- заболеваний эндокринной системы;
- генетических заболеваний;
- недостаточного потребления минералов и витаминов;
- возрастных изменений;
- частых стрессов;
- недостатка солнечного света.
На недостаток меланина могут указывать следующие внешние признаки:
- солнечные ожоги;
- неравномерный загар;
- белесые пятна;
- ранние морщины и седина;
- блеклые радужки глаз.
При возникновении перечисленных признаков нужно потреблять больше продуктов питания, которые помогают нормализовать выработку меланина, отказаться от вредных привычек и вести здоровый образ жизни. Прием лекарственных препаратов и БАДов лучше согласовать со специалистом.
ПЕРЕЙТИ В ГЛОССАРИЙ
Компания umetex aesthetics предлагает косметологическим клиникам лазерные аппараты для омоложения, устранения патологий кожного покрова и сосудов. Смотрите каталог компании, выбирайте лазеры для косметологии.
Смотрите каталог компании, выбирайте лазеры для косметологии.
Путь производства меланина
Меган Найт, бакалавр наук
Что такое меланин?
Меланин — основной пигмент позвоночных. Тип и скорость синтезируемого меланина определяют цвет кожи и волос. Меланин — это светопоглощающий полимер, полученный из незаменимой аминокислоты тирозина, который рассеивает УФ-свет и преобразует его в тепло. Способность меланина поглощать свет выполняет множество защитных функций у позвоночных, включая маскировку, защиту от разрушающего солнечного излучения УФА и УФВ, а также терморегуляцию.
У популяций, продуцирующих более высокие уровни эпидермального меланина, ниже уровень заболеваемости раком кожи из-за его фотозащитных свойств.
Меланин также действует как антибиотик и поглощает свободные радикалы. Благодаря широкому спектру функций меланин экспрессируется в нескольких областях человеческого тела, включая кожу, волосы, глаза и мозг. Однако специфическая роль меланина в этих тканях недостаточно изучена.
Основными типами меланина являются:
- Феомеланин — пигмент от оранжевого до красного, выраженный в волосах и коже.Низкие защитные свойства от повреждений ДНК, вызванных УФ-излучением.
- Эумеланин — пигмент от коричневого до черного, выраженный в волосах и коже. Более высокие защитные свойства от повреждений ДНК, вызванных УФ-излучением.
- Нейромеланин — экспрессируется в нескольких областях мозга. Его потеря связана с рядом неврологических расстройств.
Меланоциты и меланогенез
Меланин синтезируется в цитоплазматических органеллах, называемых меланосомами, которые находятся в клетках кожи и волосяных фолликулах, называемых меланоцитами.Этот процесс известен как меланогенез.
Путь производства меланина »/> Меланоциты и меланин. слои эпидермиса. Меланоциты производят пигмент меланин, который затем могут переноситься в другие клетки эпидермиса. Кредит изображения: Designua / Shutterstock
Кредит изображения: Designua / Shutterstock
Меланоциты экспрессируют высокополиморфный ген, который кодирует рецептор, связанный с G-белком (GPCR), называемый рецептором меланокортина 1 (MC1R). У людей существует более 100 вариантов MC1R, каждый с разным уровнем активности.Помимо продукции меланина, уровень активности MC1R в меланоцитах является основным определяющим фактором цвета кожи человека.
Меланоциты в основном ограничены базальным слоем эпидермиса, где они образуют «эпидермальную меланиновую единицу», состоящую из одного меланоцита, примерно 36 кератиноцитов и одной клетки Лангерганса.
Ультрафиолетовое излучение как регулятор меланогенеза
Основным внешним регулятором меланогенеза является ультрафиолетовое излучение (УФР), включая УФА и УФВ свет.Это главный стимул для выработки меланина, приводящий к индуцированной пигментации кожи или «загару». Другие стимулы меланогенеза включают андрогены, которые являются естественным стероидным гормоном, и медиаторы воспаления.
UVR увеличивает пролиферацию и привлечение меланоцитов в эпидермис, а также производство меланосом. Это происходит из-за повышенного уровня активных форм кислорода, которые вызывают повреждение ДНК и активацию ферментов, участвующих в меланогенезе, таких как тирозиназа.Длительные периоды воздействия ультрафиолетового излучения B на высоких уровнях могут вызвать обширное повреждение ДНК. Это может вызвать запрограммированную гибель (или апоптоз) пораженных клеток кожи, что также является причиной «солнечных ожогов».
В других клетках запускается путь восстановления повреждений ДНК. На этом пути фактор транскрипции и белок-супрессор опухолей p53 стабилизируются и активируются в кератиноцитах с повреждением ДНК. Это приводит к увеличению выработки меланоцит-стимулирующего гормона (МСГ).Затем MSH связывается с рецепторами MC1R, экспрессируемыми на меланоцитах, вызывая циклический AMP-специфический ответ.
цАМФ активирует протеинкиназу А, которая фосфорилирует фактор транскрипции элемента ответа цАМФ (CREB). CREB усиливает экспрессию фактора транскрипции, связанного с микрофалмией (MITF), что приводит к усилению активности ферментов, участвующих в меланогенезе, и белков, транспортирующих меланосомы. MITF также может быть активирован митоген-активируемыми протеинкиназами (MAPK).
CREB усиливает экспрессию фактора транскрипции, связанного с микрофалмией (MITF), что приводит к усилению активности ферментов, участвующих в меланогенезе, и белков, транспортирующих меланосомы. MITF также может быть активирован митоген-активируемыми протеинкиназами (MAPK).
киназных путей цАМФ и MAP, запускаемых после УФР-индуцированного повреждения ДНК, синтезируют аминокислотный тирозин.Тирозин превращается ферментом тирозиназой, активируемым УФ-излучением, в допахинон. Сам допахинон может превращаться в эумеланин или в допахром, который затем превращается в эумеланин. Допахинон также может превращаться в цистеинил-допа, который превращается в феомеланин. Недостаток тирозина связан с альбинизмом, который характеризуется потерей пигментации кожи и волос.
Меланосомы затем переносятся из меланоцитов в кератиноциты, которые находятся в верхних слоях эпидермиса.Внутри кератиноцитов мембрана меланосом разрушается лизосомальными ферментами. Это высвобождает меланин в цитоплазму, где он образует меланиновую «шапку» вокруг генетического материала клеток. Это защищает ДНК от дальнейшего повреждения ультрафиолетом.
Источники
- Видерия, И. Ф. С., Моура, Д. Ф. Л., Магина, С. Механизмы, регулирующие меланогенез. Бюстгальтеры Dermatol . 2013; 88 (1): 76-83 .
- Агар, Н., Янг, А. Р. Меланогенез: фотозащитный ответ на повреждение ДНК ?. Исследование мутаций . 2005; 571: 121–132 .
- Парк, Х. Ю., Космадаки, М., Яар, М., Гилчрест, Б. А. Клеточные механизмы, регулирующие меланогенез человека. Cell Mol Life Sci . 2009; 66: 1493–1506 .
Дополнительная литература
Что такое меланин? Что делает меланин в организме?
Если у вас есть какие-либо медицинские вопросы или опасения, обратитесь к своему врачу. Статьи в Health Guide основаны на рецензируемых исследованиях и информации, полученной от медицинских обществ и правительственных агентств.Однако они не заменяют профессиональные медицинские консультации, диагностику или лечение.
Меланин — это термин, обозначающий группу природных пигментов, встречающихся в большинстве форм жизни. У людей меланин вырабатывается клетками внутреннего слоя кожи (базальный слой) и волосяных фолликулов, называемых меланоцитами. Пигмент присутствует и придает цвет частям тела, таким как кожа, волосы, нос, внутреннее ухо и сосудистая оболочка глаз (область между сетчаткой и белой склерой).
- Меланин — это натуральный пигмент, придающий цвет коже, волосам и т. Д.
- Меланин в некоторых отношениях защищает, а в других опасен.
- Не существует проверенного способа безопасного повышения уровня меланина.
- Полноценная диета может помочь организму и выработке меланина нормально функционировать.
Меланин играет тонкую двойную роль в организме. Он помогает защитить тело от воздействия ультрафиолетового (УФ) света от солнца (и солнечных лучей), производя коричневатый пигмент (загар).Но меланин также может накапливаться в концентрированных формах, представляющих опасность для здоровья. Хотя нет проверенного способа безопасного повышения уровня меланина, есть шаги, которые вы можете предпринять, чтобы сохранить свою кожу здоровой и нормально функционировать.
Существует три типа меланина: эумеланин, феомеланин и нейромеланин. Эумеланин можно разделить на черный и коричневый тип. Например, уровень эумеланина влияет на внешний вид цвета волос. Большое количество черного или коричневого эумеланина приводит к более темным волосам, а небольшое количество — к светлым.
Объявление
Roman Daily — поливитамины для мужчин
Наша команда штатных врачей создала Roman Daily для устранения распространенных недостатков питания у мужчин с помощью научно обоснованных ингредиентов и дозировок.
Учить больше Волосы становятся седыми, когда в более позднем возрасте производство эумеланина замедляется. И если у вас есть мутация в так называемом рецепторе меланокортина 1 (MC1R), который участвует в превращении феомеланина в эумеланин, преобладает феомеланин, и именно это вызывает рыжие волосы. Уровень феомеланина также влияет на цвет кожи, создавая желтые, красные и розовые оттенки.
Уровень феомеланина также влияет на цвет кожи, создавая желтые, красные и розовые оттенки.
Считается, что этот особый тип пигмента придает отчетливый темный цвет частям мозга, таким как черная субстанция и голубое пятно. Некоторые исследователи говорят, что присутствие пигмента помогает предотвратить гибель клеток в этих частях мозга, и связывают потерю феомеланина с признаками и симптомами болезни Паркинсона, неврологического расстройства (Vila, 2019).
Меланин играет важную роль в определении цвета ваших волос, кожи и глаз.Ваши гены, унаследованные от родителей, во многом определяют, сколько меланина вы производите; у людей с темной кожей больше меланина, чем у людей со светлой (светлой) кожей.
Тело вырабатывает меланин посредством нескольких химических реакций, известных как меланогенез. Ключевым этапом в этой сложной последовательности является окисление аминокислоты тирозина, которая является одним из нескольких строительных блоков белка. Примечательно, что разница во внешности людей со светлой и темной пигментацией определяется уровнем производства меланоцитов, а не количеством меланоцитов в коже.
Можно ли получить достаточно витамина D от солнца?
4 минуты чтения
К сожалению, с пигментацией кожи не всегда все идет так, как должно. Например, люди с генетическим нарушением альбинизма имеют мало пигмента меланина или совсем не имеют его, что приводит к минимальному окрашиванию или отсутствию окрашивания кожи, волос и глаз; у большинства белые или светло-русые волосы и очень бледная кожа.
Витилиго — еще одно заболевание, связанное с недостатком меланина. Это происходит, когда клетки, которые обычно производят меланин, перестают работать или умирают.
С одной стороны, меланин является широкополосным УФ-абсорбентом и солнцезащитным кремом, обеспечивающим защиту как от УФ-А, так и от УФ-В-лучей. Под воздействием ультрафиолетового света производство и активность меланоцитов возрастают, а кожа темнеет по мере повышения уровня меланина.
Под воздействием ультрафиолетового света производство и активность меланоцитов возрастают, а кожа темнеет по мере повышения уровня меланина.
Обладая защитным действием, пигмент меланина — веснушки — может образовываться после пребывания на солнце.Меланин также служит антиоксидантом и поглотителем свободных радикалов, помогая избавиться от аномальных клеток, которые могут привести к заболеваниям.
Объявление
Упростите процедуру ухода за кожей
Каждая бутылка прописанного врачом Nightly Defense изготовлена для вас из тщательно отобранных, сильнодействующих ингредиентов и доставлена к вашей двери.
Учить большеНаступает переломный момент, когда повышенный уровень меланина не помогает, а повышает риск возникновения проблем.Увеличение выработки меланина, потемнение тона кожи и накопление концентрированных участков меланина в течение 48 часов после воздействия УФ-излучения могут увеличить риск рака кожи, такого как злокачественная меланома. Из двух основных типов УФ-лучей УФ-B в значительной степени отвечает за солнечный ожог. Оба типа могут вызвать рак кожи.
Пожалуйста, не собирайте солнечную энергию своим анальным отверстием, говорят ученые
6 минут на чтение
Хотя необходимы дополнительные исследования, чтобы понять связь и подтвердить, что у них больше меланина, люди с более темной кожей, по-видимому, с меньшей вероятностью заболеют меланомой и другими видами рака кожи.Однако это возможно — безопасного загара не существует. Любой может заболеть раком кожи.
Также неясно: рискуют ли люди с более темной кожей получать слишком мало витамина D, поскольку людям с темным оттенком кожи может потребоваться воздействие солнечного света по крайней мере в три-пять раз дольше, чтобы выработать такое же количество витамина D, как и человеку с белой кожей. делает (Наир, 2012).
Слишком мало витамина D небезопасно. Помимо прочего, этот витамин помогает предотвратить сердечные заболевания, депрессию, грипп, рак и аутоиммунные заболевания.Поскольку лишь небольшое количество продуктов содержат витамин D, диетические добавки могут быть ответом для этих людей (Управление диетических добавок NIH, 2020).
Нет доказательств того, что уровень меланина можно безопасно повысить с помощью пищевых добавок, витаминов или других средств. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предупреждает, что не существует «волшебной таблетки» для ускорения загара при небольшом воздействии ультрафиолетового излучения (U.S. FDA, 2018).
Но, хотя мгновенного решения проблемы не существует, питательная и сбалансированная диета, вероятно, может помочь сохранить уровень меланина на должном уровне.Наиболее эффективен для упругой и здоровой кожи? Скорее всего, продукты, богатые витаминами-антиоксидантами (A, C и E).
Считается, что антиоксидантыпомогают предотвратить или отсрочить повреждение клеток кожи и другие типы повреждений, противодействуя окислительному стрессу от нестабильных молекул, называемых свободными радикалами (Liu-Sith, F, 2016).
- Витамин A: Учитывая его антиоксидантный эффект, некоторые ученые утверждают, что этот жирорастворимый витамин больше, чем любой другой, может быть ключом к здоровой выработке меланина (Godic, 2014).Так что положите на тарелку рыбу, листовые зеленые овощи, брокколи, морковь, томатные продукты и другие оранжевые и желтые овощи.
- Витамин C: Этот антиоксидант, вероятно, улучшает здоровье кожи, поддерживая иммунитет. Организм также использует его для выработки коллагена, белка и ранозаживляющего вещества, жизненно важного для укрепления кожи, а также волос, сухожилий, связок и т. Д., А также для предотвращения обвисания кожи. У американцев редко бывает дефицит витамина С, но вы можете подстраховаться, употребляя много фруктов и овощей, богатых этим питательным веществом, таких как красный и зеленый перец, киви, брокколи, клубника, помидоры и печеный картофель.

- Витамин E: Смягчающее и антиоксидантное средство, витамин E может защищать мембраны от повреждения ультрафиолетом. Попробуйте наносить составы непосредственно на кожу, чтобы уменьшить повреждение кожи, вызванное солнцем. И через продукты: используйте растительные масла и ешьте орехи, семена и зеленые листовые овощи.
- Травы и растительные вещества: Экстракты цельных трав, содержащие ключевые витамины, могут помочь коже оставаться здоровой и хорошо заживать. Считается, что сложная смесь ингредиентов зеленого и черного чая способствует заживлению кожи.То же самое с гелем алоэ вера (особенно после солнечных ожогов) и кунжутным маслом. Тем не менее, ни один из них не является убедительным доказательством того, что он играет роль в повышении производства меланина (Korac, 2011).
- Форсколин: Несмотря на волнение, вызванное «Письмом в редакцию» Института рака Дана-Фарбер в журнале Nature в 2006 году, нет никаких доказательств того, что экстракт корня индийского растения Coleus forskholii может увеличивать выработку меланина в организме человека ( Д’орацио, 2006; MSKCC, 2020). Хотя форсколин действовал как защита от вредных ультрафиолетовых лучей у мышей со светлой кожей, а также работал как средство для загара, исследование никогда не распространялось на людей.
Хотите, чтобы производство меланина продолжало расти? Ограничьте пребывание на солнце и упакуйте эти овощи!
- Бреннер, М., и Хиринг, В. Дж. (2007). Защитная роль меланина от УФ-излучения в коже человека †. Фотохимия и фотобиология, 84 (3), 539–549. https://doi.org/10.1111/j.1751-1097.2007.00226.x.
- Д’Оразио, Дж. А., Нобухиса, Т., Цуй, Р., Арья, М., Спрай, М., Вакамацу, К.,… Фишер, Д. Э. (2006). Стратегия местного применения лекарств и защита кожи, основанная на роли Mc1r в УФ-индуцированном загаре.Природа, 443 (7109), 340–344. https://doi.org/10.1038/nature05098. https://pubmed.ncbi.
 nlm.nih.gov/16988713/
nlm.nih.gov/16988713/ - Годич, А., Полйшак, Б., Адамич, М., и Дахман, Р. (2014). Роль антиоксидантов в профилактике и лечении рака кожи. Окислительная медицина и клеточное долголетие, 2014, 1–6. https://doi.org/10.1155/2014/860479. https://pubmed.ncbi.nlm.nih.gov/247/
- Интегративная медицина в Мемориальном онкологическом центре им. Слоуна Кеттеринга. (2020, апрель). Форсколин. Получено с https: // www.mskcc.org/cancer-care/integrative-medicine/herbs/forskolin.
- Ито, С., и Вакамацу, К. (2011). Разнообразие пигментации волос человека по данным химического анализа эумеланина и феомеланина. Журнал Европейской академии дерматологии и венерологии, 25 (12), 1369–1380. https://doi.org/10.1111/j.1468-3083.2011.04278.x.
- Korać, R., & Khambholja, K. (2011). Потенциал трав в защите кожи от ультрафиолета. Обзоры фармакогнозии, 5 (10), 164.https://doi.org/10.4103/0973-7847. https://pubmed.ncbi.nlm.nih.gov/22279374/
- Лю-Смит, Ф., & Мейскенс, Ф. Л. (2016). Молекулярные механизмы флавоноидов в синтезе меланина и потенциал для профилактики и лечения меланомы. Молекулярное питание и исследования пищевых продуктов, 60 (6), 1264–1274. https://doi.org/10.1002/mnfr.201500822 https://pubmed.ncbi.nlm.nih.gov/26865001/
- Наир Р., Масих А. (2012). Витамин D: витамин «солнечного света». J. Pharmacol Pharmacother, 3 (2), 118-126.DOI: 10.4103 / 0976-500X.95506, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3356951/
- Управление пищевых добавок, Национальные институты здравоохранения. Витамин А. Получено с https://ods.od.nih.gov/factsheets/VitaminA-HealthProfessional/ .
- Управление пищевых добавок, Национальные институты здравоохранения. Витамин D. Получено с https://ods.od.nih.gov/factsheets/VitaminD-HealthProfessional/.
- Шлессингер Д.И., Аноруо М.Д., Шлессингер Дж. Биохимия, Меланин.[Обновлено 27 апреля 2020 г.]. В: StatPearls [Интернет]. Остров сокровищ (Флорида): StatPearls Publishing; 2020 Янв.
 Доступно по адресу: https://www.ncbi.nlm.nih.gov/books/NBK459156/.
Доступно по адресу: https://www.ncbi.nlm.nih.gov/books/NBK459156/. - Фонд рака кожи. Загар и твоя кожа. Источник: https://www.skincancer.org/risk-factors/tanning/.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. (2018, март) Таблетки для загара. Получено с: https://www.fda.gov/cosmetics/cosmetic-products/tanning-pills#:~:text=In%20their%20quest%20for%20the,to%20appear%20on%20the%20market.
- Вила, М. (2019). Нейромеланин, старение и уязвимость нейронов при болезни Паркинсона. Расстройства движения, 34 (10), 1440–1451. https://doi.org/10.1002/mds.27776. https://pubmed.ncbi.nlm.nih.gov/31251435/
Подробнее
Что вам нужно знать — SkinKraft
Вы когда-нибудь задумывались, что придает цвет вашей коже или вызывает обесцвечивание некоторых частей тела? Основная причина всего этого — меланин, пигмент от коричневого до черного, обнаруженный в вашей коже, волосах и радужной оболочке глаза, который отвечает за ваш цвет / цвет лица.
Наш главный дерматолог доктор Хариш Коутам, аккредитованный член Индийской ассоциации дерматологов, венерологов и лепрологов (IADVL) и косметических хирургов Индии, утверждает, что меланин играет двойную роль в защите, а также в нанесении определенного вреда.
Итак, хотите ли вы загореть или осветлить загорелую кожу, вам необходимо понимать, что такое меланин и как вы можете увеличить или уменьшить его содержание. Прокрутите вниз, чтобы узнать.
Основные характеристики:
1.Что такое меланин и почему он важен?
С научной точки зрения, меланин вырабатывается меланоцитами (клетками) в базальном слое (нижнем слое) кожи [1]. Это происходит, когда фермент тирозиназа катализирует превращение тирозина в дигидроксифенилаланин (ДОФА) [2].
Согласно научным исследованиям, меланин может не только придать коже ее цвет, но и защитить ее от вредных ультрафиолетовых лучей солнца. Недавние исследования также демонстрируют способность меланина снижать риск рака кожи.[3]
Недавние исследования также демонстрируют способность меланина снижать риск рака кожи.[3]
Доктор Хариш говорит: «Защитный эффект меланина достигается за счет его способности служить физическим барьером, рассеивающим УФ-лучи, и поглощающим фильтром, который снижает проникновение УФ-излучения через эпидермис (68). Эффективность меланина в качестве солнцезащитного крема находилась между 1,5 солнцезащитными факторами (SPF) и 4 SFP, что означает, что меланин поглощает от 50% до 75% УФ-излучения ».
Далее он добавляет: «Он также действует как поглотитель свободных радикалов, что в конечном итоге защищает кожу.Однако исследования показали, что меланин может иметь слабый канцерогенный эффект, который может способствовать образованию рака. Но его вредные эффекты еще не доказаны, и исследования продолжаются ».
2. Могу ли я снизить уровень меланина в коже?
Многие индийские женщины одержимы светлым цветом кожи. Некоторые люди хотят снизить уровень меланина в коже для более светлого оттенка кожи. Пигмент меланина можно уменьшить с помощью домашних процедур, процедур в клинике и домашних средств.
Клинические процедуры
А.Химический пилинг
Химический пилинг действует, удаляя верхний слой кожи. [4] При таком отшелушивании удаляются отложения меланина в верхнем слое и обнажается свежий слой кожи. Химический пилинг включает высокие концентрации кислот, таких как гликолевая кислота или молочная кислота. Они проводятся в кабинете дерматолога.
Химический пилинг — эффективный способ снизить уровень меланина в коже, но он может вызывать побочные эффекты, такие как покраснение и жжение. Перед началом лечения проконсультируйтесь с врачом.Чрезвычайно важно использовать солнцезащитный крем во время этого лечения, поскольку новые клетки склонны к повреждению солнцем.
B. Микродермабразия
Микродермабразия удаляет верхний слой кожи с помощью ручного устройства. Это малоинвазивная процедура для отшелушивания кожи и избавления от избытка пигмента меланина.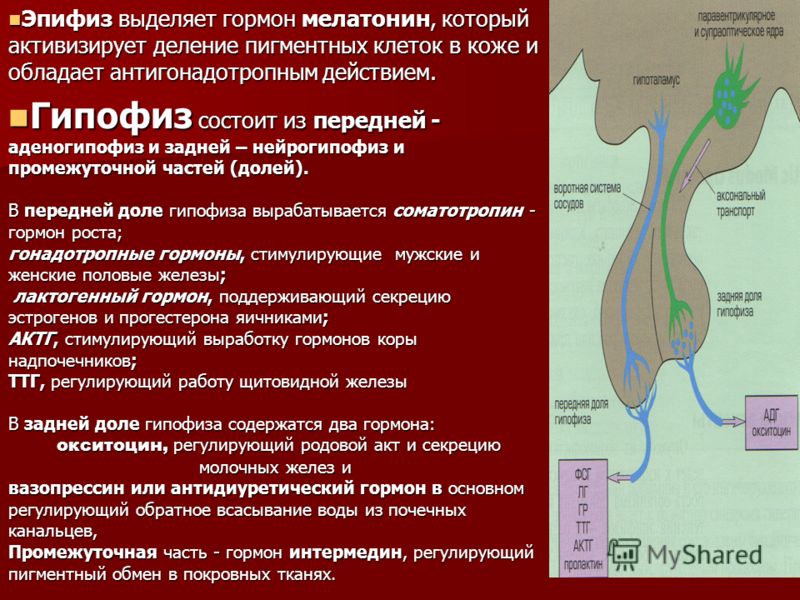 [5]
[5]
В этой процедуре используются мелкие кристаллы для соскабливания или соскабливания верхнего слоя кожи. Это процедура с низким уровнем риска, эффективная для удаления загара и разглаживания кожи.
C. Лазерная шлифовка
Лазерная шлифовка использует лучи света для нацеливания на слой кожи. [6] Далее он делится на абляционный и неаблативный. Абляционные лазеры удаляют верхние слои кожи через раны, в то время как неабляционные лазеры вызывают рост коллагена в эпидермисе.
Абляционный лазер может быть немного более опасным по сравнению с неабляционным. Проконсультируйтесь с дерматологом по поводу наилучшего лазерного лечения для уменьшения содержания меланина в коже.
Домашние процедуры
А.Койевая кислота
Койевая кислота получают из определенных видов грибов. Он действует путем ингибирования аминокислоты тирозина, ответственной за производство меланина [7]. Койевая кислота является проверенным средством для осветления кожи и используется в концентрациях менее 1%.
Койевая кислота может вызывать побочные эффекты, такие как контактный дерматит, состояние, которое приводит к зуду или покраснению кожи и т. Д. После контакта с определенными ингредиентами. Продолжительное употребление койевой кислоты может сделать вашу кожу восприимчивой к солнечным лучам.
B. Гидрохинон
Гидрохинон — одно из старейших и наиболее эффективных средств удаления меланина с кожи. Уменьшает количество меланоцитов в коже. [8]
Со временем гидрохинон осветляет кожу. Натуральная альтернатива — шелковица. Но у некоторых людей гидрохинон может вызывать сухость.
C. Ретиноиды
Ретиноиды — это производные витамина А, которые действуют путем ингибирования фермента тирозиназы [9]. Третиноин (ретиноид) используется для осветления кожи.Ретиноиды помогают в обновлении клеток кожи и равномерно распределяют оставшиеся гранулы меланина по коже.
Новые клетки свежие, нежные и требуют солнцезащитного крема. Поэтому при использовании ретиноидов всегда используйте солнцезащитный крем широкого спектра действия.
Поэтому при использовании ретиноидов всегда используйте солнцезащитный крем широкого спектра действия.
Домашние средства
Люди использовали кухонные ингредиенты для уменьшения содержания меланина в коже, но у них нет научных доказательств. Однако они приносят пользу людям, осветляя их кожу.
A. Картофель
Картофель содержит фермент катехолаза, который снижает уровень меланина в коже.Картофель — отличный антиоксидант, помогающий коже от окислительного стресса.
Б. Лимонный
Лимон содержит альфа-гидроксикислоту, которая отшелушивает верхний слой кожи, содержащий меланин. Лимон — натуральный отбеливающий агент.
C. Помидор
Помидор полезен для кожи. Одним из них является его способность ингибировать фермент тирозиназу, который помогает в синтезе меланина. Он также обладает противовоспалительными и антивозрастными свойствами.
3. Что вызывает повышенное производство меланина?
УФ-А лучи солнечного света проникают в нижние слои эпидермиса и заставляют меланоциты производить больше меланина.Меланин вырабатывается как защитный механизм.
Солнечный свет — основная причина увеличения выработки меланина. Другие факторы включают гормональный дисбаланс, старение и воспалительные процессы.
4. Могу ли я повысить уровень меланина?
Если вы хотите учесть тот факт, что меланин может снизить риск рака кожи и защитить вас от УФ-лучей, вот несколько способов увеличить количество меланина в вашей коже:
Как навсегда увеличить содержание меланина в коже с помощью еды
Нет научных исследований, показывающих, как увеличить уровень меланина.Но определенные питательные вещества повышают уровень меланина в коже:
A. Антиоксиданты
Антиоксиданты защищают вас от окислительного повреждения. Свободные радикалы в вашем теле всегда ищут дополнительный электрон и могут химически сжечь клетки во время этого процесса. Антиоксиданты могут отдавать свободный электрон, тем самым стабилизируя дикие свободные радикалы.
Продукты, содержащие антиоксиданты, включают рыбу, виноград, ягоды, зелень, зеленый чай, бобы, темный шоколад, свеклу, сладкий картофель, краснокочанную капусту и т. Д.
B. Витамин A
Поскольку витамин А также является мощным антиоксидантом, он связан с увеличением производства меланина. Витамин А — это жирорастворимый витамин, который содержится в организме.
Витамин А можно получить из пищевых источников, таких как зеленые листовые овощи, морковь, манго, горох, сладкий картофель, жир печени трески, лосось, тунец, масло, брокколи, салат, красный сладкий перец, сыр и т. Д.
C. Витамин C
Витамин С, еще один антиоксидант, не доказал свою полезность для производства меланина, но может повышать уровень меланина.
Витамин С присутствует в таких продуктах, как сливы, вишня, гуава, брокколи, ростки, лимон, папайя, клубника, апельсин и т. Д.
D. Витамин E
Возможно, вы уже много раз слышали о продуктах по уходу за кожей, обогащенных витамином Е. Витамин Е при местном применении успокаивает кожу.
Считается, что пероральный витамин Е увеличивает количество меланина. Миндаль, фундук, арахис, авокадо, манго и омары — все это богатые источники витамина Е.
5. Означает ли большее количество меланина более темную кожу?
В зависимости от уровня меланина в коже цвет лица в целом подразделяется на светлый, средний и темный.Чем выше пигмент меланина, тем темнее кожа.
6. Что происходит, когда у вас слишком много или слишком мало меланина?
Слишком мало меланина может привести к состоянию, называемому альбинизмом. У людей с альбинизмом бледная кожа и белые волосы. С другой стороны, дефицит меланина может указывать на гиперпигментацию.
7. Может ли меланин вызывать рак кожи?
УФ-излучение производит реактивный кислород, который возбуждает электрон в меланине. Эта энергия может вызвать разрывы цепей ДНК и привести к канцерогенным мутациям.
Исследователи подчеркнули роль меланина в развитии рака кожи после воздействия УФ-лампы на клетки меланоцитов человека. Они подвергли меланоциты мыши и клетки меланоцитов человека воздействию УФ-ламп. Они обнаружили повреждение ДНК в обоих, но продолжающееся повреждение в клетках меланоцитов человека (содержащих меланин) даже после нескольких часов воздействия ультрафиолетового света. Это привело их к выводу, что меланин может вызывать рак кожи [10].
Все вышеперечисленные методы стоит попробовать, чтобы увеличить или уменьшить уровень меланина. Но не забудьте проконсультироваться с дерматологом перед тем, как начинать какие-либо процедуры или диету.Сообщите нам, что сработало для вас.
Начни с познания своей кожи
Пигментация | Биология для майоров II
Результаты обучения
- Описать роль меланоцитов в пигментации кожи
На цвет кожи влияет ряд пигментов, включая меланин, каротин и гемоглобин. Напомним, что меланин вырабатывается клетками, называемыми меланоцитами, которые разбросаны по всему базальному слою эпидермиса.Меланин переносится в кератиноциты через клеточную везикулу, называемую меланосомой (рис. 1).
Рис. 1. Относительная окраска кожи зависит от количества меланина, продуцируемого меланоцитами базального слоя и поглощаемого кератиноцитами.
Меланин существует в двух основных формах. Эумеланин, наиболее распространенная форма меланина, существует в черном и коричневом цвете, тогда как феомеланин имеет красный цвет. Темнокожие люди производят больше меланина, чем люди с бледной кожей.Воздействие ультрафиолетовых лучей солнца или в солярии вызывает производство меланина и его накопление в кератиноцитах, поскольку воздействие солнца стимулирует кератиноциты выделять химические вещества, которые стимулируют меланоциты. Накопление меланина в кератиноцитах приводит к потемнению кожи или загару. Это повышенное накопление меланина защищает ДНК клеток эпидермиса от повреждения ультрафиолетовыми лучами и распада фолиевой кислоты, питательного вещества, необходимого для нашего здоровья и благополучия.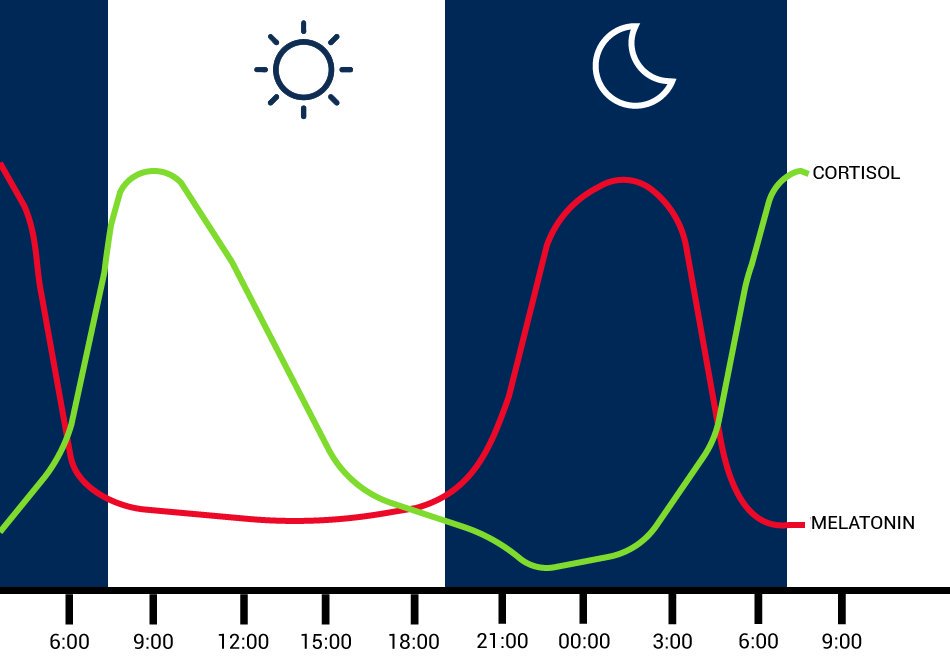 Напротив, слишком много меланина может препятствовать выработке витамина D, важного питательного вещества, участвующего в усвоении кальция.Таким образом, количество меланина, присутствующего в нашей коже, зависит от баланса между доступным солнечным светом и разрушением фолиевой кислоты, а также от защиты от УФ-излучения и производства витамина D.
Напротив, слишком много меланина может препятствовать выработке витамина D, важного питательного вещества, участвующего в усвоении кальция.Таким образом, количество меланина, присутствующего в нашей коже, зависит от баланса между доступным солнечным светом и разрушением фолиевой кислоты, а также от защиты от УФ-излучения и производства витамина D.
Для достижения пика синтеза меланина требуется около 10 дней после первого пребывания на солнце, поэтому люди с бледной кожей вначале обычно страдают солнечными ожогами эпидермиса. Темнокожие люди также могут получить солнечные ожоги, но они более защищены, чем люди с бледной кожей. Меланосомы — это временные структуры, которые в конечном итоге разрушаются путем слияния с лизосомами; Этот факт, наряду с отслаиванием заполненных меланином кератиноцитов в роговом слое, делает загар непостоянным.
Чрезмерное пребывание на солнце может в конечном итоге привести к появлению морщин из-за разрушения клеточной структуры кожи, а в тяжелых случаях может вызвать повреждение ДНК, которое может привести к раку кожи. При нерегулярном скоплении меланоцитов на коже появляются веснушки. Родинки представляют собой более крупные скопления меланоцитов, и, хотя большинство из них доброкачественные, их следует отслеживать на предмет изменений, которые могут указывать на наличие рака (рис. 2).
Рис. 2. Родинки варьируются от доброкачественных скоплений меланоцитов до меланом.Эти структуры населяют ландшафт нашей кожи. (кредит: Национальный институт рака)
Практический вопрос
От чего зависит цвет кожи, и каков процесс, при котором кожа темнеет под воздействием ультрафиолета?
Покажи ответ Пигмент меланин, вырабатываемый меланоцитами, в первую очередь отвечает за цвет кожи. Меланин бывает разных оттенков коричневого и черного. Люди с более темной кожей имеют более темный и более обильный меланин, тогда как люди со светлой кожей имеют более светлый оттенок кожи и меньше меланина.Воздействие УФ-излучения стимулирует меланоциты производить и секретировать больше меланина.
Покровная система
Первое, что видит врач, — это кожа, поэтому осмотр кожи должен быть частью любого тщательного физического обследования. Большинство кожных заболеваний относительно доброкачественные, но некоторые из них, включая меланомы, при отсутствии лечения могут привести к летальному исходу. Пара более заметных нарушений, альбинизм и витилиго, влияют на внешний вид кожи и ее дополнительных органов.Хотя ни один из них не смертельный, было бы трудно утверждать, что они доброкачественные, по крайней мере, для людей, страдающих от этого.
Рис. 3. У людей с витилиго наблюдается депигментация, в результате чего участки кожи становятся более светлыми. Состояние особенно заметно на более темной коже. (кредит: Клаус Д. Питер)
Альбинизм — это генетическое заболевание, которое влияет (полностью или частично) на окраску кожи, волос и глаз. Дефект в первую очередь связан с неспособностью меланоцитов вырабатывать меланин.Люди с альбинизмом, как правило, выглядят белыми или очень бледными из-за нехватки меланина в их коже и волосах. Напомним, меланин помогает защитить кожу от вредного воздействия УФ-излучения. Люди с альбинизмом, как правило, нуждаются в большей защите от УФ-излучения, поскольку они более склонны к солнечным ожогам и раку кожи. Они также более чувствительны к свету и имеют проблемы со зрением из-за отсутствия пигментации на стенке сетчатки. Лечение этого расстройства обычно включает устранение симптомов, например ограничение воздействия ультрафиолетового света на кожу и глаза.При витилиго меланоциты в определенных областях теряют способность производить меланин, возможно, из-за аутоиммунной реакции. Это приводит к потере цвета участков (рис. 3). Ни альбинизм, ни витилиго напрямую не влияют на продолжительность жизни человека.
Другие изменения окраски кожи могут указывать на заболевания, связанные с другими системами организма. Заболевание печени или рак печени могут вызывать накопление желчи и желтого пигмента билирубина, в результате чего кожа становится желтой или желтушной ( jaune — французское слово, означающее «желтый»).Опухоли гипофиза могут вызывать секрецию большого количества меланоцит-стимулирующего гормона (МСГ), что приводит к потемнению кожи. Точно так же болезнь Аддисона может стимулировать выброс избыточного количества адренокортикотропного гормона (АКТГ), который может придавать коже глубокий бронзовый цвет. Внезапное снижение оксигенации может повлиять на цвет кожи, в результате чего кожа сначала станет пепельной (белой). При длительном снижении уровня кислорода темно-красный дезоксигемоглобин становится доминирующим в крови, из-за чего кожа становится синей. Это состояние называется цианозом (кианос — это греческое слово, означающее «синий»).Это происходит, когда подача кислорода ограничена, например, когда кто-то испытывает затруднение дыхания из-за астмы или сердечного приступа. Однако в этих случаях влияние на цвет кожи не имеет ничего общего с ее пигментацией.
Внесите свой вклад!
У вас была идея улучшить этот контент? Нам очень понравится ваш вклад.
Улучшить эту страницуПодробнее
Клетки кожи мыши и человека производят меланин в течение 48-часового цикла — ScienceDaily
Исследователи обнаружили, что кожа мыши и клетки кожи человека производят пигментацию в ответ на солнечный свет в течение 48-часового цикла.Они заметили, что воздействие ультрафиолетового света каждые 2 дня приводит к более темной пигментации с меньшим радиационным повреждением, чем при ежедневном воздействии. Результаты появятся 25 октября в журнале Molecular Cell .
«Повреждающее действие высоких доз ультрафиолетовых лучей известно, но нам было любопытно увидеть влияние частоты воздействия на кожу», — говорит старший автор Кармит Леви, молекулярный генетик из Тель-Авивского университета. «Оказывается, если вы каждый день идете на пляж, вы можете нарушить естественный график и синхронизацию систем защиты кожи.«
Кожа реагирует на ультрафиолетовый свет, высокоэнергетический свет, составляющий часть солнечных лучей, двумя способами: во-первых, путем воспаления и запуска иммунного ответа, восстановления вызванного радиацией разрыва ДНК и размножения своих клеток для защиты более нежные нижележащие слои. Во-вторых, производя меланин, пигмент цвета от коричневого до черного в коже, глазах и волосах, он загорает на коже и действует как естественный солнцезащитный крем при следующем воздействии. Стрессовая реакция на ультрафиолетовое излучение начинается в течение нескольких минут, в то время как производство меланина может начаться через часы или дни.
КомандаЛеви, возглавляемая докторантом Тель-Авивского университета Хагаром Малков-Брогом, хотела понять, как соотносятся друг с другом сроки двух программ защиты кожи. Они подвергали живых мышей воздействию ультрафиолета каждый день, через день и каждые 3 дня. Затем они измерили количество меланина с помощью колориметра и подсчитали количество разрывов ДНК в клетках кожи. Они заметили, что 48-часовой цикл воздействия привел к наиболее темному окрашиванию клеток при минимальном воздействии стресса, даже когда они контролировали общую дозу воздействия.
«Результаты были настолько удивительными, — говорит Леви. «Мы ожидали ежедневной синхронизации защитных циклов клетки».
Леви и ее коллеги, в том числе соавтор и системный биолог Шай Шен-Орр и его аспирант Авелет Альперт из Техниона — Израильского технологического института, заметили, что MITF (фактор транскрипции, связанный с микрофтальмией), по-видимому, играет роль в синхронизация защитных циклов. Ранее было показано, что MITF контролирует выработку меланина и его распространение на окружающие клетки кожи.Они обнаружили, что после одного ультрафиолетового воздействия экспрессия MITF колеблется каждые 48 часов. Другое воздействие через 24 часа, похоже, нарушило этот паттерн выражения.
Затем группаЛеви провела сопоставимый эксперимент с пигментированными клетками человека, полученными из линии раковых клеток, но одобренными в качестве модели для производства пигмента в незлокачественных клетках. Ультрафиолетовое воздействие может активировать выработку меланина только в присутствии других типов клеток кожи, поэтому им приходилось имитировать воздействие ультрафиолетового излучения на культивируемые клетки.Таким образом, они напрямую стимулировали активность MITF в культивируемых клетках, используя расположенный ниже регулятор. Они обнаружили, что 48-часовой цикл стимуляции вызывает наибольшую пигментацию в клетках человека, минимизируя вызванную стрессом пролиферацию.
Команда Леви предполагает, что 48-часовой цикл возник у древних людей, когда мы потеряли защитный мех, что, по мнению многих, произошло, когда мы спустились с деревьев и начали ходить на двух ногах. Другие предположили, что мы потеряли мех из-за жары саванны, в гигиенических целях или в результате полового отбора.
«В то время мы также начали экспрессировать важный рецептор производства пигмента в нашей коже, называемый MC1R, — говорит Леви. «Развитие скоординированных действий программ — другими словами, связывание черт — в ответ на общее давление отбора может дать адаптивное преимущество. Однако мы не уверены, почему мы эволюционировали по 48-часовому циклу, когда древние люди вероятно, подвергались воздействию солнца каждый день. Мы знаем, что витамин D, который вырабатывается кожей при воздействии солнца, стабилен в крови в течение 48 часов после воздействия.Возможно есть ссылка. «
Команда считает, что понимание динамики факторов транскрипции может привести к важным открытиям для правильного выбора времени лечения рака кожи, некоторые из которых, как ранее было показано, зависят от частоты. Их результаты необходимо будет воспроизвести в испытаниях на людях, прежде чем можно будет сделать какие-либо заявления об их терапевтическом потенциале или даже просто о более безопасных привычках загара.
«Мы продолжим изучать эти циклы, и мы хотели бы лучше понять влияние ультрафиолетового излучения на белки в наших клетках и кровотоке», — говорит Леви.«Я думаю, что в нашем теле есть еще« часы », которые нужно открыть».
Это исследование финансировалось Европейским исследовательским советом, Регуляцией генов I-CORE при сложных заболеваниях человека, Израильским научным фондом, Fritz Thyssen Stiftung, Израильским фондом исследований рака, Саломеей (Мика) и Фондом Германа Бергера Z «L, США. -Israel Binational Science Foundation, Премия семьи Штахеров и Фонд Наоми.
История Источник:
Материалы предоставлены компанией Cell Press . Примечание. Содержимое можно редактировать по стилю и длине.
границ | Производство меланинов рекомбинантными микроорганизмами
Введение
Меланины представляют собой группу полимерных пигментов, широко встречающихся в природе (d’Ischia et al., 2015). Это результат катализируемого ферментами окисления фенольных или индольных субстратов. Меланины считаются одними из самых древних пигментов, встречающихся в природе. Эти пигменты были обнаружены в окаменелостях птиц и динозавров (Zhang et al., 2010). Примечательно, что сохранившийся меланин был обнаружен в чернильных мешочках головоногих моллюсков юрского периода (Glass et al., 2012). Таким образом, меланин предлагается в качестве биомаркера для изучения эволюции (Wogelius et al., 2011).
Основными типами меланина являются эумеланин, феомеланин, алломеланины и пиомеланин. Эумеланин является продуктом окисления аминокислоты L-тирозина и / или L-дигидроксифенилаланина (L-DOPA). Полученный полимер имеет коричневый или черный цвет. Феомеланин образуется, когда L-тирозин и / или L-ДОФА окисляются в присутствии L-цистеина, в результате чего получается пигмент красно-желтого цвета.Алломеланины являются результатом окисления одного из следующих соединений: 4-гидроксифенилуксусной кислоты, катехинов, дигидроксинафталина (DHN), γ-глутамил-4-гидроксибензола или тетрагидроксинафталина, протокатехуальдегида и кофейной кислоты. Пиомеланин — это тип меланина, образующийся в результате окисления гомогентизиновой кислоты (HGA) (рис. 1) (Lindgren et al., 2015).
Рисунок 1 . Биохимические реакции, приводящие к синтезу эумеланина, феомеланина, алломеланинов и пиомеланина.
У человека и многих млекопитающих преобладающими пигментами кожи являются эумеланин и феомеланин. Пигментация кожи вызывала интерес с древних времен. Есть упоминания о заболеваниях, влияющих на цвет кожи, таких как витилиго, относящиеся к 2200 году до нашей эры. Только в 1819 году пигментные клетки, называемые хроматофорами, были описаны в исследованиях с кальмарами. Спустя несколько лет подобные структуры были обнаружены в коже и глазах человека. Термин меланин впервые был использован К.P. Robin в 1873 г. и позже были идентифицированы специализированные клетки, ответственные за синтез меланина в коже, меланоциты. Дальнейшие исследования в последующие годы установили существование зерен меланина в меланоцитах и процесс переноса этих структур в эпителиальные клетки (Westerhof, 2006).
Благодаря своему химическому составу меланины обладают отчетливыми физико-химическими свойствами. Таким образом, эти полимеры могут действовать как поглотители ультрафиолетового света, рентгеновского и γ-излучения, катиониты и аморфные полупроводники (Sarna et al., 1976; делла-Чиоппа и др., 1990; Крол и Либлер, 1998; Rózanowska et al., 1999; Ambrico et al., 2014). Также было показано, что меланины обладают антиоксидантной и противовирусной активностью (Montefiori and Zhou, 1991; Nofsinger et al., 2002). Разнообразные применения и продукты, полученные из меланинов, зависят от получения этих полимеров по относительно низкой цене и в большом количестве. Меланины могут быть извлечены из тканей растений и животных или получены путем химического синтеза. Однако эти процессы относительно дороги и в некоторых случаях неустойчивы (Saini and Melo, 2015).Потенциально жизнеспособная альтернатива получению меланинов основана на культуре меланогенных микроорганизмов. Преимущество этого метода в том, что он масштабируем и обеспечивает хороший выход меланинов. Этот подход может быть улучшен путем применения методов генной инженерии для увеличения естественной меланогенной способности некоторых организмов или создания новых продуцирующих меланин штаммов. Наиболее распространенная генетическая модификация для усиления / создания продуцирующего штамма включает экспрессию генов, кодирующих ферменты, участвующие в окислении предшественников меланина.
Ферменты, участвующие в образовании меланина
Фермент-зависимое окисление фенольных или индольных соединений является первым шагом, ведущим к образованию меланинов. Меланогенные ферменты принадлежат в основном к семействам белков тирозиназы и лакказы. Тирозиназы — наиболее распространенный тип ферментов, связанных с меланогенезом. Эти ферменты могут использовать как моно, так и дифенольные соединения в качестве субстратов. Примерами этих субстратов являются L-тирозин, L-ДОФА и катехины. Тирозиназы представляют собой монооксигеназы с двухъядерным каталитическим центром из меди.Эти ферменты катализируют орто-гидроксилирование монофенолов (активность крезолазы), а также окисление катехолов (активность катехолазы), образуя продукты орто-хинона (Garcia-Molina et al., 2007) (рис. 1). Фермент тирозиназа катализирует гидроксилирование L-тирозина до L-DOPA с использованием молекулярного кислорода, а затем окисляет это соединение до допахрома, который неферментативно полимеризуется с образованием меланина (Ito, 2003). По аминокислотной последовательности и функциональным особенностям микробные тирозиназы можно разделить на пять основных групп (Fairhead and Thöny-Meyer, 2012).Тирозиназа из Streptomyces sp. входит в одну из этих групп. Их объединяет потребность в белке-шапероне, который вставляет атомы меди в активный центр тирозиназы. Напротив, тирозиназы из бактерий, таких как Rhizobium etli, Bacillus megaterium и Bacillus thuringiensis , не требуют шаперона для встраивания меди в активный центр. Лакасы — еще одна группа ферментов, участвующих в меланогенезе. Эти ферменты не связаны с тирозиназами, но также являются медьзависимыми оксидоредуктазами.Лакказы были обнаружены в бактериях, грибах и растениях (Valderrama et al., 2003). Фермент гидроксилаза 4-гидроксифенилуксусной кислоты (4-HPA) участвует в катаболизме 4-HPA у бактерий. Эта группа ферментов демонстрирует широкий диапазон субстратов, они могут гидроксилировать различные одноатомные и двухатомные фенолы (Prieto et al., 1993). 4-HPA-гидроксилаза представляет собой двухкомпонентную флавинадениндинуклеотидную (FAD) -зависимую монооксигеназу (Gibello et al., 1995).
Биологические функции меланинов
Меланины обнаружены у видов из трех сфер жизни: архей, бактерий и эукариев.Эти пигменты выполняют разнообразные функции, связанные с выживанием многих видов в естественной среде обитания (рис. 2). У человека эумеланин и феомеланин участвуют в защите от УФ-излучения (Coelho et al., 2009). Еще одно важное защитное действие этих пигментов включает их функции улавливателей свободных радикалов. Эта деятельность снижает производство активных форм кислорода (Meredith and Sarna, 2006). Меланин также содержится в глазах и мозге людей и других позвоночных.Однако роль пигмента в этих органах до конца не изучена. У птиц меланин участвует в окраске перьев. Эта функция связана с передачей сигналов, влияя на репродуктивную пригодность (McGraw, 2008). Темный цвет, придаваемый меланином, выполняет функцию терморегуляции, поглощая лучистую энергию в организмах, таких как земноводные и рептилии (Clusella-Trullas et al., 2007). У некоторых видов моллюсков, осьминогов и кальмаров образование и выделение чернил является отличительным защитным механизмом.Основным компонентом этого продукта является эумеланин, который у этих организмов синтезируется чернильной железой (Palumbo, 2003). У насекомых образование меланина связано со склеротизацией кутикулы. Кутикула — это внешний компонент экзоскелета насекомых. Меланогенез приводит к затвердеванию кутикулы, обеспечивая защиту от физических повреждений. Кроме того, меланизация у насекомых действует как защитный механизм от патогенов. При инфицировании образование меланина вокруг патогена блокирует его распространение (Vavricka et al., 2014). У грибов меланизация — общий признак, связанный с патогенезом. В этих организмах предшественники меланина включают DHN, HGA, γ-глутаминил-4-гидроксибензол, катехол и тирозин. Помимо фотозащиты и антиоксидантной активности, у грибов меланины также участвуют в обеспечении устойчивости к химическим и механическим воздействиям (Cordero and Casadevall, 2017). Кроме того, меланин был предложен в качестве пигмента для сбора энергии у грибов. Было установлено, что сублетальные дозы гамма-лучей вызывают усиленное повышение уровня НАДФН и скорости роста у некоторых видов грибов (Дадачова и др., 2007). Производство меланина бактериями было идентифицировано у видов из Rhizobium, Streptomyces, Marinomonas, Pseudomonas, Serratia и Bacillus . У этих организмов меланин участвует в вирулентности, а также в защите от ультрафиолета и окислителей (Trias et al., 1989; Patel et al., 1996; López-Serrano et al., 2004; Piñero et al., 2007). ; Manivasagan et al., 2013).
Рисунок 2 . Основные биологические функции меланинов.
Применение меланинов
Меланины имеют очень сложную полимерную структуру, что приводит к различным химическим и физическим свойствам. Помимо блокирования УФ-света, они также могут поглощать рентгеновское и γ-излучение (Hill, 1992). Эти полимеры также обладают способностью поглощать активные формы кислорода и свободные радикалы, а также проявлять окислительно-восстановительное поведение (Liu et al., 2015). Меланин — аморфный полупроводник, поэтому он оценивается как компонент электронных схем, батарей, а также солнечных элементов (Bothma et al., 2008; Ким и др., 2013; Ambrico et al., 2014). В настоящее время для этих целей используются неорганические полупроводники. Однако они оказывают сильное воздействие на окружающую среду и относительно высокую стоимость. Напротив, органические полупроводники, такие как меланины, не имеют тех же недостатков и их легче обрабатывать. Дополнительным преимуществом меланина перед традиционными полупроводниками является его биосовместимость, что делает его пригодным для использования в имплантируемых устройствах.
В другом типе применения меланин использовался в качестве шаблона для синтеза наноструктур и наночастиц серебра или золота, которые могут быть использованы в пищевой и медицинской промышленности (Apte et al., 2013; Патил и др., 2018). Меланин также был оценен как добавка синтетического полимера. Было обнаружено, что добавление эумеланина к полиметилметакрилату (ПММА) вызывает значительное увеличение термостабилизации (Shanmuganathan et al., 2011). Потребуются дальнейшие исследования, чтобы показать, можно ли использовать меланины для улучшения свойств других синтетических полимеров. В аналогичном исследовании было продемонстрировано, что алломеланин может быть включен в качестве красителя в гидрогель мягких контактных линз (Ahn et al., 2019). По сравнению с синтетическими красителями использование алломеланина дает преимущество в виде антибактериальной и антиоксидантной активности. В области медицины сообщалось, что клеток Escherichia coli , экспрессирующих ген melA , кодирующий тирозиназу из Rhizobium etli , можно использовать для фотоакустической визуализации, метода с улучшенным соотношением глубины к разрешению по сравнению с оптическим отображением. (Папроски и др., 2015). Такой подход может улучшить понимание бактериальных патогенных процессов.В другом приложении для визуализации меланин использовался в качестве контрастного вещества в датчиках магнитно-резонансной томографии (Williams, 1994). Кожные и косметические применения меланина включают его использование для окрашивания волос. Широко используемые синтетические окислительные красители вызывают повреждение волос, и с ними нелегко обращаться. Напротив, процесс, основанный на использовании предшественников меланина, которые могут связываться с волосами после окисления воздухом, имеет то преимущество, что не вызывает повреждений и является более безопасным (Koike and Ebato, 2013).
Меланины могут действовать как хелаторы металлов, и эту способность можно использовать в экологических приложениях.Связывание металлов с меланином включает множественные координационные связи между гидроксильными, аминными и карбоксильными функциональными группами в этом полимере. В исследовании биоремедиации почвы было показано, что меланин из грибов эффективно связывает тяжелые металлы, такие как цинк и свинец (Fogarty and Tobin, 1996). В другом исследовании меланин был синтезирован с использованием тирозиназы, экстрагированной из растения Amorphophallus campanulatus , и L-DOPA в качестве субстрата. Было установлено, что меланин может эффективно удалять уран из водного раствора (Saini, Melo, 2013).
Следует отметить, что предыдущие кейсы все еще находятся в стадии разработки и еще не были коммерциализированы. Однако есть несколько примеров коммерчески доступных продуктов, содержащих меланин. В настоящее время меланин используется в основном в качестве красителя для линз солнцезащитных очков. В этом случае неизвестно, какие химические красители заменены меланином, но естественное происхождение пигмента и способность уменьшать видимый свет высокой энергии выделены как преимущество (https: // espeyewear.com /). Коммерческий продукт, связанный с дерматологией, представляет собой солнцезащитный крем для сухой кожи, содержащий чернила кальмара в качестве антиоксиданта. Преимущество этого продукта перед конкурирующими солнцезащитными кремами заключается в ожидаемом уменьшении раздражения кожи по сравнению с синтетическими красителями (https://chicet.com/product/melanin-sunscreen-for-dry-skin/).
Производство меланинов природными меланогенными организмами
Текущие и потенциальные применения меланинов зависят от возможности получения этих пигментов из обильных и относительно недорогих источников.Эти продукты могут быть извлечены из природных источников, таких как ткани животных или растений, относительно недорогими методами. Однако эти источники обычно содержат смесь различных типов меланинов и родственных веществ, которые усложняют процедуры очистки и могут давать продукт переменного состава. Эти полимеры также могут быть получены путем химического или ферментативного окисления фенольных или индольных субстратов (Saini and Melo, 2015). Эти методики позволяют получать меланины с высокой степенью чистоты, но при относительно высоких затратах.Другой вариант получения этих полимеров основан на культуре естественных микробов, продуцирующих меланин, или микробов, которые были генетически сконструированы для производства меланинов. Такой подход имеет потенциал для создания этого класса продуктов с относительно низкой стоимостью и высоким выходом.
Хотя в этом обзоре основное внимание уделяется сконструированным микроорганизмам, в него включено краткое описание усилий по разработке процессов производства меланина с помощью естественных меланогенных организмов.Производство меланина наблюдается у нескольких видов микроорганизмов и грибов как в естественной среде, так и в лабораторных условиях выращивания. Виды организмов с меланогенной способностью, которые использовались для разработки производственных процессов, включают Pseudomonas stutzeri, Gliocephalotrichum simplex, Rhizobium sp., Brevundimonas sp., Aspergillus fumigatus, Bacillus safensis Jalmi et al., 2012; Чжао и Тонг-Суо, 2012; Ганеш Кумар и др., 2013; Surwase et al., 2013; Guo et al., 2014; Мадхусудхан и др., 2014; Тарангини и Мишра, 2014; Raman et al., 2015). Процессы получения меланина с помощью этих организмов обычно включают статистические экспериментальные методы, направленные на определение условий культивирования и компонентов среды, которые положительно влияют на продуктивность (Zhao and Tong-Suo, 2012; Tarangini and Mishra, 2014). Было обнаружено, что параметры культуры, такие как температура, pH, концентрация кислорода и предшественников меланина, способствуют продуктивности.Разработанные процессы позволили производить меланин в титрах от 0,01 до 13,7 г / л (Guo et al., 2014; Raman et al., 2015). В большинстве этих процессов наблюдалась положительная корреляция с производством полимера при увеличении в питательной среде количества L-тирозина или компонентов, которые его содержат. Таким образом, полученный полимер, вероятно, является эумеланином. Однако в большинстве случаев питательные среды включают дрожжевой экстракт или гидролизаты белка. Следовательно, в процессе образования меланина некоторые компоненты среды, помимо L-тирозина, могут быть включены в полимер, давая пигмент, который не является чистым эумеланином.Это важный недостаток большинства процессов, разработанных с меланогенными организмами, которые требуют сложных сред для роста и производства.
Производство меланинов с помощью генетически модифицированных микроорганизмов
Экспериментальные методологии, известные как методы генной инженерии, позволяют модифицировать генетический материал микробов с целью усиления или создания способности производить определенные молекулы. В настоящее время возможно генетическое конструирование разнообразных микроорганизмов, и это число постоянно растет.Применение технологии секвенирования ДНК в сочетании с биохимическим анализом позволило выяснить пути и конкретные гены, связанные с производством меланинов. Эти знания и технологии являются основой для создания рекомбинантных микробов для увеличения выработки меланина и для передачи этой способности немеланогенным микроорганизмам.
Получение меланогенных микроорганизмов путем экспрессии генов, кодирующих тирозиназы
Далее следует обзор и анализ достижений, связанных с созданием рекомбинантных штаммов микробов и производственными процессами для синтеза меланинов.О первом примере рекомбинантного меланогенного микроба сообщалось о бактерии E. coli . Этот организм был модифицирован для экспрессии генов актиномицета Streptomyces antibioticus . В S. antibioticus локус mel включает два гена, mel и ORF438, которые необходимы для продукции меланина. Было показано, что рекомбинантный штамм E. coli продуцирует эумеланин из L-тирозина в чашках с агаром и жидких культурах, но титры не сообщаются.Интересно, что также было продемонстрировано, что синтетические неприродные аминокислоты, такие как N-ацетил-L-тирозин и этиловый эфир L-тирозина, могут использоваться в качестве субстратов для тирозиназы S. antibioticus , давая синтетические меланины (della-Cioppa и др., 1990). В другом сообщении локус mel из S. antibioticus также был использован для создания рекомбинантного штамма E. coli , полученного из JM109. Ген mel был помещен под транскрипционный контроль промотора фага T5 и двух операторов lac .Культивирование этого рекомбинантного штамма в среде LB привело к выделению 0,4 г / л эумеланина (таблица 1). Извлечение эумеланина из культуральной среды основывалось на осаждении путем доведения pH до 3,0 с последующим растворением его в дистиллированной воде при pH 8,0. После этой процедуры была проведена жидкостная хроматография на Sephadex LH-20. Очищенный эумеланин использовали для изучения влияния присутствия этого полимера на антимикробную активность нескольких антибиотиков. Было установлено, что эумеланин снижал действие антибиотика на E.coli ампициллина, канамицина, полимиксина B и тетрациклина в зависимости от дозы (Lin et al., 2005). Помимо клинической важности таких результатов, наблюдаемый ответ может быть использован для выбора рекомбинантных штаммов с более высоким уровнем продуцирования меланина на основе устойчивости к антибиотикам.
Таблица 1 . Разработаны штаммы микробов для производства меланинов.
В другом раннем примере было показано, что штамм 4D11 Bacillus thuringiensis продуцирует меланин при культивировании в течение нескольких часов с L-тирозином при 42 ° C (Ruan et al., 2004). Эти результаты показали, что этот организм должен содержать в своем геноме ген, кодирующий тирозиназу. Поскольку последовательность генома B. thuringiensis 4D11 не была известна, была разработана стратегия клонирования, основанная на ожидаемом сходстве последовательности с геном тирозиназы из Bacillus cereus 10987. На основе гена тирозиназы была сконструирована пара праймеров для ПЦР. последовательность из B. cereus 10987 и использовалась для амплификации фрагмента ДНК размером 1179 п.н. из B.thuringiensis 4D11 очищенная ДНК. Анализ последовательности показал, что этот фрагмент ДНК демонстрирует 99% сходства аминокислотной последовательности с тирозиназой из B. cereus 10987. Продукт ПЦР клонировали в плазмиде pGEM-7zf под контролем промотора lac . Штамм E. coli DH5α трансформировали этой плазмидой, и было показано, что рекомбинантный штамм продуцирует эумеланин с титром 5,6 г / л при выращивании в казеиновой жидкой среде (таблица 1). Интересно, что также было установлено, что этот рекомбинантный штамм показал значительно более высокую выживаемость по сравнению с DH5α в экспериментах по воздействию УФ-излучения (Ruan et al., 2005). Эти результаты показывают, как в дополнение к способности продуцировать меланин в качестве биотехнологического продукта, гетерологичная экспрессия гена, кодирующего тирозиназу, может увеличить способность хозяина противостоять УФ-излучению. Это следствие выработки меланина, признак, который может быть полезным в случае микроорганизмов, используемых в этой области, таких как B. thuringiensis . Возможность инженерных микробов выживать в средах с высоким УФ-излучением также актуальна для будущих космических приложений.Считается, что микробы необходимы для поддержания жизни человека, обеспечивая пищу, полезные химические вещества и перерабатывая отходы в космических полетах дальнего действия и проектах по колонизации планет (Horneck et al., 2010; https://blogs.scientificamerican.com/observations/ микробы-могли-быть-ключом-к-марсу-миссии /). Меланин также может поглощать рентгеновские и γ-лучи, что может увеличить выживаемость искусственно созданных микробов в окружающей среде за пределами нашей планеты.
Среди почвенных бактерий Rhizobium etli особенно важен для сельского хозяйства, поскольку он может связывать азот, когда образует клубеньки в корне растения Phaseolus vulgaris .Было установлено, что эта бактерия может продуцировать меланин в симбиотических узелках, и ген, кодирующий тирозиназу, был идентифицирован в симбиотической плазмиде ( melA ) (González et al., 2003; Piñero et al., 2007). Ген melA был клонирован в векторе экспрессии pTrc99A под контролем сильного промотора trc , и полученная плазмида pTrc melA была трансформирована в E. coli . Рекомбинантный штамм E. coli продуцировал эумеланин, когда L-тирозин использовался в качестве субстрата при 30 ° C и в гораздо меньшем количестве при 37 ° C (Cabrera-Valladares et al., 2006). Также было отмечено, что синтез меланина происходил только во время стационарной фазы культивирования. Во время клонирования гена melA было обнаружено, что колония рекомбинантной E. coli в среде, содержащей L-тирозин, имела более темный цвет по сравнению с остальными колониями. После секвенирования ДНК гена melA в этом клоне было определено, что он имел спонтанную мутацию с заменой одного нуклеотида, когда остаток Asp535 был заменен на остаток Gly в ферменте тирозиназы MelA.Эта мутантная версия MelA была названа MutMelA. Дальнейшая характеристика показала, что продукция эумеланина в жидких культурах начинается раньше в культурах E. coli , экспрессирующих MutmelA, по сравнению со штаммом, экспрессирующим версию этого фермента дикого типа. Для разработки и оптимизации процесса производства эумеланина было проведено исследование по определению оптимальных условий для синтеза пигментов в жидких культурах с рекомбинантным штаммом E. coli , экспрессирующим MutmelA. Определяли влияние концентрации антибиотика на давление отбора плазмиды, изопропил-d-тиогалактопиранозида (IPTG) в качестве индуктора гена, температуры культивирования и pH на концентрацию эумеланина.Наилучшие условия для производства в биореакторе заключались в использовании 0,1 ммоль / л IPTG, температуре культивирования 30 ° C и изменении pH среды с 7,0 до 7,5 в начале фазы продуцирования эумеланина. Всего в культуральную среду добавляли 6 г / л L-тирозина в качестве предшественника эумеланина. В этих условиях наблюдали 100% -ный выход превращения L-тирозина в эумеланин с конечным титром 6 г / л (таблица 1) (Lagunas-Muñoz et al., 2006). Эти результаты подчеркивают важность оптимизации условий культивирования как фактора для достижения максимального урожая и продуктивности рекомбинантного меланогенного штамма.
В ходе биоразведочного исследования микроорганизмы, способные продуцировать меланин, были выделены из образцов почвы в Китае. Один из таких микробов был идентифицирован как Streptomyces kathirae SC-1, он показал самую высокую способность к продукции меланина среди всех изолятов. Метод поверхностного отклика был использован для оптимизации среды и условий роста, что позволило производить 13,7 г / л меланина (Guo et al., 2014). Важно отметить, что питательная среда, использованная в этом исследовании, включала дрожжевой экстракт, который представлял собой смесь предшественников меланина.Следовательно, полученный полимер должен быть охарактеризован, чтобы определить его химический состав, чтобы определить тип производимого меланина. Чтобы лучше понять меланогенез в этом организме, новая тирозиназа была очищена до гомогенности. Это фермент массой 30 кДа, показывающий K m для L-DOPA и L-тирозина 0,42 и 0,25 мМ соответственно. Неполная аминокислотная последовательность этой тирозиназы была использована для конструирования праймеров, которые позволили амплифицировать кодирующий ген melC и его промоторную область.Анализ последовательности промоторной области выявил два предполагаемых промотора: P skmel и P 135 . Ген melC был клонирован под транскрипционным контролем любого предполагаемого промотора и конститутивного промотора Perm E * в репликативной плазмиде pIJ86, и полученные конструкции трансформировали в S. lividans и S. kathirae . Рекомбинантные штаммы S. lividans были охарактеризованы, и было определено, что P skmel является функциональным промотором для melC .Рекомбинантные штаммы S. kathirae культивировали в условиях продуцирования меланина. Было определено, что штаммы, экспрессирующие melC из Perm E * или P skmel , продуцировали 24,9 и 28,8 г / л меланина соответственно (таблица 1) (Guo et al., 2015). Следует отметить, что это самые высокие титры меланина, о которых сообщалось на сегодняшний день, что подчеркивает потенциал применения методов генной инженерии для дальнейшего повышения производственной способности меланогенных организмов (Таблица 1).Эта производственная система имеет потенциал для дальнейшей оптимизации, в частности, в отношении состава питательной среды. Среда содержит относительно большое количество дрожжевого экстракта (37 г / л), который является дорогостоящим компонентом. Дрожжевой экстракт может усложнить процедуры очистки меланина, и некоторые из его компонентов могут реагировать с предшественниками меланина, давая полимер, не полностью состоящий из предшественника L-тирозина. По этим причинам поиск питательной среды, содержащей только соли и простой источник углерода, должен стать целью будущих исследований для улучшения существующей схемы производства.
Фенольные альдегиды — это соединения, находящие применение в химической и пищевой промышленности. Микробиологическое производство этого класса химикатов в E. coli включает экспрессию гетерологичных генов и другие модификации метаболической сети. В рамках исследования по созданию штамма E. coli для синтеза фенольных альдегидов этот организм был модифицирован для производства кофейной кислоты из L-тирозина. Это включает экспрессию тирозинаммиаклиазы (TAL) для преобразования L-тирозина в кумаровую кислоту и p -кумарат-3-гидроксилазу (C3H) с образованием кофейной кислоты (рис. 3).В этих экспериментах наблюдался темный пигмент, имеющий характеристики меланина. Этот меланин кофейной кислоты, вероятно, образуется в результате окисления катехиновой части некоторыми оксидазами, кодируемыми в геноме E. coli . Было также замечено, что протокатехуальдегид, добавленный к культуральной среде и инкубированный с E. coli , давал пигмент меланин коричневого цвета, тогда как меланин кофейной кислоты был черным. В рамках этой работы гены, кодирующие ферулоил-КоА-синтетазу (FCS) и еноил-КоА-гидратазу / альдолазу (ECH) из Burkholderia glumae BGR1, были экспрессированы в E.coli (рисунок 3). Рекомбинантный штамм приобрел способность превращать кофейную кислоту в протокатехуальдегид. В рамках этого исследования было обнаружено, что в присутствии 5 мМ кофейной кислоты E. coli BL21 (DE3) дикого типа производила 0,15 г / л меланина (Таблица 1). Когда такое же количество кофейной кислоты было добавлено к культуре с рекомбинантным штаммом, экспрессирующим fcs и ech , меланин производился с большей скоростью, достигая титра 0,2 г / л (Jang et al., 2018).Этот меланин химически не охарактеризован, вероятно, это полимер, состоящий из смеси компонентов кофейной кислоты и протокатехуальдегида. Эти результаты демонстрируют продукцию меланинов кофейной кислоты и протокатехуальдегида с помощью рекомбинантной E. coli . Очевидно, что активности FCS и ECH влияют на синтез меланина и / или предшественников меланина в этом штамме, однако механизмы наблюдаемых результатов еще не полностью поняты. Химическая характеристика продуцируемого меланина должна обеспечить дальнейшее понимание химических предшественников, участвующих в его образовании.Также представляет интерес идентификация нативного фермента из E. coli , который участвует в окислении кофейной кислоты и протокатехуальдегида, что приводит к их полимеризации в меланин. Клонирование и сверхэкспрессия гена, кодирующего эту еще не идентифицированную оксидазу, должны позволить улучшить штаммы, продуцирующие меланин. В последующем отчете было продемонстрировано, что меланин на основе протокатехуальдегида можно использовать для окрашивания мягких контактных линз (Ahn et al., 2019). Антибактериальная и антиоксидантная активность меланинов должна иметь преимущество при таком применении по сравнению с химически синтезированными красителями.
Рисунок 3 . Метаболические пути и экспрессируемые гены, связанные с синтезом меланинов с помощью сконструированных микроорганизмов. Пунктирные стрелки указывают на две или более ферментативных реакции. Подчеркнутые гены были сверхэкспрессированы из плазмид. PTS, белок транспорта глюкозы фосфотрансферазной системы; Гли, глицерин; Gly3P, глицерин-3-фосфат; G6P, глюкозо-6-фосфат; E4P, D-эритрозо-4-фосфат; PEP, фосфоенолпируват; DAHP, 3-дезокси-D- арабино -гептулозонат 7-фосфат; HPP, 4-гидроксифенилпируват; ЦДХ, хоризмат; ANT, антранилат; PPA, фенилпируват; HPPD, гидроксифенилпируватдегидрогеназа; HGO, гомогентизат-1,2-диоксигеназа; L-Тир, L-тирозин; L-Phe, L-фенилаланин; L-Trp, L-триптофан; tktA , ген, кодирующий транскетолазу; aroG fbr , ген, кодирующий устойчивую к ингибированию с помощью обратной связи DAHP-синтазу; trpEG , гены, кодирующие антранилатсинтазный компонент I; trpD9923 представляет собой мутантную версию trpD , вызывающую потерю активности антранилатфосфорибозилтрансферазы и сохраняющую активность антранилатсинтазы; tyrC , ген, кодирующий циклогексадиенилдегидрогеназу; C3H, ген, кодирующий p -кумарат-3-гидроксилазу; TAL, ген, кодирующий тирозин-аммиак-лиазу; FCS, ген, кодирующий форму ферулоил-КоА синтетазы B.glumae BGR1; ECH, ген, кодирующий еноил-CoA гидратазу / альдолазу из B. glumae BGR1; antABC , кодирует концевые оксигеназные и редуктазные компоненты антранилат-1,2-диоксигеназы из P. aeruginosa PAO1; pheA CM , ген, кодирующий хоризматмутазный домен из хоризматмутазы-префенатдегидратазы; Mut melA , ген, кодирующий мутантную версию тирозиназы из R. etli .
Случайный мутагенез для отбора меланогенного штамма
Штамм F6 почвенной бактерии Pseudomonas putida обнаружил способность продуцировать меланин при выращивании в среде, содержащей L-тирозин.Чтобы понять роль генов, участвующих в меланогенезе, был проведен мутагенез транспозонов. В результате были получены два мутанта с повышенной производительностью меланина. Один из таких мутантов (F6-HDO) продуцировал 0,35 г / л меланина, что соответствует 6-кратному увеличению по сравнению с P. putida F6 (Таблица 1). Интересно, что этот мутант проявлял более высокую устойчивость к УФ-свету и H 2 O 2 по сравнению с диким типом. Генетический анализ показал, что мутагенез транспозонов нарушил ген, кодирующий 1,2-диоксигеназу HGA (HGO).Этот фермент превращает HGA в 4-малеилацетоацетат как часть пути разложения. Следовательно, ожидается, что эта мутация снизит потребление HGA HGO. Этот результат указывает на то, что HGA является предшественником алломеланина в этом мутантном штамме (Рисунок 3) (Nikodinovic-Runic et al., 2009). Синтез HGA происходит по пути биосинтеза L-тирозина. Промежуточный 4-гидроксифенилпируват (HPP) превращается в HGA под действием фермента гидроксифенилпируватдегидрогеназы (HPPD) (рис. 3). Это пример, когда случайный мутагенез был использован для выделения мутантов с улучшенным меланогенезом.Важным преимуществом работы с меланогенными организмами является простота процесса идентификации мутантов, поскольку их можно обнаружить визуально. Исследования, подобные этому, необходимы для выявления новых генов, участвующих в процессе меланогенеза. Как только меланогенные пути идентифицированы, можно применить рациональную стратегию для увеличения естественной меланогенной способности или передачи ее другому организму.
Случайный мутагенез — относительно простой метод улучшения штаммов, но он ограничен организмами, которые уже обладают природной способностью продуцировать меланин.Обычно сайт и тип мутации в улучшенном меланогенном организме неизвестны, что ограничивает использование рациональных стратегий для дальнейшего улучшения штамма. Кроме того, генетические изменения, вызванные случайным мутагененисом, могут быть нестабильными, поэтому штамм может вернуться к фенотипу с низким продуцентом. Решение этих проблем может быть основано на секвенировании генома улучшенного штамма, что дает информацию о типе мутации, а также о генах и путях, участвующих в наблюдаемом фенотипе.Эта информация может быть использована для «обратного проектирования» меланогенного организма путем использования методов генной инженерии для повторного введения идентифицированных мутаций. Эта стратегия может использоваться для отделения генетических изменений, связанных с улучшенным фенотипом, от тех, которые могут быть вредными или возникать в результате генетической нестабильности.
В предыдущих примерах описаны рекомбинантные штаммы и процессы превращения различных ароматических соединений в меланины. Добавляя различные предшественники меланина в культуральную среду, тирозиназы могут использовать их в качестве субстратов для создания специфических пигментов (таблица 1).Такие процессы могут демонстрировать высокую производительность. Кроме того, используя различные ароматические предшественники, можно производить различные типы меланинов. Несмотря на эти преимущества, можно рассмотреть несколько недостатков. Одна из них — относительно высокая стоимость использования чистых предшественников меланина. Однако возникает другая проблема, когда используются нечистые и относительно недорогие предшественники меланина, такие как дрожжевой экстракт или гидролизаты белка. Использование сложных сред может приводить к изменчивости в составе продуцируемых меланинов, поскольку эти культуральные среды могут содержать разнообразные и переменные количества соединений, которые могут быть субстратами тирозиназ или могут реагировать с молекулами предшественников меланина.Кроме того, использование неопределенных сред делает процессы очистки меланина более сложными и дорогими.
Генетические модификации, используемые для создания ранее описанных штаммов-продуцентов, в основном основаны на клонировании генов, кодирующих тирозиназу, на плазмиде экспрессии с несколькими копиями (Таблица 1). Этот подход оказался эффективным для получения титров в граммах на нескольких примерах. Однако еще предстоит определить, может ли хромосомная экспрессия этих генов привести к появлению эффективных продуцирующих штаммов, имеющих то преимущество, что не требуется использование антибиотиков для отбора плазмид.Следует отметить, что E. coli часто выбирается в качестве хозяина продукции меланинов. Вероятно, это результат обширного набора инструментов генетической и метаболической инженерии, доступных для этого организма (Таблица 1). Однако следует принимать во внимание потенциальные преимущества инженерии природных меланогенных организмов. Самый высокий титр меланина, о котором сообщалось на сегодняшний день, был получен в процессе с рекомбинантным штаммом S. kathirae . Можно было ожидать, что меланогенные организмы обладают физиологическими особенностями, которые делают их более подходящими в качестве производственных штаммов.Например, специализированные метаболические пути для образования предшественников меланина, усиленные транспортные процессы для интернализации субстратов тирозиназы или для выделения меланина.
Метаболическая инженерия, применяемая для производства меланинов из простых источников углерода путем увеличения предложения прекурсоров
Одно из возможных решений упомянутых выше проблем включает создание штаммов микробов для полного синтеза меланинов из простых источников углерода.Этот подход основан на применении стратегий метаболической инженерии для увеличения потока в путь шикимата, который обеспечивает предшественники ароматических аминокислот. В одном примере методы метаболической инженерии были применены для создания штамма E. coli , способного продуцировать предшественник эумеланина L-тирозин из глюкозы (Chávez-Béjar et al., 2008). Этот штамм был модифицирован для увеличения притока углерода к пути биосинтеза L-тирозина путем сверхэкспрессии генов, кодирующих нечувствительную к обратной связи версию фермента 3-дезокси-D- арабино -гептулозонат-7-фосфат (DAHP) синтазу ( aroG ). fbr ), циклогексадиенилдегидрогеназа (TyrC) из Zymomonas mobilis и хоризматмутазный домен из нативного фермента хоризматмутаза-префенатдегидратаза.Кроме того, этот штамм экспрессировал ген Mut melA , кодирующий тирозиназу MutMelA (фигура 3). Этот штамм мог синтезировать эумеланин из глюкозы. Однако было определено, что активность MutMelA истощает пул L-тирозина, вызывая нарушение роста клеток. Фермент тирозиназа требует Cu в качестве кофактора для активности. Следовательно, этот элемент был исключен из среды в течение первой половины культивирования, чтобы избежать истощения L-тирозина под действием MutMelA. Фазу продукции эумеланина начинали добавлением в среду CuSO 4 , вызывая активацию тирозиназы.Эта стратегия была использована в биореакторных культурах со средой, содержащей 60 г / л глюкозы в качестве единственного источника углерода. За 120 ч продуцировалось 3,2 г / л эумеланина (таблица 1) (Chávez-Béjar et al., 2013). Эти результаты были первым примером применения метаболической инженерии для создания штамма для полного синтеза эумеланина. Это исследование предоставило полезную информацию о потенциальных негативных последствиях для физиологии клеток, возникающих в результате высокого уровня экспрессии тирозиназы. Эта проблема была решена путем принятия отложенной активации гетерологичного фермента.Альтернативное решение может быть основано на точном контроле индукции генов на определенной фазе производственной культуры.
Во время характеристики фермента MutMelA было определено, что помимо L-тирозина он также может использовать катехол в качестве субстрата. Таким образом, этот фермент можно использовать для синтеза катехолового меланина. Чтобы проверить эту идею, был разработан процесс биоконверсии со штаммом E. coli , экспрессирующим MutMelA и растущим в среде, содержащей глицерин 40 г / л в качестве источника углерода и катехол 0.85 г / л в качестве субстрата тирозиназы. Через 54 часа было произведено 0,29 г / л катехолового меланина. Чтобы улучшить этот процесс, была проведена оценка метаболической инженерии для создания штамма, способного генерировать катехоловый меланин из простого источника углерода. Применяемая стратегия основана на использовании сконструированного штамма E. coli , который может продуцировать катехол из простого источника углерода (Balderas-Hernández et al., 2014). Штамм E. coli W3110 trpD9923 является мутантом пути биосинтеза L-триптофана, который продуцирует промежуточный антранилат (Yanofsky et al., 1971). Этот штамм был модифицирован для увеличения притока углерода к антранилату за счет сверхэкспрессии генов aroG fbr и tktA , кодирующих нечувствительную к обратной связи версию DAHP-синтазы и транскетолазы, соответственно (рис. 3). Эти модификации вызывали двукратное увеличение титра антранилата в колбовых культурах (Balderas-Hernández et al., 2009). Этот штамм был дополнительно модифицирован экспрессией генов antABC , кодирующих антранилат 1,2-диоксигеназу из Pseudomonas aeruginosa PAO1.Этот фермент катализирует превращение антранилата в катехол (рис. 3). На заключительном этапе конструирования штамма ген Mut melA был интегрирован в хромосому на участке гена lacZ . Полученный штамм оценивали в биореакторных культурах в масштабе 1 литр. Питательная среда содержала глицерин 40 г / л в качестве источника углерода. В качестве источника углерода вместо глюкозы был выбран глицерин, поскольку первый не потребляет предшественник ароматических соединений PEP во время его интернализации и фосфорилирования.Кроме того, глицерин является относительно недорогим, распространенным и возобновляемым источником углерода и энергии, который получается в основном как побочный продукт при производстве биодизеля и мыла (Tan et al., 2013). Питательные среды также содержали 2 г / л дрожжевого экстракта, поскольку штамм является ауксотрофом L-триптофана. В этих условиях сконструированный штамм демонстрировал рост в течение 17 часов, затем он перешел в стационарную фазу, которая закончилась через 72 часа от общего времени культивирования. Наблюдалось, что накопление катехол меланина началось через 18 часов, очень близко к началу стационарной фазы.В конце культивирования из культуральной среды было извлечено 1,21 г / л катехол-меланина (таблица 1) (Mejía-Caballero et al., 2016). В конце культивирования наблюдали накопление 0,73 г / л катехола. Этот результат указывает на то, что скорость синтеза этого предшественника превышает способность MutMelA потреблять его. Следовательно, в этом случае повышение активности тирозиназы должно быть целью улучшения характеристик штамма.
Усилия в области метаболической инженерии для увеличения производства меланина до сих пор были сосредоточены на E.coli . Это результат накопленных знаний, связанных с разработкой центрального метаболизма и пути шикимата в этом организме. Для дрожжей Saccharomyces cerevisiae также проводится большой объем работ, связанных с рациональной модификацией метаболических путей для производства ароматических соединений. Некоторые из этих модификаций были направлены на увеличение поступления L-DOPA, поскольку это соединение является ранним промежуточным продуктом для синтеза бензилизохинолиновых алкалоидов (BIA).В одном сообщении с целью улучшения штамма S. cerevisiae для продукции BIAs была использована стратегия, основанная на использовании биосенсора, связанного с ферментом, и мутагенезе. Было обнаружено, что цитохром P450 L-DOPA-оксидаза CYP76AD1 из сахарной свеклы Beta vulgaris проявляет тирозингидроксилазную активность, что приводит к синтезу L-DOPA. Чтобы улучшить эту активность, была использована подверженная ошибкам ПЦР для создания мутантной библиотеки CYP76AD1. Идентификация мутантов с более высокой активностью была основана на визуальном обнаружении колоний, демонстрирующих самую высокую флуоресценцию, поскольку клетки экспрессируют фермент, который превращает L-DOPA в бетаксантин.На втором этапе перетасовка ДНК использовалась с генами шести изолированных улучшенных вариантов CYP76AD1 для объединения мутаций. Эта процедура позволила выделить мутантную версию CYP76AD1, которая показала 2,8-кратное увеличение титра L-DOPA по сравнению с ферментом дикого типа (DeLoache et al., 2015). В другом примере штамма S. cerevisiae были сконструированы для синтеза природных и новых BIA. Одновременная делеция zwf1 , кодирующая глюкозо-6-фосфатдегидрогеназу, повышающая регуляция TKL1 , кодирующая транскетолаза и экспрессия ARO4 Q 166 K , кодирующая устойчивую версию ингибирования мутанта с обратной связью ингибированной тирозином ДАГФ-синтазы улучшил эндогенное поступление L-тирозина, что привело к 60-кратному увеличению синтеза бензилизохинолинового каркаса.В попытке создать штамм для продукции норкоклаурина были введены дополнительные модификации, чтобы обеспечить синтез L-DOPA. Была выбрана BH 4 -зависимая тирозингидроксилаза из Rattus norvegicus . Оптимизированные по кодонам гены, кодирующие ферменты, участвующие в биосинтезе BH 4 и тирозингидроксилазу, были экспрессированы, что привело к синтезу 94,5 мкг / л L-DOPA.
Следует отметить, что эти усилия не были направлены исключительно на получение S.cerevisiae для продукции L-тирозина или L-DOPA. Таким образом, возможно дальнейшее улучшение производительности. Ожидается, что экспрессия фермента с тирозиназной активностью в этих штаммах должна приводить к продуцентам эумеланина. Интересно отметить сходства и различия в отношении целей метаболической инженерии при сравнении штаммов, продуцирующих L-тирозин или L-ДОФА E. coli и S. cerevisiae . Одно очевидное сходство заключается в необходимости экспрессии устойчивых к ингибированию обратной связи мутантных версий ферментов в ключевых точках ароматических путей биосинтеза.
Выводы и перспективы
Меланины — это класс натуральных продуктов, которые можно рассматривать как функциональные полимеры с множеством потенциальных применений в промышленности. Получение этих продуктов в больших масштабах, с определенным химическим составом и по относительно низкой цене является серьезной технической проблемой. Как обсуждается в этом обзоре, один из подходов в этом направлении может быть основан на выделении и использовании природных меланогенных микроорганизмов. Эта схема имеет ряд преимуществ, например, возможность разработки производственного процесса в относительно короткие сроки.Однако использование природных меланогенных организмов может иметь некоторые недостатки, такие как частая потребность в использовании сложных сред, которые необходимы для индукции выработки меланина. Использование сложных сред усложняет процедуры очистки, а также может привести к синтезу меланина с нежелательными химическими компонентами. Одно из решений этих проблем было основано на использовании генной инженерии для модификации экспрессии нативных генов, участвующих в меланогенезе, а также на создании новых меланогенных организмов.Накопленные знания о биохимии и генетике производства меланина в различных организмах сделали возможным прямое управление компонентами этого пути. Используя методы генетической и метаболической инженерии, стало возможным повысить синтетическую способность природных меланогенных организмов. Кроме того, были созданы новые меланогенные организмы, способные синтезировать меланины из простых источников углерода. Эти усилия привели к созданию штаммов и способов получения этих полимеров в граммах (таблица 1).
Основная генетическая модификация, используемая для создания или улучшения меланогенных организмов, включает сверхэкспрессию генов, кодирующих тирозиназы. Это часто основано на помещении гена тирозиназы под контроль индуцибельного промотора в репликативном плазмидном векторе. Эта стратегия позволяет точно контролировать величину и время экспрессии генов путем добавления индукторов, что позволяет оптимизировать производственный процесс. Однако использование экспрессионных плазмид, подобных тем, которые используются в рассмотренных здесь примерах, требует добавления антибиотиков в качестве селективного давления, чтобы избежать роста бесплазмидных клеток.Другой недостаток — требование включения химического индуктора в питательную среду. Использование антибиотиков и индукторов увеличивает производственные затраты и усложняет процедуры очистки. Этих проблем можно избежать, используя альтернативные методы отбора плазмид, не основанные на антибиотиках, а также методы индукции генов, не зависящие от добавления химикатов (Vidal et al., 2008).
В нескольких отчетах, рассмотренных здесь, можно заметить, что титры меланина и объемная продуктивность ниже в процессах, в которых производственный штамм был модифицирован метаболической инженерией для преобразования источников углерода в меланины по сравнению со штаммами, которые трансформируют предшественники меланина, представленные в питательная среда (таблица 1).Сообщенные титры и продуктивность эумеланина не соответствуют тем, которые наблюдаются для производства его предшественника L-тирозина (Santos et al., 2012). Это говорит о том, что все еще есть потенциал для улучшения деформации и производственного процесса. Потребуется дальнейшее развитие сконструированных штаммов, чтобы сделать их более конкурентоспособными.
Применение синтетической биологии, адаптивной лабораторной эволюции (ALE) и стратегий мутагенеза должно быть оценено для улучшения существующих штаммов, продуцирующих меланин (Bassalo et al., 2016). Использование ALE позволяет создавать сложные фенотипы. В одном отчете синтетический биосенсорный модуль, который реагирует на внутриклеточную концентрацию ароматических аминокислот, был объединен с ALE, чтобы обеспечить создание улучшенного штамма S. cerevisiae для производства муконовой кислоты (Leavitt et al., 2017). Этот штамм демонстрирует усиленный поток в общем пути ароматических аминокислот, поэтому его можно модифицировать для увеличения синтеза L-тирозина, следуя установленным методам.С такой модификацией штамм S. cerevisiae , разработанный в этом исследовании, мог бы стать подходящей платформой для синтеза эумеланина. В другом сообщении был разработан высокопроизводительный скрининг продукции L-тирозина путем сочетания синтеза этой аминокислоты с производством меланина в штамме E. coli , экспрессирующем тирозиназу MelA из R. etli (Santos and Стефанопулос, 2008). Этот метод был применен для идентификации штаммов E. coli с улучшенной производительностью L-тирозина.В этом исследовании E. coli был сконструирован путем применения рациональных стратегий метаболической инженерии, которые вызывают гиперпродукцию L-тирозина. Для дальнейшего улучшения способности к синтезу L-тирозина этот штамм подвергали глобальной инженерии транскрипционных машин (gTME) (Alper et al., 2006). Этот метод был реализован в E. coli путем экспрессии в сконструированном штамме двух отдельных библиотек gTME субъединиц РНК-полимеразы rpoA и rpoD . Улучшенные продуценты L-тирозина из этих двух библиотек были идентифицированы в чашках с агаром на основе пигментации меланина колонии.Были охарактеризованы три мутантных изолята, показывающих двукратное увеличение титра L-тирозина по сравнению с сконструированным родительским штаммом (Santos et al., 2012). Следует отметить, что в этом случае эти штаммы могут быть использованы непосредственно в процессе производства меланина из глюкозы.
В рамках характеристики штаммов, модифицированных для синтеза меланина из простого источника углерода, было определено, что активность тирозиназы является фактором, ограничивающим продуктивность (Chávez-Béjar et al., 2013; Mejía-Caballero et al., 2016). Возможно, что активность тирозиназы также может ограничивать выработку меланина в других сконструированных штаммах. Поэтому важно оценить ферменты тирозиназы из различных биологических источников, чтобы определить те, которые обладают желаемыми свойствами для биотехнологического применения. Обширные данные о геномах и метагеномах, доступные в настоящее время, должны предоставить большое количество генов, кодирующих предполагаемые тирозиназы, которые можно оценить экспериментально. Кроме того, применение белковой инженерии является жизнеспособным вариантом для улучшения этого класса ферментов.Эта методология еще не применялась в рамках стратегии по улучшению штамма, продуцирующего меланин. Одним из важных преимуществ работы с тирозиназами является простой анализ активности, основанный на продукции меланина, который позволяет использовать высокопроизводительные методы отбора (Santos and Stephanopoulos, 2008).
Несмотря на технический прогресс в разработке штаммов и процессов для производства меланина, многие основные вопросы все еще не решены. Один из важных вопросов связан с динамикой полимеризации меланина.Предполагается, что предшественники меланина синтезируются в цитозоле, затем эти молекулы покидают клетку и начинают полимеризоваться в культуральной среде. Полимер постепенно увеличивается в размере, образуя большое разнообразие молекул меланина. Интересно, что меланин, выделенный в разное время в производственных культурах, проявляет разные цвета от желтого до черного (Chávez-Béjar et al., 2013). Можно ожидать, что эти макромолекулы также будут обладать различными физико-химическими свойствами.Проведение исследований динамики полимеризации меланина в производственных культурах и свойств полимеров определенных размеров имеет большое значение, поскольку они могут дать полезную информацию, ведущую к выделению продуктов с определенными характеристиками.
Для использования в качестве биотехнологического продукта меланины должны быть извлечены из питательной среды и очищены. Общий метод экстракции и частичной очистки этих продуктов основан на низкой растворимости этих полимеров при низких значениях pH.Метод экстракции, которому следуют большинство авторов, начинается с удаления клеток из культуральной среды центрифугированием, а затем осаждения меланина путем доведения pH до 2,0–3,0 с помощью HCl в течение 4–16 часов при 4–25 ° C. Осажденный меланин центрифугируется, и его можно сушить в духовке при 45–70 ° C в течение 24 часов или сушить вымораживанием и хранить при 4 ° C. В качестве альтернативы осажденный меланин можно повторно растворить в воде при pH 8,0–9,0, и цикл осаждения и повторного растворения повторяется несколько раз с сушкой в качестве заключительного этапа.Сообщалось, что жидкостная хроматография с помощью Pharmacia Sephadex LH-20 является дополнительной стадией очистки эумеланина (Lin et al., 2005). Ожидается, что эти методы экстракции и очистки позволят получить меланины различной степени чистоты. Вероятно, что меланин, полученный с помощью ранее упомянутых процедур, может содержать различные количества белка и других клеточных компонентов. Однако до сих пор не существует общего стандарта для определения чистоты меланина для конкретных применений.
Как видно из рассмотренных здесь рукописей, большинство опубликованных работ по микробному производству меланина сосредоточено на эумеланине.Это понятно, поскольку этот полимер широко охарактеризован и является наиболее распространенным типом меланина, обнаруживаемым у людей. Следовательно, доступность эумеланина может привести к его применению в косметической и медицинской промышленности, а также в других технологических областях. Однако следует отметить, что меланины представляют собой химически разнообразную группу полимеров. Пока изучена лишь малая часть этого химического разнообразия. Сообщалось о процессах производства катехола, кофейной кислоты и протокатехуальдегидных меланинов, помимо эумеланина.Для конкретных приложений можно предположить, что разные типы меланинов будут демонстрировать разные характеристики. Действительно, в недавнем исследовании было показано, что меланин на основе протокатехуальдегида демонстрирует лучшие характеристики в качестве красителя в мягких контактных линзах по сравнению с эумеланином или меланином с кофейной кислотой (Ahn et al., 2019). Следует также отметить, что неприродные меланины можно получить, используя синтетические неприродные аминокислоты и другие соединения, которые могут использоваться в качестве субстратов для тирозиназ (della-Cioppa et al., 1990). Поэтому ожидаемое разнообразие полимеров этого типа очень велико. Разработка штаммов и процессов для получения новых природных и синтетических меланинов должна значительно увеличить количество применений этих ароматических полимеров.
Авторские взносы
LM, AM и GG участвовали в поиске и анализе информации для этого обзора, а также в написании и критическом обзоре рукописи.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
Ан, С. Ю., Чой, М., Чон, Д. В., Парк, С., Парк, Х., Джанг, К. С. и др. (2019). Синтез и анализ химического состава нового меланинового красителя на основе протокатехуальдегида методом 15T FT-ICR: высокая эффективность окрашивания мягких контактных линз. Красители и пигменты 160, 546–554. DOI: 10.1016 / j.dyepig.2018.08.058
CrossRef Полный текст | Google Scholar
Альпер, Х., Моксли, Дж., Невойгт, Э., Финк, Г. Р., и Стефанопулос, Г. (2006).Разработка оборудования для транскрипции дрожжей для улучшения толерантности к этанолу и его производства. Science 314, 1565–1568. DOI: 10.1126 / science.1131969
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Амбрико, М., Веккья, Н. Ф. Д., Амбрико, П. Ф., Кардоне, А., Чикко, С. Р., Лигонцо, Т. и др. (2014). Светочувствительный сополимер на основе полидофамина на основе рыжих волос для гибридных фотоемкостных датчиков. Adv. Функц. Матер. 24, 7161–7172. DOI: 10.1002 / adfm.201401377
CrossRef Полный текст | Google Scholar
Апте, М., Гирме, Г., Банкар, А., РавиКумар, А., и Зинджарде, С. (2013). Меланин, производный от 3,4-дигидрокси-L-фенилаланина из Yarrowia lipolytica , опосредует синтез наноструктур серебра и золота. Дж. Нанобиотехнологии 11: 2. DOI: 10.1186 / 1477-3155-11-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бальдерас-Эрнандес, В. Э., Сабидо-Рамос, А., Сильва, П., Кабрера-Валладарес, Н., Эрнандес-Чавес, Г., Баес-Виверос, Дж. Л. и др. (2009). Метаболическая инженерия для улучшения синтеза антранилата из глюкозы в Escherichia coli . Microb. Cell Fact. 8:19. DOI: 10.1186 / 1475-2859-8-19
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бальдерас-Эрнандес, В. Э., Тревиньо-Кинтанилья, Л. Г., Эрнандес-Чавес, Г., Мартинес, А., Боливар, Ф., и Госсет, Г. (2014). Биосинтез катехолов из глюкозы в штаммах Escherichia coli с избыточным продуцентом антранилата путем гетерологичной экспрессии антранилат 1,2-диоксигеназы из Pseudomonas aeruginosa PAO1. Microb. Cell Fact. 13: 136. DOI: 10.1186 / s12934-014-0136-x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бассало, М. К., Лю, Р., и Гилл, Р. Т. (2016). Направленные приложения эволюции и синтетической биологии к микробным системам. Curr. Opin. Biotechnol. 39, 126–133. DOI: 10.1016 / j.copbio.2016.03.016
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Bothma, J. P., de Boor, J., Divakar, U., Schwenn, P.Э. и Мередит П. (2008). Электропроводящие тонкие пленки меланина приборного качества. Adv. Матер. 20, 3539–3542. DOI: 10.1002 / adma.200703141
CrossRef Полный текст | Google Scholar
Кабрера-Валладарес, Н., Мартинес, А., Пинеро, С., Лагунас-Муньос, В. Х., Тиноко, Р., Де Анда, Р. и др. (2006). Экспрессия гена melA из Rhizobium etli CFN42 в Escherichia coli и характеристика кодируемой тирозиназы. Enzyme Microb.Technol. 38, 772–779. DOI: 10.1016 / j.enzmictec.2005.08.004
CrossRef Полный текст | Google Scholar
Чавес-Бехар, М. И., Бальдерас-Эрнандес, В. Э., Гутьеррес-Алехандре, А., Мартинес, А., Боливар, Ф., и Госсет, Г. (2013). Метаболическая инженерия Escherichia coli для оптимизации синтеза меланина из глюкозы. Microb. Cell Fact. 12: 108. DOI: 10.1186 / 1475-2859-12-108
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чавес-Бехар, М.И., Лара, А. Р., Лопес, Х., Эрнандес-Чавес, Г., Мартинес, А., Рамирес, О. Т. и др. (2008). Метаболическая инженерия Escherichia coli для продукции L-тирозина путем экспрессии генов, кодирующих домен хоризматмутазы нативной хоризматмутазы-префенатдегидратазы и циклогексадиенилдегидрогеназы из Zymomonas mobilis . Заявл. Environ. Microbiol. 74, 3284–3290. DOI: 10.1128 / AEM.02456-07
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Clusella-Trullas, S., ван Вик, Дж. Х., и Спотила, Дж. Р. (2007). Тепловой меланизм у эктотерм. Дж. Термал Биол . 32, 235–245. DOI: 10.1016 / j.jtherbio.2007.01.013
CrossRef Полный текст | Google Scholar
Коэльо, С. Г., Чжоу, Ю., Бушар, Х. Ф., Миллер, С. А., Змудзка, Б. З., Слушание, В. Дж. И др. (2009). Стойкая пигментация (LLP) кожи человека, новый взгляд на игнорируемую реакцию на УФ-излучение. Pigment Cell Melanoma Res. 22: 238–241. DOI: 10.1111 / j.1755-148X.2009.00550.х
CrossRef Полный текст | Google Scholar
Кордеро, Р. Дж., И Касадеваль, А. (2017). Функции грибкового меланина выходят за рамки вирулентности. Fungal Biol. Ред. 31, 99–112. DOI: 10.1016 / j.fbr.2016.12.003
CrossRef Полный текст | Google Scholar
Дадачева Е., Брайан Р. А., Хуанг X., Моадель Т., Швейцер А. Д., Айсен П. и др. (2007). Ионизирующее излучение изменяет электронные свойства меланина и усиливает рост меланизированных грибов. PLoS ONE 2: e457. DOI: 10.1371 / journal.pone.0000457
PubMed Аннотация | CrossRef Полный текст | Google Scholar
della-Cioppa, G., Garger, S.J., Sverlow, G.G., Turpen, T.H., и Grill, L.K. (1990). Производство меланина в Escherichia coli из клонированного гена тирозиназы. Биотехнология 8, 634–638. DOI: 10.1038 / nbt0790-634
PubMed Аннотация | CrossRef Полный текст | Google Scholar
DeLoache, W. C., Russ, Z. N., Наркросс, Л., Гонсалес, А. М., Мартин, В. Дж., И Дьюбер, Дж. Э. (2015). Биосенсор, связанный с ферментом, позволяет производить (S) -ретикулин дрожжами из глюкозы. Nat. Chem. Биол. 11: 465–471. DOI: 10.1038 / nchembio.1816
PubMed Аннотация | CrossRef Полный текст | Google Scholar
d’Ischia, M., Wakamatsu, K., Cicoira, F., Di Mauro, E., Garcia-Borron, J.C., Commo, S., et al. (2015). Меланины и меланогенез: от пигментных клеток до здоровья человека и технологических приложений. Pigment Cell Melanoma Res. 28, 520–544. DOI: 10.1111 / PCMr.12393
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ганеш Кумар, К., Саху, Н., Нарендер Редди, Г., Прасад, Р. Б. Н., Нагеш, Н., и Камаль, А. (2013). Производство пигмента меланина из Pseudomonas stutzeri , выделенного из красных морских водорослей Hypnea musciformis . Lett. Прил. Microbiol. 57, 295–302. DOI: 10.1111 / lam.12111
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гарсия-Молина, Ф., Муньос, Дж. Л., Варон, Р., Родригес-Лопес, Дж. Н., Гарсия-Кановас, Ф., и Тудела, Дж. (2007). Обзор спектрофотометрических методов измерения монофенолазной и дифенолазной активности тирозиназы. J. Agric. Food Chem. 55, 9739–9749. DOI: 10.1021 / jf0712301
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гибелло А., Феррер Э., Санс Дж. И Мартин М. (1995). Производство полимера Klebsiella pneumoniae Гены гидроксилазы 4-гидроксифенилуксусной кислоты клонированы в Escherichia coli . Заявл. Environ. Microbiol. 61, 4167–4171.
PubMed Аннотация | Google Scholar
Гласс, К., Ито, С., Уилби, П. Р., Сота, Т., Накамура, А., Бауэрс, К. Р. и др. (2012). Прямые химические доказательства пигмента эумеланина юрского периода. Proc. Natl. Акад. Sci. США 109, 10218–10223. DOI: 10.1073 / pnas.1118448109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гонсалес, В., Бустос, П., Рамирес-Ромеро, М.A., Medrano-Soto, A., Salgado, H., Hernández-González, I., et al. (2003). Мозаичная структура симбиотической плазмиды Rhizobium etli CFN42 и ее связь с другими компартментами симбиотического генома. Genome Biol. 4: R36. DOI: 10.1186 / GB-2003-4-6-r36
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Го, Дж., Рао, З., Ян, Т., Ман, З., Сюй, М., и Чжан, X. (2014). Высокий уровень продукции меланина новым изолятом Streptomyces kathirae . FEMS Microbiol. Lett. 357, 85–91. DOI: 10.1111 / 1574-6968.12497
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Го, Дж., Рао, З., Ян, Т., Ман, З., Сюй, М., Чжан, X., и др. (2015). Клонирование и идентификация новой тирозиназы и ее сверхэкспрессия в Streptomyces kathirae SC-1 для увеличения продукции меланина. FEMS Microbiol. Lett. 362: fnv041. DOI: 10.1093 / femsle / fnv041
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джалми, П., Бодке, П., Вахидуллах, С., и Рагхукумар, С. (2012). Грибок Gliocephalotrichum simplex как источник обильного внеклеточного меланина для биотехнологических применений. World J. Microbiol. Biotechnol. 28, 505–512. DOI: 10.1007 / s11274-011-0841-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джанг, С., Ганг, Х., Ким, Б. Г., и Чой, К. Ю. (2018). FCS и ECH-зависимое производство фенольного альдегида и пигмента меланина из l-тирозина в Escherichia coli . Enzyme Microb. Technol. 112, 59–64. DOI: 10.1016 / j.enzmictec.2017.10.011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ким, Ю. Дж., Ву, В., Чун, С. Е., Уитакр, Дж. Ф., и Беттингер, К. Дж. (2013). Биологически полученные меланиновые электроды в водных накопителях энергии иона натрия. Proc. Natl. Акад. Sci. США 110, 20912–20917. DOI: 10.1073 / pnas.1314345110
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Койке, К., и Эбато, А. (2013). Однокомпонентные составы краски для волос, содержащие соединения индола . Японское издание Tokkyo Koho 2013, JP5363703B220131211.
Google Scholar
Лагунас-Муньос, В. Х., Кабрера-Валладарес, Н., Боливар, Ф., Госсет, Г., и Мартинес, А. (2006). Оптимальное производство меланина с использованием рекомбинантной Escherichia coli . J. Appl. Microbiol. 101, 1002–1008. DOI: 10.1111 / j.1365-2672.2006.03013.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ливитт, Дж.М., Вагнер, Дж. М., Ту, К. К., Тонг, А., Лю, Ю., и Альпер, Х. С. (2017). Направленная эволюция с помощью биосенсора для улучшения продукции муконовой кислоты у Saccharomyces cerevisiae . Biotechnol. J. 12: 1600687. DOI: 10.1002 / biot.201600687
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лин, В. П., Лай, Х. Л., Лю, Ю. Л., Чиунг, Ю. М., Шиау, К. Ю., Хан, Дж. М. и др. (2005). Влияние меланина, продуцируемого рекомбинантной Escherichia coli , на антибактериальную активность антибиотиков. J. Microbiol. Иммунол. Заразить. 38, 320–326.
PubMed Аннотация | Google Scholar
Линдгрен, Дж., Мойер, А., Швейцер, М. Х., Шевалл, П., Увдал, П., Нильссон, Д. Э. и др. (2015). Интерпретация окраски на основе меланина через глубокое время: критический обзор. Proc. R. Soc. B Biol. Sci. 282: 20150614. DOI: 10.1098 / rspb.2015.0614
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лю, Ю. К., Чен, С. М., Лю, Дж. Х., Сюй, Х. В., Лин, Х. Ю., Чен, С. Ю. (2015). Механические процессы и процессы фотофрагментации для нанонизации меланина с целью повышения его эффективности в защите клеток от стресса, связанного с активными формами кислорода. J. Appl. Phys. 117: 064701. DOI: 10.1063 / 1.4
7CrossRef Полный текст | Google Scholar
Лопес-Серрано, Д., Солано, Ф., и Санчес-Амат, А. (2004). Идентификация оперона, участвующего в активности тирозиназы и синтезе меланина, у Marinomonas mediterranea . Ген 342, 179–187. DOI: 10.1016 / j.gene.2004.08.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мадхусудхан, Д. Н., Мазари, Б. Б. З., Дастагер, С. Г., и Агсар, Д. (2014). Продукция и цитотоксичность внеклеточного нерастворимого и капелек растворимого меланина Streptomyces lusitanus DMZ-3. Biomed Res. Int. , 2014: 306895. DOI: 10.1155 / 2014/306895
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Манивасаган, П., Венкатесан, Дж., Сивакумар, К., и Ким, С. К. (2013). Актинобактериальные меланины: текущее состояние и перспективы на будущее. World J. Microbiol. Biotechnol. 29, 1737–1750. DOI: 10.1007 / s11274-013-1352-y
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мехиа-Кабальеро, А., де Анда, Р., Эрнандес-Чавес, Г., Рогг, С., Мартинес, А., Боливар, Ф. и др. (2016). Биосинтез катехол-меланина из глицерина с использованием метаболически сконструированного Escherichia coli . Microb. Cell Fact. 15: 161. DOI: 10.1186 / s12934-016-0561-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Монтефиори, Д. К., и Чжоу, Дж. (1991). Селективная противовирусная активность синтетических растворимых L-тирозина и меланинов L-допа против вируса иммунодефицита человека in vitro . Antiviral Res. 15, 11–25. DOI: 10.1016 / 0166-3542 (91)-R
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Никодинович-Руник, Я., Мартин, Л. Б., Бабу, Р., Блау, В., и О’Коннор, К. Э. (2009). Характеристика мутантов-транспозонов Pseudomonas putida F6, сверхпродуцирующих меланин. FEMS Microbiol. Lett. 298, 174–183. DOI: 10.1111 / j.1574-6968.2009.01716.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Нофсингер, Дж. Б., Лю, Ю., и Саймон, Дж. Д. (2002). Агрегация эумеланина снижает фотогенерацию активных форм кислорода. Free Radic. Биол. Med. 32, 720–730.DOI: 10.1016 / S0891-5849 (02) 00763-3
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Папроски Р. Дж., Ли Ю., Барбер К., Льюис Дж. Д., Кэмпбелл Р. Э. и Земп Р. (2015). Проверка гомолога тирозиназы melA в качестве фотоакустического репортерного гена для визуализации Escherichia coli . J. Biomed. Опт. 20: 106008. DOI: 10.1117 / 1.JBO.20.10.106008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Патель, К. Р., Вайман, Дж.А., Патель, К. А., и Бёрден, Б. Дж. (1996). Мутант Bacillus thuringiensis , продуцирующий темно-коричневый пигмент с повышенной устойчивостью к ультрафиолету и инсектицидной активностью. J. Invertebr. Патол. 67, 120–124. DOI: 10.1006 / jipa.1996.0018
CrossRef Полный текст | Google Scholar
Патил С., Систла С., Бапат В. и Джадхав Дж. (2018). Опосредованный меланином синтез наночастиц серебра и их сродство к тирозиназе. Заявл. Biochem. Microbiol. 54, 163–172. DOI: 10.1134 / S0003683818020096
CrossRef Полный текст | Google Scholar
Пиньеро, С., Ривера, Дж., Ромеро, Д., Севаллос, М.А., Мартинес, А., Боливар, Ф. и др. (2007). Тирозиназа из Rhizobium etli участвует в эффективности клубеньков и устойчивости к стрессам, связанным с симбиозом. J. Mol. Microbiol. Biotechnol. 13, 35–44. DOI: 10.1159 / 000103595
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Прието, М.А., Перес-Аранда А. и Гарсия Дж. Л. (1993). Характеристика ароматической гидроксилазы Escherichia coli с широким диапазоном субстратов. J. Bacteriol. 175, 2162–2167. DOI: 10.1128 / jb.175.7.2162-2167.1993
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Раман, Н. М., Шах, П. Х., Мохан, М., и Рамасами, С. (2015). Повышение производства меланина из Aspergillus fumigatus AFGRD105 за счет оптимизации факторов среды. AMB Express 5:72.DOI: 10.1186 / s13568-015-0161-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Розановска, М., Сарна, Т., Лэнд, Э. Дж., И Траскотт, Т. Г. (1999). Свойства меланина улавливать свободные радикалы: взаимодействие моделей eu- и pheo-меланина с восстанавливающими и окислительными радикалами. Free Radic. Биол. Med. 26, 518–525. DOI: 10.1016 / S0891-5849 (98) 00234-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Руан, Л., Хе, В., Хе, Дж., Сан, М., Ю, З. (2005). Клонирование и экспрессия гена mel из Bacillus thuringiensis в Escherichia coli . Антони Ван Левенгук 87, 283–288. DOI: 10.1007 / s10482-004-4775-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Жуань, Л., Ю, З., Фанг, Б., Хе, В., Ван, Ю., и Шен, П. (2004). Образование пигмента меланина и повышение устойчивости к ультрафиолетовому излучению у Bacillus thuringiensis после индукции при высокой температуре. Syst. Прил. Microbiol. 27, 286–289. DOI: 10.1078 / 0723-2020-00265
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шайни, А.С., Мело, Дж. С. (2013). Биосорбция урана меланином: кинетические, равновесные и термодинамические исследования. Биоресурсы. Technol. 149, 155–162. DOI: 10.1016 / j.biortech.2013.09.034
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шайни, А.С., Мело, Дж. С. (2015). Зеленый синтез эумеланина в одном горшке: оптимизация процесса и его характеристика. RSC Adv. 5, 47671–47680. DOI: 10.1039 / C5RA01962A
CrossRef Полный текст | Google Scholar
Сантос, К. Н. С. и Стефанопулос, Г. (2008). Высокопроизводительный скрининг на основе меланина для производства L-тирозина в Escherichia coli . Заявл. Environ. Microbiol. 74, 1190–1197. DOI: 10.1128 / AEM.02448-07
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сантос, С. Н., Сяо, В., и Стефанопулос, Г. (2012).Рациональный, комбинаторный и геномный подходы к разработке продукции L-тирозина в Escherichia coli . Proc. Natl. Акад. Sci. США 109, 13538–13543. DOI: 10.1073 / pnas.1206346109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сарна Т., Хайд Дж. С. и Шварц Х. М. (1976). Ионный обмен в меланине: исследование электронного спинового резонанса с зондами лантаноидов. Science 192, 1132–1134. DOI: 10.1126 / science.179142
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шанмуганатан, К., Чо, Дж. Х., Айер, П., Барановиц, С., Эллисон, К. Дж. (2011). Термоокислительная стабилизация полимеров с использованием природных и синтетических меланинов. Макромолекулы 44, 9499–9507. DOI: 10.1021 / ma202170n
CrossRef Полный текст | Google Scholar
Сурвасе, С. Н., Джадхав, С. Б., Фугаре, С. С., и Джадхав, Дж. П. (2013). Оптимизация производства меланина с помощью Brevundimonas sp. SGJ с использованием методологии поверхности отклика. 3 Biotech 3, 187–194. DOI: 10.1007 / s13205-012-0082-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тан, Х. В., Азиз, А. А., Ароуа, М. К. (2013). Производство глицерина и его применение в качестве сырья: обзор. Обновить. Поддерживать. Energy Rev. 27, 118–127. DOI: 10.1016 / j.rser.2013.06.035
CrossRef Полный текст | Google Scholar
Тарангини, К., Мишра, С. (2014). Производство меланина почвенным микробным изолятом на экстракте фруктовых отходов: двухэтапная оптимизация основных параметров. Biotechnol. Rep. 4, 139–146. DOI: 10.1016 / j.btre.2014.10.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Триас, Дж., Виньяс, М., Гвинея, Дж., И Лорен, Дж. Г. (1989). Коричневая пигментация в культурах Serratia marcescens связана с метаболизмом тирозина. Банка. J. Microbiol. 35, 1037–1042. DOI: 10,1139 / m89-172
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вальдеррама, Б., Оливер, П., Медрано-Сото А. и Васкес-Духальт Р. (2003). Эволюционное и структурное разнообразие лакказ грибов. Антони Ван Левенгук 84, 289–299. DOI: 10.1023 / A: 1026070122451
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ваврика, К. Дж., Хан, К., Мехере, П., Динг, Х., Кристенсен, Б. М., и Ли, Дж. (2014). Ферменты метаболизма тирозина насекомых и млекопитающих: сравнительная перспектива. Insect Sci. 21, 13–19. DOI: 10.1111 / 1744-7917.12038
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Видаль, Л., Пинсах, Дж., Стриднер, Г., Каминал, Г., и Феррер, П. (2008). Разработка системы отбора плазмид без антибиотиков, основанной на ауксотрофии глицина, для избыточной продукции рекомбинантного белка в Escherichia coli . J. Biotechnol. 134, 127–136. DOI: 10.1016 / j.jbiotec.2008.01.011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уильямс, Р.Ф. (1994). Агенты на основе меланина для улучшения изображения . Патент США № 5310539.
Google Scholar
Вогелиус Р. А., Мэннинг П. Л., Барден Х. Э., Эдвардс Н. П., Уэбб С. М., Селлерс В. И. и др. (2011). Следы металлов как биомаркеры пигмента эумеланина в летописи окаменелостей. Science 333, 1622–1626. DOI: 10.1126 / science.1205748
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Яновский, К., Хорн, В., Боннер, М., и Стасевский, С. (1971). Полярность и функции ферментов у мутантов первых трех генов триптофанового оперона Escherichia coli . Генетика 69, 409.
PubMed Аннотация | Google Scholar
Zhang, F., Kearns, S.L., Orr, P.J., Benton, M.J., Zhou, Z., Johnson, D., et al. (2010). Окаменелые меланосомы и окраска меловых динозавров и птиц. Nature 463, 1075–1078. DOI: 10.1038 / nature08740
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжао, С.Х., Тонг-Суо М.А. (2012). Высокий выход продукции меланина штаммом Rhizobium sp. R 593 в жидком состоянии ферментации. Asian J. Chem. 24, 335–338.
Google Scholar
5.1D: Цвет кожи — Medicine LibreTexts
- Последнее обновление
- Сохранить как PDF
- ЦЕЛЬ ОБУЧЕНИЯ
- Ключевые выводы
- Ключевые моменты
- Ключевые термины
- Меланин
- Как определяется цвет кожи
- Роль кератиноцитов
- Другие детерминанты цвета кожи
Цвет кожи во многом определяется количество пигмента меланина, продуцируемого меланоцитами кожи.
ЦЕЛЬ ОБУЧЕНИЯ
Объясните, как образуются разные степени пигментации
Основные выводы
Ключевые точки
- Цвет кожи в основном определяется пигментом под названием меланин.
- Меланин вырабатывается меланоцитами в процессе, называемом меланогенезом.
- Разница в цвете кожи у людей со светлой и темной пигментацией обусловлена уровнем активности меланоцитов; это не связано с количеством меланоцитов в их коже.
Ключевые термины
- меланин : Любой из группы встречающихся в природе темных пигментов, отвечающих за цвет кожи.
- меланоцит : клетка в коже, вырабатывающая пигмент меланин.
- кератиноцитов : клетки, которые поглощают и хранят меланин.
- эумеланин : Тип меланина, в основном отвечающий за коричневую и черную кожу.
- stratum basale : Эпидермальный слой, в котором находятся меланоциты.
Меланин
Цвет кожи в значительной степени определяется пигментом под названием меланин, но здесь также присутствуют и другие факторы. Ваша кожа состоит из трех основных слоев, самый поверхностный из которых называется эпидермисом. Сам эпидермис состоит из нескольких слоев.
Меланоциты: Поперечный срез кожи с меланином в меланоцитах
Самый глубокий из эпидермальных слоев называется базальным слоем или зародышевым слоем.В этом слое лежат важные клетки, называемые меланоцитами. Их название происходит от двух частей: мелано-, что означает черный или темный цвет, и -цит, что означает клетка.
Меланоциты — это клетки неправильной формы, которые производят и накапливают пигмент под названием меланин. Самый распространенный тип меланина — эумеланин. Этот пигмент хранится в органеллах, называемых меланосомами.
Эумеланин отвечает за коричневую и черную пигментацию кожи человека или ее отсутствие, если вырабатывается мало.Производство меланина называется меланогенезом — генез означает образование или развитие.
Как определяется цвет кожи
Независимо от происхождения, у каждого человека в основном одинаковое количество меланоцитов, но генетика каждого человека определяет, сколько меланина вырабатывается и как он распределяется по коже. Например, у людей со светлой кожей могут быть более темные места, такие как соски и родинки. И наоборот, у темнокожих людей ладони имеют более светлый оттенок.
Другой важный фактор, воздействие солнечного света, также запускает производство меланина. Это то, что дает нам загар. Меланин, вырабатываемый в ответ на солнечные лучи, защищает нашу кожу и остальное тело от вредного воздействия солнечных ожогов и вызывающего рак ультрафиолетового излучения. радиация.
Роль кератиноцитов
У людей с более темной кожей меланоциты активнее, чем у людей со светлой кожей. Однако пигмент нашей кожи также включает самые многочисленные клетки нашего эпидермиса — кератиноциты.
В то время как меланоциты производят, хранят и выделяют меланин, кератиноциты являются крупнейшими реципиентами этого пигмента. Перенос меланина от меланоцитов к кератиноцитам происходит благодаря длинным щупальцам, каждый меланоцит простирается до 40 кератиноцитов.
Если человек не может производить меланин, он страдает альбинизмом.
Другие детерминанты цвета кожи
Загорелая кожа: Воздействие УФ-излучения в результате загара вызывает изменения пигментации кожи за счет увеличения выработки меланина.
Помимо меланина, на общий или местный цвет кожи играют роль и другие факторы. К ним относятся:
- Количество каротина, обнаруженного в роговом слое эпидермиса и в самом глубоком слое кожи, в гиподерме. Каротин — это желто-оранжевый пигмент, содержащийся в моркови. Ваша кожа может стать этого цвета, если вы едите много продуктов, богатых каротином. Кожа может пожелтеть из-за другого фактора, называемого желтухой или желтухой, который возникает при серьезном заболевании печени. В этом случае желчные пигменты откладываются в коже и придают ей желтый цвет.
- Количество насыщенного кислородом гемоглобина, обнаруженного в кровеносных сосудах среднего слоя нашей кожи, дермы. Гемоглобин — это железосодержащий белковый пигмент наших клеток крови. Недостаток насыщения кислородом придает коже более бледный, серый или синий цвет. Кожа также может стать бледнее в результате анемии (пониженного количества гемоглобина и / или эритроцитов), низкого кровяного давления или плохого кровообращения.
- И наоборот, у людей со светлой кожей (по сравнению с темнокожими) кожа может быть розовой благодаря относительно более богатому кислородом гемоглобину, протекающему по кровеносным сосудам их дермы.Кожа красного цвета также может появиться в результате расширения (расширения) кровеносных сосудов в коже или рядом с ней из-за смущения, лихорадки, аллергии или воспаления.
- Наконец, на коже могут быть красные, черные, синие, пурпурные и зеленые синяки — все в результате утечки крови в окружающие ткани.


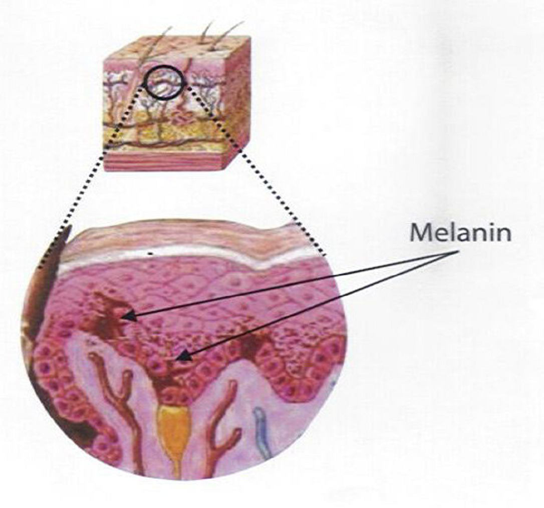
 nlm.nih.gov/16988713/
nlm.nih.gov/16988713/ Доступно по адресу: https://www.ncbi.nlm.nih.gov/books/NBK459156/.
Доступно по адресу: https://www.ncbi.nlm.nih.gov/books/NBK459156/.